
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ii II II
|
|
|
|
O O O
II II
O O
Смешанные кетоны получают из смесей кальциевых солей двух различных кислот. Такую смесь можно представит как смешанную соль.
Например, чтобы получить метилэтилкетон, надо взять кальциевую соль уксусной и пропионовой кислот:
3СН3—С—О—Са—О—С—СН2—СН3 ¾® 3СаСО3 +
кальциевая соль уксусной и пропионовой кислот
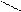
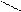
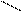 СH3 CH3 CH3—CH2
СH3 CH3 CH3—CH2
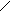
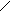
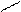 + C=O + C=O + C=O
+ C=O + C=O + C=O
CH3—CH2 CH3 CH3—CH2
метилэтилкетон диметилкетон диэтилкетон
Как видно из уравнения, наряду со смешанным кетоном в качестве побочных продуктов образуются два симметричных кетона. Если исходить из смеси, в которой одна из кальциевых солей – соль муравьиной кислоты, то могут быть получены соответствующие альдегиды. Например:
СН3—С—О—Са—О—С—Н ¾® СН3—С—Н + СаСО3
кальциевая соль муравьиной и уксусный альдегид
уксусной кислот
Не трудно понять, что в качестве побочных продуктов при этом образуется муравьиный альдегид Н2С=О и симметричный кетон (в данном случае диметилкетон). В описанных реакциях могут быть использованы и бариевые соли кислот.
Отдельные представители альдегидов и кетонов
Формальдегид СН2=О (муравьиный альдегид, метаналь).
Представляет собой бесцветное горючее вещество с острым раздражающим запахом. Ткип. = –19,2 оС, Тпл. = –92 оС, Температура самовоспламенения 430 оС, область воспламенения 7,73 % объемных. (Тушить тонкораспыленной водой, воздушно-механической пеной на основе ПО-11.) Растворим в воде, обычно используется в виде 33-40 % водного раствора, который называют формалином. Газообразный формальдегид самопроизвольно полимеризуется, образуя тример состава (СН2О)3, Тпл.= 62 оС, циклического строения, подобный тримеру уксусного альдегида, но не содержащий боковых метилных групп. При длительном стоянии водных растворов формальдегида, особенно при низких температурах, а также при упаривании в них осаждается белый осадок – полимер формальдегида состава (СН2О)n, который называют параформальдегидом (или параформом). Он представляет собой смесь низкомолекулярных полиформальдегидов с величиной n от 10 до 50. При нагревании до 140-160 оС параформальдегид деполимеризуется и превращается в газообразный формальдегид; процесс ускоряется в присутствии кислот.
В промышленности формальдегид обычно получают из метилового спирта; пары спирта в смеси с воздухом пропускают через контактный аппарат с раскаленной медной спиралью:
О2
2СН3—ОН ¾® 2СН2=О + 2Н2О
метанол Cu формальдегид
Образующийся формальдегид улавливают в воду. Другой важный способ получения формальдегида заключается в неполном окислении кислородом воздуха метана, входящего в состав природных газов. Процесс ведут в присутствии катализаторов (соединения Mn и Cu) при температуре около 400 оС:
СН4 + О2 ¾® СН2=О + Н2О
|
|
|
Дата добавления: 2013-12-12; Просмотров: 395; Нарушение авторских прав?; Мы поможем в написании вашей работы!