
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Аминокислоты и белки
|
|
|
|
XII. Белки
Белки – важнейший класс природных полимеров.
Существуют три основных класса биополимеров: полисахариды, нуклеиновые кислоты и белки.
Белки по химической природе являются полиамидами, построенные из аминокислот. В образовании белка участвует около двадцати аминокислот. Это так называемые основные, или белокобразующие (протеиногенные), аминокислоты.
В зависимости от вида радикала основные аминокислоты делят на три группы:
1) Неполярные (аланин, метионин, валин, про-лин, лейцин, изолейцин, триптофан, фенилаланин);
2) Полярные незаряженные (аспарагин, глутамин, серии, глицин, тирозин, треонин, цистеин);
3) Полярные заряженные (аргинин, гистидин, лизин — положительно; аспарагиновая и глутаминовая кислоты — отрицательно).
Общая формула аминокислот:
 |

 α O
α O
 R – CH – C
R – CH – C
| OH
NH2
Некоторые аминокислоты, входящие в состав белков:
1. Глицин (гликокол или аминоуксусная кислота);
H2C– COOH
|
NH2
2. Аланин (α-аминопропионовая кислота);
H3C – CH – COOH
|
NH2
3. Валин * (α-аминоизовалериановая кислота);
H3C – CH – CH – COOH
| |
CH3 NH2
4. Серин (α-амино-β-оксипропионовая кислота или α-амино-β-гидроксипропионовая кислота);
H2C – CH – COOH
| |
OH NH2
5. Цистеин (α-амино-β-тиопропионовая кислота или α-амино-β-сульфгидрилпропионовая кислота);
H2C – CH – COOH
| |
SH NH2
6. Двухосновные аминокислоты;
6.1. Аспарагиновая кислота (α-аминоянтарная кислота);
HOOC – CH2 – CH – COOH
|
NH2
6.2. Глутаминовая кислота (α-аминоглутаровая кислота).
HOOC – CH2 – CH2 – CH – COOH
|
NH2
7. Одноосновные диаминокислоты;
Лизин (2,6-диаминогексановая кислота или α,ε-диаминокапроновая кислота)
NH2 – (CH2)4 – CH – COOH
|
NH2
8. Двухосновные диаминокислоты.
Цистин* (β,β’-дитио-α-аминопропионовая кислота или ди-β-тио- α-аминопропионовая кислота, или 3,3’-дитио-бис-2-аминопропионовая кислота, или дицистеин). Цистин является дисульфидом цистиена.
HOOC – CH – CH2 – S – S – CH2 – CH – COOH
| |
NH2 NH2
Все природные кислоты (кроме глицина) имеют ассиметричный атом углерода и обладают оптической активностью. Оптически активные вещества существуют в виде двух изомерных форм (энантиомеры): L- (левовращающаяся) и D- (правовращающаяся). Молекулы относятся друг к другу как объект и его зеркальное изображение. Все природные белки построены только из L-аминокислот.
Получение глицина
1. Из уксусной кислоты;
|
|

 H3C – COOH + Cl2 H2C – COOH H2C – COOH
H3C – COOH + Cl2 H2C – COOH H2C – COOH
| |
C l NH2
2. Из формальдегида.
|

|
 О
О
 HC + HCN HO – CH2 – CN H2N–CH2 –С
HC + HCN HO – CH2 – CN H2N–CH2 –С  N H2C – COOH
N H2C – COOH
Н гидроксиацетонитрил |
NH2
Во всех аминокислотах есть группы [NH2] и [COOH], которые вступают в характерные для них реакции.

 R – CH – COO¯ R – CH – COOH
R – CH – COO¯ R – CH – COOH
| |
NH3 NH2
|
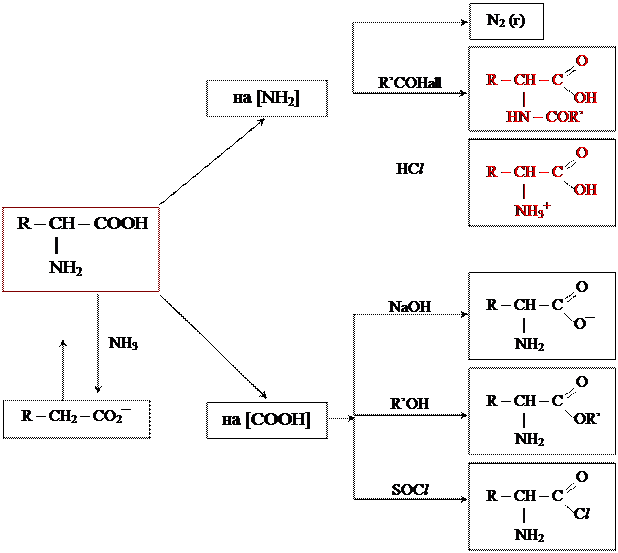

В кислых растворах аминокислоты присоединяют протоны (протонируют).
Аминогруппа → до NH3+
В щелочах → до CO2¯
В промежуточных значениях pH аминокислоты образуют биполярные ионы (цвиттер-ионы).
R – CH – CO2¯
|
NH3+
|

 измененная структуру (денатурация).
измененная структуру (денатурация).
|
 смесь аминокислот
смесь аминокислот
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 744; Нарушение авторских прав?; Мы поможем в написании вашей работы!