
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Natrii citras pro injectionibus. Натрия цитрат для инъекций
Calcii gluconas. Кальция глюконат
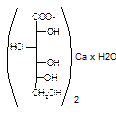
Описание: белый зернистый или кристаллический порошок без запаха и вкуса
Растворимость: умеренно медленно растворим в холодной воде, легко растворим в горячей с образованием мутного раствора, практически нерастворим в спирте и эфире.
Получение: окисление глюкозы в присутствии CaBr2, CaCl2
Подлинность: ИКС, характерные реакции на кальций; при добавлении к раствору препарата хлорида окисного железа появляется светло-зеленое окрашивание.
Чистота: Прозрачность в сравнении с эталоном, рН 6-7, галогены – Cl-, Br-, SO42-, тяж. Ме – допустимы, потеря в массе при высушивании – 1%.
Специфические – декстрин, сахароза. Препарат растворяют при нагревании в смеси из 2 мл разведенной соляной кислоты и 10 мл воды и кипятят 2 минуты. К охлажденному раствору приливают постепенно 8 мл раствора карбоната натрия и через 5 минут фильтруют (CaCO3). 5 мл фильтрата кипятят в течение 1 минуты с 2 мл реактива Фелинга; не должно наблюдаться образование красного осадка
Количественноеопределение: прямая комплексонометрия. Расчет на кристаллогидрат.
Хранение: сухое место
Применение: источник кальция, антиаллергическое средство.
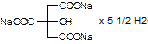
Описание: белые кристаллы или кристаллический порошок без запаха, выветривающиеся на воздухе
Растворимость: легко – в воде, практически нерастворим в спирте
Получение: взаимодействие лимонной кислоты с карбонатом Nа. Полученную соль перекристаллизовывают из спирта.
Подлинность: ИКС, реакция А на цитраты (с хлоридом кальция):
2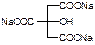 + 3CaCl2
+ 3CaCl2 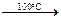 (
(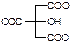 )2Ca3 + 6NaCl
)2Ca3 + 6NaCl
Осадок растворим в HCl.
Реакции на Na.
Нефармакопейные:
1. Реакция Б на цитраты: при нагревании цитрата с уксусным ангидридом через 20-40 секунд развивается карминово-красное окрашивание
2. Реакция Штаре:
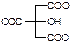
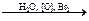 CO2 + HOOC-CH2-CO-CH2-COOH
CO2 + HOOC-CH2-CO-CH2-COOH 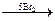 2CO2 + 5HBr + Br2CH-CO-CHBr2
2CO2 + 5HBr + Br2CH-CO-CHBr2
Выпадает белый кристаллический осадок.
3. С реактивом Денеже: свежеприготовленный раствор основного сульфата ртути.
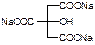 + KMnO4
+ KMnO4 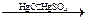
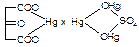
Чистота: раствор должен быть прозрачным и бесцветным; рН 7,8-8,3; недопустимы As (III), допустимы общие.
Специфические: тартраты – насыщенный раствор + ацетатный буфер – раствор должен быть прозрачен.
Оксалаты: навеску растворяют в воде, прибавляют HCl, спирт и CaCl2, оставляют на час, раствор должен остаться прозрачным.
Потеря в массе при выслушивании – 25-28%, микробиологическая чистота
Количественноеопределение: неводное титрование
1. HClO4 + CH3COOH «ClO4- + CH3COOH2+
2. натрия цитрат + 3CH3COOH «3Na+ + 3CH3COO- + лимонная кислота
3. CH3COO- + CH3COOH2+ à 2CH3COOH
4. Na+ + ClO4-«NaClO4
f=1/3
ГФX: ионобменная хроматография
Цитарт натрия + [катионит]Н+ à [катионит]3Na+ + лимонная кислота.
Титруют NaOH с фенолфталеином. f=1/3.
Нефармакопейные:
1. Прямая ацидиметрия:
натрия цитрат + 3HCl 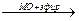 3 NaCl + лимоннам кислота.
3 NaCl + лимоннам кислота.
f=1/3
2. Обратная аргентометрия:
натрия цитрат + 3AgNO3 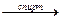 цитрат серебра¯ + 3NaOH
цитрат серебра¯ + 3NaOH
Избыток нитрата серебра оттитровывают роданометрически (NH4SCN).f=1/3
3. Образование комплекса с медью – прямая куприметрия (CuSO4) с мурексидом.
Хранение: сухое прохладное место
Применение: консервант препаратов крови.
Natrii oxybutyras. Натрия оксибутират. HO-CH2-CH2-CH2-COONa
Описание: белый с желтоватым оттенком гигроскопичный порошок. ЛР в воде, Р в спирте, ПНР в эфире, хлороформе.
Получение: из g-бутиролактона (специфическая примесь)
Подлинность:ИКС, Б – на Na; лактона – гидроксамовая проба
Количественноеопределение: неводное титрование f=1; прямая ацидиметрия f=1.
Хранение: список Б, в сухом, защищенном от света месте.
Применение: снотворное, неингаляционный наркоз, порошки, ампулы, сиропы, концентрат (66,7%).
Lithii oxybutyras. HO-CH2-CH2-CH2-COOLi
Подлинность: окрашивает пламя в фиолетовый цвет, рефрактометрия.
Количественное определение: неводное титрование.
Хранение: список Б
Применение: в психиатрии.
|
Дата добавления: 2013-12-12; Просмотров: 1278; Нарушение авторских прав?; Мы поможем в написании вашей работы!