
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Алкалиметрия
|
|
|
|
Методы количественного определения АК.
1. Метод Кьельдаля.
Точную навеску АК, смешивают с порошком K2SO4, CuSO4 (10:1). К полученой смеси прибавляют H2SO4. Проводят реакцию в колбе Кьельдаля, соединенной с холодильником и специальным приемником. При нагреве идет минерализация:
CàCO2; NàNH3à(NH4)2SO4
Нагревают до полного просветления раствора, затем колбу охлаждают, прибавляют NaOH. Идет процесс нейтрализации избытка H2SO4, разрушение аммониевой соли.
H2SO4 + NaOH à Na2SO4 + H2O
(NH4)2SO4 + NaOH à Na2SO4 + NH3 + H2O
Аммиак в специальном приемнике реагирует с борной кислотой:
2NH3 + 4H3BO3 à (NH4)2B4O7 + 5H2O
Титруют HCl в присутствии м/о + м/с. Разрушается тетраборат с образованием H3BO4 + NH4Cl.
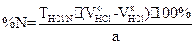
RCH2-CH(NH2)-COOH + NaOH 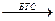 R-CH2-CH(NH2)-COONa + H2O
R-CH2-CH(NH2)-COONa + H2O
Наличие группы -NH2 затрудняет метод, ослабляя кислотные свойства аминокислоты.
3. Формольное титрование по Беренсену.
R-CH(NH2)-COOH + HCHO à RCH2-CH(N=CH2)-COOH 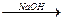 RCH2-CH(N=CH2)-COONa + H2O
RCH2-CH(N=CH2)-COONa + H2O
4. Неводное титрование (по -NH2 группе).
Титруют в ледяной уксусной кислоте раствором HClO4 как основание (по аминогруппе). Индикатор – кристаллический фиолетовый (смотри неводное титрование).
5. Газометрический метод Ван-Слейка.
При прибавлении к АК фиксированного количества NaNH2 и HCl, происходит выделение N2, который определяют газометрически (ГЖХ). По объему азота рассчитывают содержание АК.
Препараты:
Acidum glutaminicum - a-аминоглутаровая кислота.
HOOC-CH2-CH2-CH(HN2)-COOH
Описание: белый, кристаллический порошок, со слабым запахом, хорошо растворим в горячей воде.
Получение: из аминослянного эфира (ниже приведена упрощенная схема):
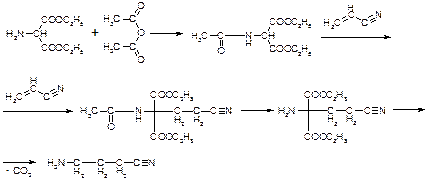
Подлинность:
1. Удельный угол вращения a
2. Нингидриновая проба.
3. Образование медных солей в щелочной среде.
4. С резорцином.

Наблюдается зеленая флюоресценция. Эта реакция специфична для глютаминовой кислоты.
Количественное определение:
1. Методом Кьельдаля.
2. Нейтрализация щелочи в водной среде с бромтимоловым синим.
HOOC-CH2-CH2-CH(NH2)-COOH + NaOH à NaOOC-CH2-CH2-CH(NH3+)-COO- + H2O
При использовании HCHO:
HOOC-CH2-CH2-CH(NH2)-COOH 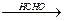 HOOC-CH(N=CH2)-CH2-CH2-COOH
HOOC-CH(N=CH2)-CH2-CH2-COOH 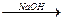 NaOOC-CH(N=CH2)-CH2-CH2-COONa
NaOOC-CH(N=CH2)-CH2-CH2-COONa
f=1/2
Чистота: рН=3,1-3,7. Посторонние АК недопустимы (с реактивом Фелинга не должно быть зеленого и бурого окрашивания при кипячении). Прозрачность, цветность, органические примеси, сульфатная зола, тяжелые металлы, хлор, мышьяк, микробиологическая чистота, потеря в массе при высушивании не более 0,5%
Применение: таблетки при заболеваниях ЦНС.
Хранение: в хорошо упакованной таре, недоступно для света.
Methioninum. a-амино-g-метилтиомаслянная кислота.
HOOC-CH(NH2)-(CH2)2-S-CH3
Описание: белый, кристаллический порошок со сладким вкусом и слабым запахом. Трудно растворим в воде, хорошо растворим в кислоте и щелочи.
Получение: как у глютаминовой кислоты, но только вместо акрилонитрила, бета-метилтиоэтанол HO-CH2CH2-S-CH3
Подлинность:
1. Удельный угол вращения.
2. Нингидриновая проба
3. Реакция на серу (сплавление со щелочью)
2HOOC-CH(NH2)-CH2-CH2-S-CH3 + 5NaOH 30% à NaOOC-CH(NH2)CH2CH3 + Na2S + CH3SNa + NH3
Na2S + CH3SNa + H2SO4 à H2S + CH3SH + Na2SO4
H2S + Pb(CH3COO)2 à Pb2S¯ + 2CH3COOH
Выпадает черный осадок.
Чистота: прозрачность, цветность; хлор и сульфат допустимы. Мышьяк недопустим. Аммиак определяется по второму методу. Цианиды – специфическая недопустимая – по отсутствию эффекта в берлинской лазури. Сульфатная зола, тяжелые металлы, потеря в массе.
Количественное определение:
1. Метод Кьельдаля.
2. Йодометрия в присутствии K2HPO4, KH2PO4
2HOOC-CH(NH2)-CH2-CH2-S-CH3 + I2 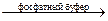 HOOC-CH(NH2)-CH2-CH2-S-CH2-CH2-CH(NH2)-COOH + 2CH3I
HOOC-CH(NH2)-CH2-CH2-S-CH2-CH2-CH(NH2)-COOH + 2CH3I
I2 + 2S2O32- à S4O62- +2I-
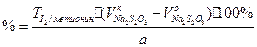 ; f=1/2
; f=1/2
3. Йодхлорметрия.
HOOC-CH(NH2)-CH2-CH2-S-CH3 + IСl à HOOC-CH(NH2)-CH2-CH2-S(=O)-CH3 + HI + HCl
IСl + HI à HCl + I2
I2 + 2Na2S2O3 à 2NaI + Na2S4O6
f=1/2
Конечная точка титрования определяется потенциометрически.
Применение: метионин – незаменимая кислота, фактор роста, широко используется для профилактики и лечения заболеваний, связанных с нарушением обменных процессов, роста и развития.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 1747; Нарушение авторских прав?; Мы поможем в написании вашей работы!