
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Предмет, структура и методы физической химии
|
|
|
|
Оглавление.
Thymolum 2-изопропил, 5-метил фенол.
Применение: антигельминтное, антисептическое.
Описание: бесцветные кристаллы или кристаллический порошок с характерным запахом.
Растворимость: ОМР в воде, легко в спирте, хлороформе, эфире, жирных маслах, ледяной уксусной кислоте, Р в растворе едкого натра.
Подлинность:
1. В холодной воде погружается вниз, при 45°С поднимается на поверхность.
2. Со смесью кислот:
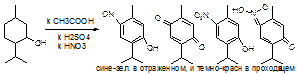
3. С хлороформом в щелочной среде фиолетовое или сиреневое окрашивание.
4. NB! тимол не образует окрашенных комплексов с FeCl3
НЕ ГФ:
1. Реакция с глюкозой в кислой среде – красный.
2. Сплавление с фталиевой кислотой, фталиевым ангидридом à тимолфталин – кислотно-основной. Переход окраски от бесцветной к васильковой. рН=9,4-10,6
КО:
Прямая броматометрия (среда HCl). Индикатор – МО
Общие темы. 1
Государственная фармакопея РФ.. 1
Структура ФС (ГФ XI) 1
Определение прозрачности и степени мутности. 1
Определение окраски жидкостей. 1
Эталонные растворы.. 2
Растворимость. 2
Реакции на общие примеси (с.166, т.1 ГФXI) 2
Cl- 2
SO42- 2
NH4+. 3
Ca2+. 3
Fe3+/Fe2+. 4
Zn2+. 4
Pb2+. 5
As. 5
Галогены и их соединения с щелочными металлами 6
Качественные реакции на катионы щелочных металлов. 6
Na+. 6
K+. 6
Качественные реакции на анионы-галогениды.. 7
Br- 7
I- 7
Количественное определение галогенидов. 7
Метод Мора - NaCl, KCl, NaBr, KBr - ГФ X.. 7
Метод Фаянса – KI, NaI (ГФ X) 8
Метод Фольгарда – Br, I, (Сl) 8
Метод Кальтгоффа-Стенгера – Br- 9
Метод Кальтгоффа – I- в присутствии Cl, Br – йодкрахмальный метод. 9
Окислительное титрование. 10
Меркуриметрия: - прямое осадительное титрование. 10
Безиндикаторная меркуриметрия для I- 10
Аргентометрия с внешним индикатором.. 11
Примеси в препаратах галогенидов. 11
Препараты: 12
Natrii chloridum.. 12
Natrii bromidum.. 12
Natrii iodidum.. 12
Kalii chloridum.. 13
Kalii bromidum.. 13
Kalii iodidum.. 13
Iodum.. 14
Solutio lodi spirituosa 5%.. 15
Соединения кислорода. 15
Препараты: 15
Aqua purificata. 15
Natrii hydrocarbonas. 16
Kalii permanganas. 17
Natrii thiosulfas. 17
Solutio Hydrogenii peroxydi diluta. 18
Другие препараты перекиси водорода. 18
Cоединения бора. 19
Acidum boricum – кислота борная – H3BO3 19
Natrii tetraborax – натрия тетраборат – Na2B4O7•10H2O.. 20
Соединения кальция, магния, бария цинка, висмута. 21
Комплексонометрия. 21
Индикаторы: 22
Производные трифенилметанового ряда. 22
Азокрасители. 22
Прочие. 22
Принцип работы индикатора. 23
Препараты: 23
Magnesii sulfas - магния сульфат – MgSO4•7H2O.. 23
Magnesii oxydum (magnesia usta) – магния окись (магнезия жженая) - MgO.. 24
Magnesii subcarbonas (magnesia alba) – магния карбонат основной (магнезия белая) 25
Barii sulfas pro roentgeno – бария сульфат для рентгеноскопии – BaSO4 25
Calcii chloridum – кальция хлорид – CaCl2•6H2O.. 26
Zinci sulfas – цинка сульфат – ZnSO4•7H2O.. 27
Zinci oxydum – окись цинка – ZnO.. 27
Bismuthi subnitras – висмута нитрат основной. 28
Соединения меди, серебра. 29
Cupri sulfas – сульфат меди – CuSO4•5H2O.. 29
Argenti nitras – нитрат серебра – AgNO3 29
Органические лекарственные вещества 30
Классификация. 30
Отличия анализа органических препаратов. 30
Методы, используемые для определения подлинности, структуры и количественного определения. 30
Связь между структурой и фармакологическим действием.. 31
Препараты галогенпроизводных углеводородов 31
Методы минерализации. 31
Для серосодержащих препаратов. 31
Для азотсодержащих препаратов. 31
Для галогенсодержащих препаратов. 32
Для мышьяксодержащих препаратов. 32
Для фосфорсодержащих препаратов. 32
Способы отщепления ковалентно-связанного галогена с целью перевода его в ионное состояние 32
Определение хлора и брома. 32
Определение йода. 33
Определение фтора. 33
Определение серы.. 34
Препараты: 35
Aethylii chloridum. CH3-CH2-Cl – хлорэтил. 35
Iodoformium. СHI3 – йодоформ.. 36
Phthorothanum seu Halotanum. F3C-CHClBr – Фторотан (1,1,1-трифтор-2-хлор-2-бром-этан) 37
Chloroformium. CHCl3 – хлороформ.. 37
Bromcamphora. 3-Бром-1,7,7-триметил-бицикло [2,2,1] гептанон-2. 38
Bilignostum seu Adipiodon. Бис-(2,4,6-трийод -3-карбокси)анилид адипиновой к-ты 38
Bromisovalum. (CH3)2CH-CHBr-CO-NH-CO-NH2 39
Triombrastum 60% et 76% pro injectonibus. 40
Препараты альдегидов и их производных. 40
Химические свойства. 40
Методы к.о. 43
Препараты: 43
Solutio Formaldehydi (Formalinum). Формальдегид – водный раствор 37%.. 43
Chlorali hydras – 2,2,2трихлорэтандиол 1,1. Cl3C-CH(OH)2 44
Glucosum.. 45
Hexamethylentetraminum (CH2)6N4 – 1,3,5,7 тетраазотрицикло[3,3,1,13,7]-декан. 46
Camphora. 48
Citralum.. 49
Препараты алифатических спиртов. 49
Spiritus aethylicus. Спирт этиловый: 95%, 90%, 70% и 40%.. 49
Glycerinum. Глицерин. HOCH2-CH(OH)-CH2OH. 50
Препараты простых эфиров. 51
Титрование в неводных средах как метод количественного определения: 51
Препараты: 53
Aether medicinalis. Эфир медицинский. C2H5-O-C2H5 53
Aether medicinalis pro narcosi 53
Dimedrolum. Димедрол. N,N – диметил – 2 – (дифенилметокси)-этиламина гидрохлорид 54
Препараты сложных эфиров азотной кислоты 55
Препараты: 55
Nitroglycerinum. Нитриглицерин. 55
Препараты карбоновых кислот и их солей 56
Препараты: 56
Kalii acetas. Калия ацетат. CH3COOK.. 56
Calcii lactas. Кальция пропионат-2-ол пентагидрат. (CH3-CHOH-COO)2Ca•5H2O.. 57
Calcii gluconas. Кальция глюконат. 58
Natrii citras pro injectionibus. Натрия цитрат для инъекций. 58
Natrii oxybutyras. Натрия оксибутират. HO-CH2-CH2-CH2-COONa. 60
Lithii oxybutyras. HO-CH2-CH2-CH2-COOLi 60
Препараты алифатических аминокислот. 60
Химические свойства: 60
Общие требования к чистоте: 61
Оптическая изомерия: 61
Методы количественного определения АК. 62
Препараты: 63
Acidum glutaminicum - a-аминоглутаровая кислота. HOOC-CH2-CH2-CH(HN2)-COOH 63
Methioninum. a-амино-g-метилтиомаслянная кислота. HOOC-CH(NH2)-(CH2)2-S-CH3 64
Asparkam seu панангин. 65
Aminalonum.. 65
Phenibutam.. 65
Леводопа. L-DOPA, L-ДОФА.. 65
Метилдопа seu Допегит. 65
Phenibutum Ph-CH(CH2NH2)-CH2COOH • HCl 66
Cysteinym HS-CH2-CH(NH2)-COOH.. 66
Glycinum NH2-CH2-COOH.. 66
Taufonum NH2-CH2CH2-SO3H.. 66
Фенолы. 66
Phenolum purum seu Acudum carbolicum crystallisatum. Фенол чистый. 67
Phenolum purum liquefactum seu Acidum carbolicum liauefactum.. 67
Resorcinum seu Resorcinolum. м-дигидрокси бензол. 69
Thymolum 2-изопропил, 5-метил фенол. 70
Фармацевтическая
химия
Курс лекций
Часть первая
Издание второе, исправленное и дополненное.
- Исправлены ошибки
- Добавлены «Аминокислоты» и «Фенолы»
Created by Aeon
http://spcpa.narod.ru
spcpa@narod.ru
[1] Смотри тему "Неводное титрование"
[2]Смотри тему "Неводное титрование"
1.1. Физическая химия изучает общие вопросы химического строения веще-ства, общие количественные закономерности химического равновесия и химических процессов, а также физических явлений, которые их сопро-вождают.
1.1.1. Термин физическая химия введен М. В. Ломоносовым. «Физическая химия - наука, которая должна на основе положений и опытов физических объяснить причину того, что происходит через химические операции в сложных телах.» Т.е. ФХ изучает связь между физическими и хими-ческими явлениями, физические процессы, которыми сопровождаются химические реакции.
1.1.2. Физическая химия – это теоретическая химия, которая рассматривает общие законы, определяющие химические процессы, а именно направление химических реакций, условия равновесия, протекание во времени, влияние различных факторов на химические реакции. ФХ дает математическое описание химических процессов, что позволяет перевести изучение химических явлений на компьютерную основу.
1.1.3. Физическая химия – основа химической технологии, она позволяет оптимизировать протекание химических реакций, сделать их более экологически безопасными.
1.1.4. Физическая химия изучает строение веществ, связь между структурой и физико-химическими свойствами веществ, т.е. дает основу материаловедения, науки, которая определяет технический прогресс.
1.1.5. Физическая химия - основа аналитической химии, т.к. она имеет дело с методами изучения структуры вещества, а, следовательно, его идентификации физическими методами.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 316; Нарушение авторских прав?; Мы поможем в написании вашей работы!