
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Экспериментальное определение теплот реакций
|
|
|
|
4.4.2.1. Калориметрия – метод непосредственного экспериментального измерения теплот химических реакций в приборе, называемом калори-метром. Различают калориметры изотермические, работающие при постоянной температуре, и с переменной температурой, которая и служит измеряемой величиной в этом случае. В последнем случае реакцию проводят в адиабатических (по возможности) условиях. В этом случае изменение DU или DH происходят за счет химической реакции и за счет изменения температуры
0 = DrH + DtH = DrH Dx + CpDT
DrH = - CpDT/x = - CpDTνk/ Dnk (3.2)
4.4.2.2. Теплота сгорания.
Для экспериментального определения теплоты реакции необходимо, чтобы реакция протекала однозначно, т.е. не сопровождалась побочными процессами и степень превращения приближалась к единице. Далеко не все реакции отвечают таким критериям. Наиболее доступны для экспериментального исследования теплоты сгорания, которые проводят в калориметрической бомбе в атмосфере кислорода без катализатора. При этом получаются устойчивые оксленные состояния элементов СО2, Н2О, SO2, N2 или NО2, обязательно требуется анализ продуктов.
С2Н5ОН +7/2 О2 = 2 СО2 + 3 Н2О; DrН = DсН
4.4.2.3. 2-ое следствие из закона Гесса – определение теплоты реакции по теплотам сгорания

 С6Н6 + 3Н2 = С6Н12 DсН1 = -3267,58 кДж/моль
С6Н6 + 3Н2 = С6Н12 DсН1 = -3267,58 кДж/моль
 DсН1 DсН 2 DсН3
DсН1 DсН 2 DсН3
| 6 СО2 + 6 Н2О |
DсН2 = DfН(Н2О) = -285,83кДж/моль
DсН3 = -3919,91 кДж/моль
DrН˚ = 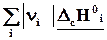 – –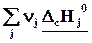 = – = – 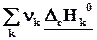
|
(3.3)
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 321; Нарушение авторских прав?; Мы поможем в написании вашей работы!