
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
II Закон Термодинамики
|
|
|
|
Формулировки закона:
1. Тепло может переходить только от более нагретых тел к менее нагретым.
2. Тело, имеющее наименьшую температуру, не может служить источником тепла.
3. Невозможно создать вечный двигатель второго рода; то есть такую машину, которая, действуя периодически, превращала бы все тепло, подведенное к ней в работу.
Возможно перевести все тепло в работу, если машина действует однократно!
Исходя из этого, был вычислен максимальный кпд тепловых машин:
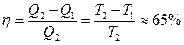
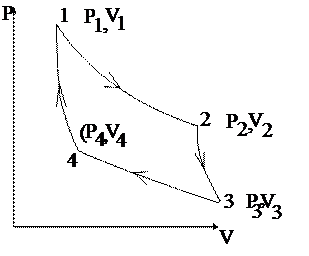
|
Все тепло, которое нельзя перевести в полезную работу рассеивается
Или диссипирует в окружающую среду. Критерием диссипативности служит приведенная теплота: 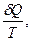 которая получила название энтропии.
которая получила название энтропии.
Для обратимого процесса приведенная элементарная теплота будет равна изменению энтропии: 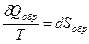
Так как Qобр.>Qнеобр. , Для необратимого процесса 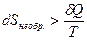
Энтропия (приведенная теплота) относится к функциям состояния, которые не зависят от пути процесса, а определяются начальными и конечными состояниями системы. В общем случае II Закон Термодинамики в математической записи выглядит так:
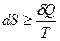
Для конечных значений S=Q/T, так как энтропия является мерой диссипативной части энергии, она должна характеризовать беспорядок в системе. Чем больше энтропия, тем меньше упорядоченность системы (порядок).
К этому же выводу пришел Больцман, который раскрыл физический смысл энтропии с помощью статистической термодинамики, которая описывает макроскопические системы, суммируя её микроскопические состояния:
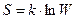 , где W – термодинамическая вероятность системы, то есть такое число микросостояний, изменение которых не приводит к изменению макроскопических параметров системы.
, где W – термодинамическая вероятность системы, то есть такое число микросостояний, изменение которых не приводит к изменению макроскопических параметров системы.
|
|
|
|
|
Дата добавления: 2013-12-12; Просмотров: 662; Нарушение авторских прав?; Мы поможем в написании вашей работы!