
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Севастьянова Галина Константиновна Карнаухова Тамара Михайловна
|
|
|
|
NO
Очень разб.
|
 Активный
Активный

 N2
N2
|
 Средней
Средней
HNO3 + Me активности N
активности N
|
 Малоактивный
Малоактивный
разб.
+4
 Активный
Активный
NO
+2


Средней
|
 HNO3 + Me
HNO3 + Me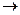 активности NO2 + Me(NO3)n + H2O
активности NO2 + Me(NO3)n + H2O
конц. Малоактивный
 NO2
NO2
Примеры:
1. Ba + HNO3 ® NH4NO3 + Ba(NO3)2 + H2O
очень разб.
1  NO
NO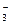 + 10H+ + 8
+ 10H+ + 8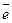 ® NH4+ + 3H2O
® NH4+ + 3H2O
4  Ba – 2
Ba – 2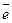 ® Ba2+
® Ba2+
NO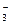 + 10H+ + 4Ba = NH4+ + 3H2O + 4Ba2+
+ 10H+ + 4Ba = NH4+ + 3H2O + 4Ba2+
4Ba + 10HNO3 = NH4NO3 + 4Ba(NO3)2 + 3H2O
2. Zn + HNO3 ® Zn(NO3)2 + N2O + H2O
разб.
 4 Zn – 2
4 Zn – 2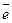 ® Zn2+
® Zn2+
 1 2NO
1 2NO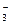 + 10H+ + 8
+ 10H+ + 8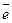 ® N2O + 5H2O
® N2O + 5H2O
4Zn + 2NO3- + 10H+ = 4Zn2+ + N2O + 5H2O
4Zn + 10HNO3 = 4Zn(NO3)2 + N2O + 5H2O
Особенности взаимодействия металлов с концентрированной серной кислотой. Концентрированная серная кислота реагирует со всеми металлами, кроме Ag, Au, Pt. В концентрированной серной кислоте более сильным окислителем, чем катионы водорода, являются сульфат-ионы SO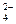 , поэтому при её взаимодействии с металлами Н2 не выделяется, а идёт восстановление серы S+6 в анионе SO
, поэтому при её взаимодействии с металлами Н2 не выделяется, а идёт восстановление серы S+6 в анионе SO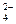 , при этом продукт восстановления зависит от активности металла:
, при этом продукт восстановления зависит от активности металла:
-2
 Активный
Активный

 Средней H2S
Средней H2S
активности
 H2SO4 + Me
H2SO4 + Me S + MeSO4 + H2O
S + MeSO4 + H2O
|
 SO2
SO2
Например,
Zn + H2SO4 ® S + ZnSO4 + H2O
 конц.
конц.
3 Zn – 2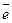 ® Zn2+
® Zn2+
 1 SO
1 SO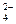 + 8H+ + 6
+ 8H+ + 6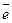 ® S + 4H2O
® S + 4H2O
3Zn + SO42- + 8H+ = 3Zn2+ + S + 4H2O
3Zn + 4H2SO4 = S + 3ZnSO4 + 4H2O
Примечание: в концентрированных растворах НNO3, Н2SO4 такие металлы как Fe, Al, Cr пассивируются образующимися оксидами.
Например,
Fe + HNO3 ® Fe2O3 + NO2 + H2O
конц.
Восстановительные свойства металлов по отношению к катионам металлов. В общем ионно-молекулярном виде такой тип взаимодействия можно представить следующим образом:
Ме1 + Ме2n+ ® Ме1m+ + Ме2
в-ль ок-ль пр. пр.
ок-ия в-ния
Ме1 – m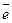 ® Ме1m+
® Ме1m+
Ме2n+ + n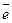 ® Ме2
® Ме2
Е0 = 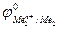 –
– 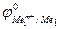
Так как самопроизвольному процессу отвечает Е0 > 0, то 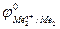 >
> 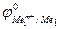 . Это означает, что более активный металл (с меньшим электродным потенциалом, Ме1) вытесняет менее активный металл (с большим электродным потенциалом, Ме2) из раствора его соли.
. Это означает, что более активный металл (с меньшим электродным потенциалом, Ме1) вытесняет менее активный металл (с большим электродным потенциалом, Ме2) из раствора его соли.
|
|
|
Например, реакция омеднения цинка в растворе сульфата меди (II) возможна, т.к.  >
> 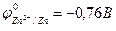 :
:
Zn + CuSO4 = ZnSO4 + Cu.
ЛИТЕРАТУРА
1. Коровин Н.В. Общая химия. – М.: Высшая школа, 2002. – 558 с.
2. Ахметов Н.С. Общая и неорганическая химия. – М.: Высшая школа, 1998. – 743 с.
3. Хомченко Г.П., Цитович И.К. Неорганическая химия. – М.: Высшая школа, 1987. – 464 с.
4. Глинка Н.Л. Общая химия. – М.: Интеграл-Пресс, 2002. – 702 с.
5. Курс лекций по общей химии / Р.Г. Чувиляев, Л.А. Байдаков, Б.Д. Курников, Л.Н. Блинов. – Л.: Изд-во Ленинградского ун-та, 1989. – 230 с.
6. Кукушкин Ю.Н., Маслов Е.И. Строение атома и химическая связь – Л.: Изд-во Ленинградского университета, 1973. – 79 с.
Приложение 1
Электронные конфигурации элементов
| Период | Порядковый номер | Элемент | Электронная конфигурация |
| H | 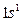
| ||
| He | 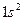
| ||
| Li | 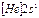
| ||
| Be | 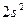
| ||
| B | 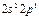
| ||
| C | 
| ||
| N | 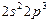
| ||
| O | 
| ||
| F | 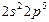
| ||
| Ne | 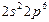
| ||
| Na | 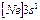
| ||
| Mg | 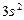
| ||
| Al | 
| ||
| Si | 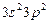
| ||
| P | 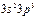
| ||
| S | 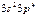
| ||
| Cl | 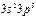
| ||
| Ar | 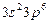
| ||
| K | 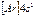
| ||
| Ca | 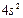
| ||
| Sс | 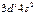
| ||
| Ti | 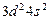
| ||
| V | 
| ||
| Cr | 
| ||
| Mn | 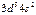
| ||
| Fe | 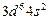
| ||
| Co | 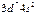
| ||
| Ni | 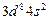
| ||
| Cu | 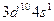
| ||
| Zn | 
| ||
| Ga | 
| ||
| Ge | 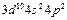
| ||
| As | 
| ||
| Se | 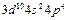
| ||
| Br | 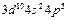
| ||
| Kr | 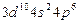
|
Продолжение
| Период | Порядковый номер | Элемент | Электронная конфигурация |
| Rb | 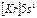
| ||
| Sr | 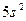
| ||
| Y | 
| ||
| Zr | 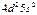
| ||
| Nb | 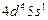
| ||
| Mo | 
| ||
| Tc | 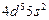
| ||
| Ru | 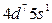
| ||
| Rh | 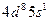
| ||
| Pd | 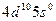
| ||
| Ag | 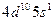
| ||
| Cd | 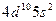
| ||
| In | 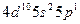
| ||
| Sn | 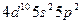
| ||
| Sb | 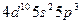
| ||
| Te | 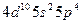
| ||
| I | 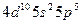
| ||
| Xe | 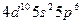
| ||
| Cs | 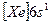
| ||
| Ba | 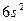
| ||
| La | 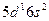
| ||
| Ce | 
| ||
| Pr | 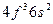
| ||
| Nd | 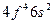
| ||
| Pm | 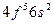
| ||
| Sm | 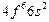
| ||
| Eu | 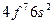
| ||
| Gd | 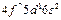
| ||
| Tb | 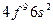
| ||
| Dy | 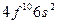
| ||
| Ho | 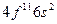
| ||
| Er | 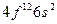
| ||
| Tm | 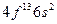
| ||
| Yb | 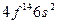
| ||
| Lu | 
| ||
| Hf | 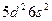
| ||
| Ta | 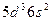
|
Продолжение
| Период | Порядковый номер | Элемент | Электронная конфигурация |
| W | 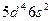
| ||
| Re | 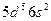
| ||
| Os | 
| ||
| Ir | 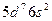
| ||
| Pt | 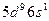
| ||
| Au | 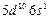
| ||
| Hg | 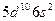
| ||
| Tl | 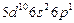
| ||
| Pb | 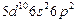
| ||
| Bi | 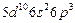
| ||
| Po | 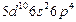
| ||
| At | 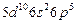
| ||
| Rn | 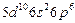
| ||
| Fr | 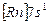
| ||
| Ra | 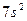
| ||
| Ac | 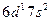
| ||
| Th | 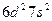
| ||
| Pa | 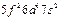
| ||
| U | 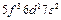
| ||
| Np | 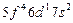
| ||
| Pu | 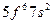
| ||
| Am | 
| ||
| Cm | 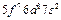
| ||
| Bk | 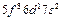
| ||
| Cf | 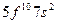
| ||
| Es | 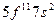
| ||
| Fm | 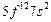
| ||
| Md | 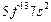
| ||
| (No) | 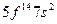
| ||
| (Lr) | 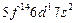
| ||
| (Ku) | 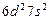
| ||
| (Ns) | 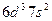
| ||
| Rf | 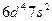
| ||
| Bh | 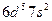
| ||
| Hn | 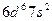
| ||
| Mt | 
|
Содержание
1. ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ.. 3
|
|
|
1.1. Определение химии. Предмет химии. Её связь с другими науками. Значение химии в изучении природы и развитии техники. 3
1.2. Основные понятия химии. 4
1.3. Основные законы химии. 7
2. СОВРЕМЕННАЯ ТЕОРИЯ СТРОЕНИЯ АТОМА. ПЕРИОДИЧЕСКИЙ ЗАКОН И СИСТЕМА ЭЛЕМЕНТОВ Д.И. МЕНДЕЛЕВА.. 10
2.1. Общие положения. 10
2.2. Развитие представлений о строении атома. 11
2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики 13
2.4. Модель состояния электрона в атоме. 14
2.5. Квантовые числа. 15
2.6. Электронные конфигурации (формулы) элементов. 19
2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах 20
2.8. Электронные семейства элементов. 22
2.9. Понятие об электронных аналогах. 22
2.10. Периодический закон и периодическая система элементов Д.И. Менделеева. 23
2.11. Структура периодической системы химических элементов Д. И. Менделеева. 24
2.12. Периодическая система Д.И. Менделеева и электронная структура атомов. 26
2.13. Периодичность свойств элементов. 29
3.ХИМИЧЕСКАЯ СВЯЗЬ И СТРОЕНИЕ МОЛЕКУЛ.. 36
3.1. Основные понятия и определения. 36
3.2. Теория метода валентных связей. 38
3.3. Ковалентная связь. 39
3.4. Насыщаемость ковалентной связи. 41
3.5. Направленность ковалентной связи …………………………………………………………45
3.6. Полярность и поляризуемость химической связи. 54
3.7. Полярность молекул (типы ковалентных молекул) 57
3.8. Ионная связь. 59
3.9. Металлическая связь. 61
4. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.. 64
4.1. Классификация веществ. 64
4.2. Оксиды.. 64
4.3. Гидроксиды.. 66
4.4. Кислоты.. 67
4.5. Основания. 69
4.6. Соли. 70
5. ЭНЕРГЕТИКА И НАПРАВЛЕННОСТЬ ХИМИЧЕСКИХ ПРОЦЕССОВ (ЭЛЕМЕНТЫ ХИМИЧЕСКОЙ ТЕРМОДИНАМИКИ) 75
5.1 Основные понятия и определения. 75
5.2. Первый закон термодинамики. 77
5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса. 78
|
|
|
5.5. Свободная энергия Гиббса. 81
5.6. Свободная энергия Гельмгольца. 83
6. ХИМИЧЕСКАЯ КИНЕТИКА.. 84
6.1. Основные понятия химической кинетики. 84
6.2. Влияние природы реагирующих веществ. 85
6.3. Закон действующих масс. 85
6.4. Зависимость скорости химической реакции от температуры.. 87
6.5. Влияние катализатора. 90
7. ХИМИЧЕСКОЕ РАВНОВЕСИЕ.. 92
7.1. Общие представления о химическом равновесии. Константа химического равновесия 92
7.2. Смещение химического равновесия. Принцип Ле Шателье. 94
7.3. Фазовые равновесия. Правило фаз Гиббса. 96
8. ДИСПЕРСНЫЕ СИСТЕМЫ. РАСТВОРЫ... 99
8.1. Дисперсные системы и их классификация. 99
8.2. Общая характеристика растворов. 100
8.3. Способы выражения концентрации растворов. 101
8.4. Растворимость. 102
8.5. Природа жидких растворов. 104
8.6. Типы и свойства растворов. 105
8.7. Свойства растворов неэлектролитов. 107
8.8. Растворы электролитов. 112
8.9. Равновесия и обменные реакции в растворах электролитов. 119
8.10. Гидролиз солей. 133
8.11. Комплексные соединения. 143
9. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ.. 152
9.1. Общие понятия и определения. 152
9.2. Восстановители и окислители. 158
9.3. Влияние среды на окислительно-восстановительные реакции. 161
9.4. Типы окислительно-восстановительных реакций. 164
9.5. Окислительно – восстановительные (электродные) потенциалы.. 165
9.6. Направление протекания окислительно-восстановительных реакций. 169
10. Электрохимические процессы... 171
10.1. Гальванические элементы (химические источники электрического тока) 171
10.2. Электролиз. 175
10.3. Коррозия металлов. 184
10.4. Защита металлов от коррозии. 191
11. СВОЙСТВА МЕТАЛЛОВ.. 196
11.1. Физические свойства металлов. 196
11.2. Химические свойства металлов. 198
ЛИТЕРАТУРА.. 203
Приложение 1. 203
Электронные конфигурации элементов. 203
Содержание. 203
Учебное издание
ОБЩАЯ ХИМИЯ
Курс лекций
Редактор В.К. Бородина
Подписано к печати Бум. ГОЗНАК
Заказ № Уч.-изд. л.
Формат 60x84 1/16 Усл-печ. л.
Отпечатано на RISO GR 3750 Тираж 200 жз.
 Издательство «Нефтегазовый университет»
Издательство «Нефтегазовый университет»
Государственного образовательного учреждения высшего профессионального образования «Тюменский государственный нефтегазовый университет»
|
|
|
625000, Тюмень, ул. Володарского, 38
Отдел оперативной полиграфии издательства «Нефтегазовый университет» 625000, Тюмень, ул. Володарского, 38
[1] Если закон Авогадро применим только для газов, то число Авогадро имеет универсальный характер для любого агрегатного состояния вещества.
[2] Все рассмотренные газовые законы строго соблюдаются при очень малых давлениях, при обычных невысоких давлениях они соблюдаются приближенно, а при высоких давлениях наблюдаются большие отклонения от этих законов.
1 Представление об электронных семействах элементов и их валентных электронах см. в разделе 2.8.
1 Валентные электроны атома – это электроны, способные участвовать в образовании химических связей в молекулах, ионах и т.д.
1 Приведены эффективные радиусы, экспериментально найденные для металлического состояния простых веществ.
2 В этом случае f-сжатие называется лантаноидным.
1 В скобках указано число электронов на внешнем энергетическом уровне иона.
[3] Реакция протекает в расплаве веществ.
1 Реакция протекает в расплаве веществ.
2 Реакция протекает в расплаве веществ.
3 Реакция протекает в растворе.
1 Массовая и молярные доли могут быть выражены в промилле, %О (умножением на 1000), в частях на миллион, ppm (умножением на 106) и в частях на миллиард, ppb (умножением на 109).
1 От латинских слов Reductio (восстановление) и Oxidato (окисление).
1 Электролитический ключ – U-образная трубка, заполненная каким-либо электролитом, чаще – насыщенным раствором хлорида калия.
1 Механизм возникновения электродных потенциалов изложен в разделе 9.5.
1 Деполяризация – связывание электронов.
2 Деаэрацию можно осуществить кипячением раствора или его продуванием инертным газом.
|
|
|
|
|
Дата добавления: 2013-12-11; Просмотров: 330; Нарушение авторских прав?; Мы поможем в написании вашей работы!