
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Элементы квантовой механики
|
|
|
|
Лекция № 4
Гипотеза Де-Бройля. Волновые свойства веществ.
Недостатки теории Бора сделали необходимым критический пересмотр основ квантовой теории и представлений о природе элементарных частиц. Возник вопрос о том, правомочно ли представление электрона в виде малой механической частицы, характеризуемой определенными координатами и определенной скоростью.
В результате углубления познания о природе света выяснилось, что в оптических явлениях обнаруживается дуализм корпускулярных и волновых свойств.
В 1924 г. Луи Де-Бройль выдвинул смелую гипотезу, что дуализм не является особенностью одних только оптических явлений. Он имеет универсальное значение и может быть распространен и на частицы вещества, в частности - на электроны.
Гипотеза Де-Бройля заключалась в том, что электрон, корпускулярные свойства которого были изучены давно, имеет еще и волновые свойства, т.е. ведет себя в определенных условиях, как волна.
Де-Бройль воспользовался соотношением для импульса фотона 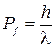 и перенес его на электрон. Таким образом, любой частице, обладающей импульсом
и перенес его на электрон. Таким образом, любой частице, обладающей импульсом 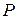 , соответствует волна, длина которой определяется по формуле Де-Бройля, т.е.
, соответствует волна, длина которой определяется по формуле Де-Бройля, т.е.
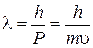 ,
,
где 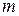 - масса частицы;
- масса частицы;
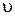 - ее скорость.
- ее скорость.
Для электрона длина волны Де-Бройля, после прохождения им ускоряющего напряжения 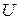 , определяется из выражения
, определяется из выражения 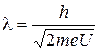 .
.
Гипотеза Де-Бройля была блестяще подтверждена экспериментально в 1927г. Девиссоном и Джермером. Еще до этого Эйнштейн указал на то, что, если идеи Де-Бройля справедливы, то для электронов должно наблюдаться явление дифракции.
Девиссон и Джермер, изучая рассеяние электронов на монокристаллах никеля, обнаружили это явление.
Схема опыта заключалась в следующем: в электронной пушке 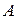 создавался поток электронов, откуда он направлялся на заземленный монокристалл никеля. Монокристалл можно было вращать. Рассеянные им электроны регистрировались подвижным приемником
создавался поток электронов, откуда он направлялся на заземленный монокристалл никеля. Монокристалл можно было вращать. Рассеянные им электроны регистрировались подвижным приемником 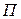 . Опыты показали, что интенсивность рассеянных электронов различна по разным направлениям: имеются максимумы и минимумы числа электронов, рассеянных под разными углами, т.е. наблюдается дифракция электронов.
. Опыты показали, что интенсивность рассеянных электронов различна по разным направлениям: имеются максимумы и минимумы числа электронов, рассеянных под разными углами, т.е. наблюдается дифракция электронов.
 Применяя методы, используемые для наблюдения дифракции рентгеновских лучей, Девиссон и Джермер смогли экспериментально определить длину волны рассеянных электронов. Эти значения оказались в полном соответствии с вычислениями длины волны по формуле Де-Бройля.
Применяя методы, используемые для наблюдения дифракции рентгеновских лучей, Девиссон и Джермер смогли экспериментально определить длину волны рассеянных электронов. Эти значения оказались в полном соответствии с вычислениями длины волны по формуле Де-Бройля.
Формула Де-Бройля впоследствии проверять неоднократно и давала полное соответствие теории с опытом. Так в 1928 г. Томсон и, независимо от него, Тартаковский получили дифракционную картину при прохождении электронного пучка через металлическую фольгу. Опыт осуществлялся следующим образом:
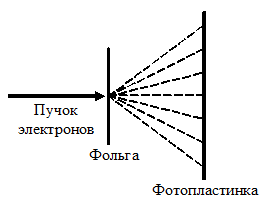 Пучок электронов проходил через тонкую металлическую фольгу и попадал на фотопластинку, создавая дифракционную картину, т.е. электрон оказывал на фотопластинку такое же действие, как и фотон. Тем самым было установлено, что электроны, как и фотоны, обладают волновыми свойствами, наряду со свойствами корпускулярными. Однако, не присущи ли волновые свойства только потоку большой совокупности электронов? Ответ на этот на этот вопрос был получен в опыте В.Фабриканта, Л.Бибермана и Н.Сушкина. Они осуществили опыт по дифракции электронов с такой малой силой тока в приборе, что каждый электрон проходил через прибор независимо от других. Среднее время между прохождениями двух электронов через прибор примерно в 30000 раз превышало время прохождения электрона через прибор. При длительной экспозиции была получена такая же дифракционная картина, как и при короткой экспозиции электронного потока большой плотности. Этот опыт показал, что волновые свойства присущи каждому электрону в отдельности.
Пучок электронов проходил через тонкую металлическую фольгу и попадал на фотопластинку, создавая дифракционную картину, т.е. электрон оказывал на фотопластинку такое же действие, как и фотон. Тем самым было установлено, что электроны, как и фотоны, обладают волновыми свойствами, наряду со свойствами корпускулярными. Однако, не присущи ли волновые свойства только потоку большой совокупности электронов? Ответ на этот на этот вопрос был получен в опыте В.Фабриканта, Л.Бибермана и Н.Сушкина. Они осуществили опыт по дифракции электронов с такой малой силой тока в приборе, что каждый электрон проходил через прибор независимо от других. Среднее время между прохождениями двух электронов через прибор примерно в 30000 раз превышало время прохождения электрона через прибор. При длительной экспозиции была получена такая же дифракционная картина, как и при короткой экспозиции электронного потока большой плотности. Этот опыт показал, что волновые свойства присущи каждому электрону в отдельности.
Волновыми свойствами обладают не только электроны. Любые частицы вещества, имеющие некоторую массу m и скорость 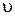 , характеризуются определенной длиной волны Де-Бройля.
, характеризуются определенной длиной волны Де-Бройля.
Так было обнаружено явление дифракции нейтронов, т.е. частиц, входящих в состав атомного ядра. Это было сделано следующим образом. Узкий пучок нейтронов претерпевает дифракцию на кристалле и попадает в приемник. Кристалл и приемник нейтронов поворачиваются таким образом, чтобы сохранялось равенство углов падения и отражения нейтронов 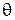 . В этом случае справедливо соотношение
. В этом случае справедливо соотношение
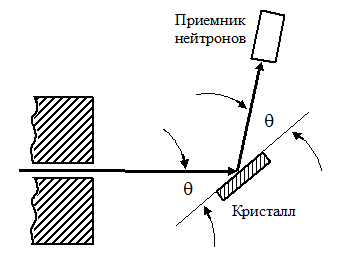
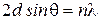 - условие Вульфа-Брэгга.
- условие Вульфа-Брэгга.
где 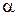 - период решетки кристал-ла.
- период решетки кристал-ла.
Отсюда можно легко найти 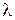 , которое очень хорошо совпадает с теоретическим значением, вычис-ленным по формуле Де-Бройля.
, которое очень хорошо совпадает с теоретическим значением, вычис-ленным по формуле Де-Бройля.
В 1929 г. О.Штерн и его сотрудники обнаружили волновые свойства в пучке нейтральных атомов и молекул.
Естественен вопрос, обнаруживаются ли волновые свойства у макроскопических тел, с которыми мы повседневно встречаемся. Для тела массой в 1г, обладающего скоростью 1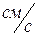 , длина волны Де-Бройля равна
, длина волны Де-Бройля равна 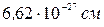 . Такая длина волны лежит очень далеко за пределами возможности ее обнаружения в любом дифракционном опыте, т.к. периодических структур с периодом порядка
. Такая длина волны лежит очень далеко за пределами возможности ее обнаружения в любом дифракционном опыте, т.к. периодических структур с периодом порядка 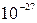 не существует.
не существует.
С увеличением массы тела обнаружение волновых свойств у макроскопических тел становится менее возможным.
Открытие волновых свойств движущихся частиц вещества явилось важнейшим достижением современной физики. Вместе с твердо установленным квантовым характером законов, описывающих внутриатомные процессы, обнаружение волновых свойств частиц вещества послужило фундаментом для создания квантовой механики, объектами изучения которой явились атомы, молекулы, атомные ядра и элементарные частицы.
Границы применимости классической механики. Принцип неопределенности.
Опыты по дифракции подтвердили, что электроны не являются материальной точкой, а представляют собой сложный материальный объект, обладающий волновыми свойствами.
В отличии от фотона электрон обладает электрическим зарядом. От положения и распределения этого заряда в пространстве, или как говорят, от его локализации зависит взаимодействие электрона с другими частицами.
Уточним, чем характеризуется пространственная локализация точечного объекта. Пусть материальная точка с массой 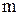 движется вдоль оси
движется вдоль оси 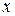 . В некоторый момент времени она занимает положение, характеризуемое координатой
. В некоторый момент времени она занимает положение, характеризуемое координатой 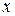 и скоростью
и скоростью 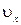 . Через некоторое время точка займет положение с координатой
. Через некоторое время точка займет положение с координатой 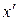 и будет иметь скорость
и будет иметь скорость 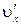 . Совокупность последовательных положений движущейся точки образует траекторию ее движения.
. Совокупность последовательных положений движущейся точки образует траекторию ее движения.
Если известны силы, действующие на материальную точку, то по ІІ -му закону Ньютона можно раcсчитать все последовательные значения координаты и скорости движущейся частицы.
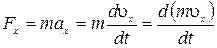 .
.
Обозначив 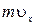 через
через 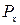 , где
, где 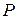 - импульс силы, получим
- импульс силы, получим
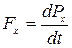 . (1)
. (1)
Так как 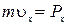 , то, разделив это равенство на
, то, разделив это равенство на 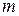 , получим
, получим
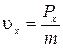 или
или 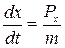 . (2)
. (2)
Уравнения (1) и (2) представляют собой математическую формулировку принципа причинности в классической механике. Он гласит: если известны силы, действующие на материальную точку, то можно определить приращения ее координаты и импульса в последовательные промежутки времени и тем самым расчитать все ее движение.
Иначе обстоит дело с локализацией волновых объектов.
Для упрощения расчетов рассмотрим одномерное распространение волны вдоль оси 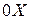 . Любая волна, независимо от ее природы, характеризуется некоторой волновой функцией
. Любая волна, независимо от ее природы, характеризуется некоторой волновой функцией 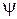 . Она может выражать, например плотность и давление в акустической волне, векторы
. Она может выражать, например плотность и давление в акустической волне, векторы 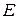 и
и 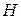 в электромагнитной волне и т.д. Значения ее различны для точек с разными координатами Х и изменяются с течением времени
в электромагнитной волне и т.д. Значения ее различны для точек с разными координатами Х и изменяются с течением времени 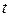 , т.е.
, т.е. 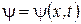 .
.
Локализация этой функции в пространстве может быть различной. Простейшая электромагнитная монохроматическая волна, распространяющаяся вдоль оси Х, изображена на рисунке.
 Пунктиром показана эта же волна через время
Пунктиром показана эта же волна через время 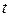 . Такая монохроматическая волна заполняет все беско-нечное пространство. Интер-вал координат
. Такая монохроматическая волна заполняет все беско-нечное пространство. Интер-вал координат 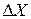 , в котором заключен волновой объект, равен бесконечности.
, в котором заключен волновой объект, равен бесконечности.
Импульс частицы, связанной с волной, как мы знаем равен 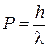 .
.
Так как волна монохроматическая 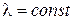 и
и 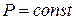 . Иными словами, интервал
. Иными словами, интервал 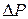 , в котором заключены все возможные значения импульса, равен нулю. Таким образом, рассмотренная волна характеризуется соотношениями
, в котором заключены все возможные значения импульса, равен нулю. Таким образом, рассмотренная волна характеризуется соотношениями 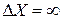 и
и 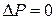 .
.
Рассмотрим другой пример: волну, локализованную в некотором интервале 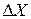 . Такая волна получается в результате сложения монохроматических волн с различными длинами волн.
. Такая волна получается в результате сложения монохроматических волн с различными длинами волн.
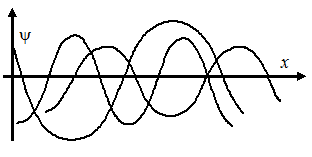 Набор таких волн различных амплитуд с длинами волн от
Набор таких волн различных амплитуд с длинами волн от 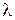 до
до 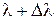 показан на рисунке.
показан на рисунке.
Ниже показан результат их сложения: так называемый волновой пакет. При такой пространственной локализации теряется смысл понятия длины волны и, следовательно, импульса.
 Чем в более узком интервале
Чем в более узком интервале 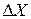 локализована волна, тем более широкий интервал длин волн
локализована волна, тем более широкий интервал длин волн 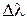 входит в пакет. Следовательно, увеличение определенности в локализации волны, т.е. уменьшение
входит в пакет. Следовательно, увеличение определенности в локализации волны, т.е. уменьшение 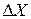 , связано с возрастанием неопределенности импульса
, связано с возрастанием неопределенности импульса 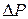 .
.
В пределе при 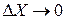 имеем
имеем 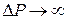 .
.
Исходя из вышеизложенного, можно сделать следующий вывод: электрон не может иметь одно-временно определенную координату 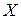 и импульс
и импульс 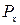 .
.
Соотношение между величинами 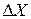 и
и 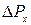 (и аналогичные им соотношения для других осей) проанализировал впервые В.Гейзенберг.
(и аналогичные им соотношения для других осей) проанализировал впервые В.Гейзенберг.
Он установил, что неопределенность в нахождении 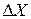 связана с неопределенностью в нахождении
связана с неопределенностью в нахождении 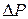 соотношением:
соотношением:
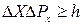 .
.
Это положение носит название принципа неопределенностей Гейзенберга. Если частицы движутся вдоль осей 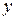 и
и 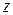 , то аналогичные соотношения будут иметь вид:
, то аналогичные соотношения будут иметь вид:
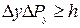
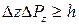 .
.
Чтобы пояснить принцип неопределенностей рассмотрим следующий пример. Для определения положения свободно летящей микрочастицы поставим на ее пути щель, шириной 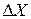 , расположенную перпендикулярно направлению движения частицы.
, расположенную перпендикулярно направлению движения частицы.
До прохождения частицы через щель составляющая импульса 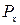 была равна нулю, т.к. щель перпендикулярна импульсу
была равна нулю, т.к. щель перпендикулярна импульсу 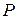 . Следовательно,
. Следовательно, 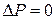 . Координата частицы
. Координата частицы 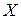 может быть любой или, как говорят в квантовой физике, неопределенной.
может быть любой или, как говорят в квантовой физике, неопределенной.
В момент прохождения частицы через щель и после прохождения положение меняется. Вследствие дифракции имеется вероятность того, что частица будет двигаться в пределах угла 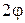 , где
, где  - угол, соответствующий первому (или центральному) дифракционному максимуму.
- угол, соответствующий первому (или центральному) дифракционному максимуму.
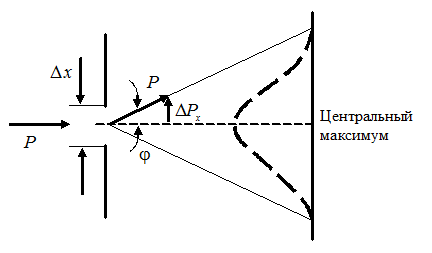 Таким образом, появ-ляется неопределенность
Таким образом, появ-ляется неопределенность
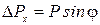 .
.
Из условия максимума интенсивности дифрак-ционной решетки, равно как и для одной щели, следует, что
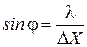 ,
,
где 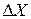 - ширина щели.
- ширина щели.
Подставив это значение в предыдущую формулу, получим:
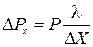 .
.
Длина волны микрочастицы, согласно формуле Де-Бройля, равна
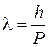 .
.
С учетом этого равенство примет вид
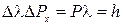 ,
,
что совпадает с выражением принципа неопределенностей Гейзенберга.
Вероятность нахождения микрочастицы в любой точке экрана в пределах центрального максимума может быть охарактеризована уже известной нам волновой функцией 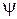 .
.
Произведение квадрата модуля волновой функции на элемент объема 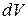 есть ни что иное, как вероятность того, что действие микрочастицы будет обнаружено в элементе объема
есть ни что иное, как вероятность того, что действие микрочастицы будет обнаружено в элементе объема 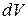 .
.
Т.е. эта вероятность равна 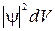 .
.
Сумма величин 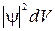 по всему пространству, или
по всему пространству, или 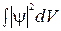 , есть вероятность обнаружения данной частицы в рассматриваемом пространстве. Так как частица существует, то она обязательно где-нибудь проявится – это достоверно. А вероятность достоверного события равна единице. Следовательно, волновая функция должна удовлетворять условию
, есть вероятность обнаружения данной частицы в рассматриваемом пространстве. Так как частица существует, то она обязательно где-нибудь проявится – это достоверно. А вероятность достоверного события равна единице. Следовательно, волновая функция должна удовлетворять условию
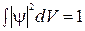 .
.
Это условие называется условием нормировки. Условие нормировки удовлетворяется подбором постоянного множителя. В дальнейшем мы будем считать, что все волновые функции, описывающие частицу, нормированы.
Знание волновой функции 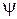 позволяет определить лишь вероятности процессов, но не позволяет определить процесс однозначно.
позволяет определить лишь вероятности процессов, но не позволяет определить процесс однозначно.
Если координаты микрочастицы, например электрона, не могут быть определены точно, то это происходит не из-за ограничений, накладываемых условиями опыта, а из-за того, что его положение в пространстве определяется не точечными значениями 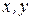 и
и 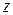 , а интервалами
, а интервалами 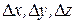 .
.
Следовательно, описание частицы с помощью волновых функций является не субъективным, а объективным.
Вернемся к принципу неопределенностей Гейзенберга. Он отражает, как мы установили, двойственную корпускулярно-волновую природу микрочастиц. Одного его соотношения достаточно, чтобы получить ряд важных результатов. В частности, он позволяет объяснить тот факт, что электрон не падает на ядро атома.
Если бы электрон упал на ядро, его координаты и импульс приняли бы определенные значения, что несовместимо с принципом неопределенности.
Принцип неопределенности является существенной частью квантовой теории. Ограничения, налагаемые на одновременность точного нахождения координат и импульса, не зависят от точности тех приборов, которыми пользуются при наблюдениях. Эта неопределенность, обусловлена не грубостью приборов, а самой природой изучаемых тел.
Координаты и импульс были введены в классической физике для характеристики движения обычных тел. Как показывает эксперимент, эти классические представления не применимы в микромире или применимы с большими ограничениями. Так как понятие координата волны в классической механике лишено физического смысла, то также не имеет смысла понятие траектории частицы.
Квантовая теория приводит также к соотношению неопределенностей между энергией 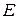 и временем
и временем 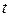
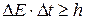 .
.
Энергия частицы в каком-либо состоянии может быть определена тем точнее, чем дольше частица находится в этом состоянии.
В заключение заметим, что соотношения Гейзенберга не являются утверждением о принципиальной ограниченности наших знаний о микромире. Они отражают лишь ограниченную применимость понятий классической физики в области микромира.
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 1096; Нарушение авторских прав?; Мы поможем в написании вашей работы!