
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Электроотрицательность
|
|
|
|
У одних атомов превалирует тенденция к потере электронов с превращением в положительные ионы, а другие стремятся приобрести электроны, переходя в отрицательные ионы. Не исключена возможность, что атом А к атому В является более электроположительным, а к атому С более электроотрицательным. Для сравнительной оценки этих свойств была введена особая характеристика, названная электроотрицательностью (Э.О).
Понятие электроотрицательности является условным. Оно позволяет оценить способность атома данного элемента оттягивать на себя электронную плотность по сравнению с атомами других элементов в соединении. Чем больше ЭО, тем сильнее атом элемента притягивает к себе электроны.
Мерой электроотрицательности может служить арифметическая сумма энергии ионизации I и сродства к электрону F

I и F следует брать в одних единицах:  ,
,  или
или 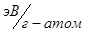 или на 1 моль.
или на 1 моль.
Согласно одному из определений (Мелликен) электроотрицательность атома может быть выражена как полусумма его энергии ионизации и сродства к электрону:
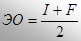
Имеется около 20 шкал электроотрицательности, в основу расчета значений которых положены разные свойства. Значения электроотрицательностей отличаются, но относительное расположение элементов в ряду электроотрицательностей, по Полингу ЭОфтора = 4,0.
ЭО имеет смысл оценивать для неметаллических элементов:
| H | ||||
| 2,15 | ||||
| B | C | N | O | F |
| 1,5 | 2,15 | 2,8 | 3,5 | 4,1 |
| Si | P | S | Cl | |
| 1,7 | 2,2 | 2,7 | 3,25 | |
| Ge | As | Se | Br | |
| 1,5 | 1,9 | 2,4 | 2,8 | |
| Sb | Te | J | ||
| 1,8 | 2,2 | 2,6 | ||
| Bi | Po | At | ||
| 1,6 | 2,0 | 2,4 |
Из этой сводки следует, что у элементов, расположенных в одном периоде (от Бора к F), ЭО возрастает слева направо.
У элементов, расположенных в одной группе ЭО наиболее выражена у стоящего выше элемента. Если их расположить по возрастанию ЭО, то получим следующий ряд:








 Ge, B, Bi, Si, Sb, As, Po, C, H, Te, P, Se, At, J, S, Br, N, Cl, O, F
Ge, B, Bi, Si, Sb, As, Po, C, H, Te, P, Se, At, J, S, Br, N, Cl, O, F
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 700; Нарушение авторских прав?; Мы поможем в написании вашей работы!