
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергия связи
|
|
|
|
Длина связи
Валентные углы
 Представление о направленности ковалентных связей позволяет объяснить взаимное расположение атомов в многоатомных молекулах. Например, при образовании воды Н2О электронные облака двух атомов водорода (s) в форме шара перекрываются с двумя неспаренными р-электронами.
Представление о направленности ковалентных связей позволяет объяснить взаимное расположение атомов в многоатомных молекулах. Например, при образовании воды Н2О электронные облака двух атомов водорода (s) в форме шара перекрываются с двумя неспаренными р-электронами.
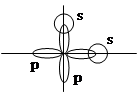 |
Поскольку р-электроны ориентированы во взаимно перпендикулярных направлениях, то молекула Н2О имеет угловое строение, угол между связи д.б. 90˚. См. также молекулу NH3. Она построена в форме пирамиды. Углы между связями или как их называют валентные углы = не 90˚; в молекуле воды угол НОН=104,5˚, а в аммиаке HNH=107,3˚, т.е. тому состоянию молекулы, которому соответствуют наименьшая потенциальная энергия, и образуется более прочная ковалентная связь.
Длинной связи d называют расстояние между центрами атомов, образующих данную связь. Экспериментальные методы позволили найти точную длину связей. Они имеют величину порядка 100 пм.
Например:
Н = 74 пм;
N2 = 110 пм;
О2 = 121 пм;
(С – С) = 154-158 пм;
(С = С) ≈ 134 пм;
(С ≡ С) ≈ 120 пм.
Определяют длину рентгеноструктурно и спектрально. Длина связи увеличивается с возрастанием атомного номера. При переходе от газов к кристаллам наблюдается увеличение длины связи, которое сопровождается её упрочнением. Длина связи позволяет также оценить жесткость связи, т.е. её сопротивляемость внешним воздействиям, вызывающем её длины.
Мерой прочности связи является энергия связи. Её величина определяется работой, необходимой для разрушения связи, или выигрышем в энергии при образовании вещества из отдельных атомов. например, энергия связи Н-Н в молекуле Н2 = 435 кДж/моль (104 ккал/моль), это значит, что при образовании 1 моля Н2 выделяется 435 кДж (104 ккал).
Н + Н = Н2 + 435 кДж/моль (104 ккал/моль)
Аналогичным путем можно оценить энергию химической связи и для других двухатомных молекул.
из свободных атомов:
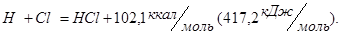
из простых веществ:
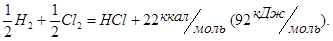
Эти данные позволяют оценить прочность связи:
С – С (85 ккал);
С = С (145 ккал);
С ≡ С (198 ккал).
Таким образом параметры связи – это энергия, длина, валентные углы, прочность, насыщаемость, направленность.
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 412; Нарушение авторских прав?; Мы поможем в написании вашей работы!