
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Закон распределения
|
|
|
|
Рассмотрим процесс перехода вещества из одной фазы в другую. При равновесии оно распределяется между этими фазами, например, двумя несмешивающимися жидкостями в определенном отношении. Если оба раствора разбавленные, то химический потенциал вещества в первой и второй фазах выражается уравнениями:
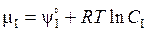 и
и 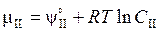
При равновесии 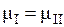 ,
, 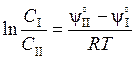 , и, следовательно, при постоянной температуре отношение
, и, следовательно, при постоянной температуре отношение
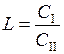 , (6.20)
, (6.20)
называемое коэффициентом распределения, является постоянной величиной, не зависящей от концентрации вещества в обеих жидкостях. Величины С 1и С 2 могут изменяться (например, при удалении вещества или разбавлении), но их отношение при равновесии должно оставаться постоянным. Оно определяется природой растворителей и растворенного вещества и температурой. Последняя зависимость, как и для константы равновесия, определяется уравнением
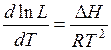
где ∆ Н – изменение энтальпии при переходе растворенного вещества из второй жидкости в первую.
Соотношение (6.20) является выражением закона распределения. Этот закон относится не только к распределению вещества между жидкостями, но имеет значительно более общий характер. Так, рассмотренный выше закон Генри является частным случаем закона распределения. Этот важный закон был сформулирован и разработан В. Нернстом, А. Яковкиным, Н. А. Шиловым.
В форме, выражаемой уравнением (6.20), закон распределения справедлив, если растворённое вещество имеет одинаковую молекулярную массу в обеих жидкостях. В случае ассоциации или диссоциации так же, как и в выражении закона Генри, необходимо учесть изменение молекулярной массы растворённого вещества. Если в жидкости она равна M I, а во второй M II, то уравнение (6.20) принимает следующий вид:
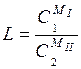
Как следует из приведенного вывода, закон распределения в виде уравнения(6.20) соблюдается лишь для разбавленных растворов.
Закон распределения имеет большое значение для анализа металлургических процессов. Чугун и шлак, сталь и шлак, шлак и штейн представляют собой пары несмешивающихся жидкостей, между которыми распределяется различные растворяющиеся в них элементы или соединения. Это явление используют для рафинирования расплавленных металлов от вредных примесей. Например, сталь очищают от серы, фосфора и кислорода при помощи жидкого шлака, в который переходят эти элементы. Распределение серы между железом и шлаком, состоящим только из окислов железа при 1600 оС, характеризуется отношением
(%S)/[%S] = LS ≈ 4
Металлургические шлаки представляют собой растворы, состоящие из различных оксидов (CaO, FeO, SiO2 и др.), а не однокомпонентную жидкость. Поэтому LS зависит от состава шлака. Далее будет показано, что L S увеличивается при уменьшении (FeO) и (SiO2 ).
Снижение концентрации серы в шлаке должно привести и к уменьшению её содержания в стали. Например, путём окисления серы при продувке шлака кислородом, увеличение количества жидкого шлака в печи или его скачивания с последующим наведением свежего шлака можно достаточно полно очистить сталь от серы. Закон распределения описывает также равновесие между разбавленными твёрдыми растворами или жидким и твёрдым растворами, например распределение примесей между твёрдой и жидкой фазами при кристаллизации. Это явление эффективно используется для очистки материалов методом зонной плавки.
Различные отрасли техники (атомная энергетика, полупроводниковая электроника, жаропрочные материалы) требуют производства очень чистых металлов. О необходимой степени чистоты материалов, применяемых в ряде специальных случаев, можно судить по используемому для их оценки способу выражения концентрации – число атомов примеси на 106 атомов основного метала (р.р.m. – parts per million, т.е. число частей на миллион).
Обычные методы выплавки и рафинирования не обеспечивают получения металлов со столь низкими концентрациями примесей. В связи с этим получили распространения новые способы производств, к числу которых относится выплавка и разливка металлов и сплавов в вакууме, рафинирование металла водородом для удаления из него следов углерода, серы, кислорода, электрошлаковый переплав и др.
Одним из наиболее эффективных методов глубокой очистки материалов является зонная плавка, изобретённая в 1952 г В. Пфаном. Метод основан на явлении распределения примеси между контактирующими в процессе плавления твёрдой и жидкой фазами. В этом случае закон распределения имеет вид 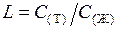 , где C (Т) и C (ж) – концентрации примеси в твёрдой и жидкой фазах при равновесии.
, где C (Т) и C (ж) – концентрации примеси в твёрдой и жидкой фазах при равновесии.
Часто величину L называют коэффициентом распределения. Если L < 1, то при плавлении материала образующаяся жидкость обогащается примесью, а равновесная твёрдая фаза очищается от этой примеси. В реальных условиях распределение примеси в соответствии с величиной L имеет место лишь в тонких слоях жидкой и твёрдой фаз, где успевает установиться равновесие. Вообще же распределение характеризуется величиной эффективного коэффициента L ´, которая зависит от условий затвердевания и скорости перемещения зоны расплавленного металла.
Схематически процесс зонной очистки металлического стержня, содержащего равномерно распределённую примесь при концентрации C 0, при помощи передвигающегося кольцевого нагревателя H (например, индуктора высокочастотного генератора) показан на рис. 6.5. Сначала расплавляют узкую зону, совпадающую с левым концом стержня. Так как эта зона слева не контактирует с твёрдой фазой, то концентрация примеси в ней остаётся равной C 0. Незначительное передвижение нагревателя в правую сторону приведёт к кристаллизации металла слева от нагревателя и перемещению расплавленной зоны в правую сторону. В первой порции затвердевшего металла концентрация примеси составит C = L ´ C 0, и, так как L ´ < 1, она будет меньше исходной. Дальнейшее перемещение расплавленной зоны приводит к увеличению концентрации примеси в жидкости и накоплению примеси в правом конце стержня. Многократное прохождение зоны вдоль стержня приводит к глубокой очистке металла и достижению особых свойств.
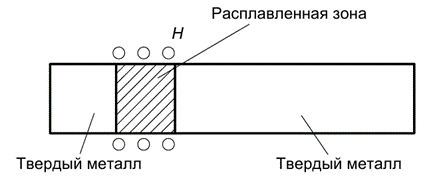
Рис.6.5. Схема зонной плавки
Примером может служить очистка германия, используемого в качестве полупроводникового материала. Присутствие в этом металле ничтожных количеств меди, железа, никеля резко изменяет его проводимость и делает непригодным для применения в радиотехнических устройствах. Очистка зонной плавкой снижает содержание указанных элементов до концентрации, меньшей, чем один атом примеси на 1010 атомов германия.
|
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 1424; Нарушение авторских прав?; Мы поможем в написании вашей работы!