
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Адсорбция ионов из растворов на твердых поверхностях. Образование двойного электрического слоя
|
|
|
|
Адсорбция электролитов не укладывается в рамки учения о молекулярной адсорбции.Сильные электролиты адсорбируются в виде ионов и в ходе их адсорбции действуют химические силы а не ван-дер-вальсовы, как в случае молекулярной адсорбции.
На адсорбцию ионов существенным образом влияет природа адсорбента. Ионы, способные поляризоваться, адсорбируются обычно только на поверхностях, состоящих из полярных молекул или из ионов. Микроучастки поверхности, несущие определенный заряд, адсорбируют противоположно заряженные ионы. При этом ионы электролита, несущие противоположный знак адсорбировавшимся ионам, непосредственно не адсорбируются, но под действием сил электростатического притяжения остаются вблизи адсорбированных ионов, образуя вместе с ними двойной электрический слой. Строение этого слоя подробно будет рассмотрено в следующей лекции, посвященной электрическим свойствам коллоидных частиц.
Радиус ионов сильно влияет на их способность адсорбироваться. Из ионов одинаковой валентности максимальную адсорбционную способность проявляют ионы наибольшего радиуса. Причина этого явления, с одной стороны, заключается в большей поляризуемости таких ионов и, следовательно, их способности притягиваться поверхностью, состоящей из ионов или полярных молекул; с другой стороны, в меньшей степени гидратации этих ионов (чем больше радиус иона, тем меньше при одном и том же заряде его гидратация). Гидратация (сольватация) вообще препятствует адсорбции ионов, поскольку наличие гидратной оболочки уменьшает электрическое взаимодействие.
Катионы и анионы одинакового заряда можно расположить в порядке уменьшения их сродства к воде (каждый последующий гидратируется хуже). Эти ряды называются лиотропными рядами, или рядами Гофмейстера. Так, одновалентные катионы можно расположить в следующий ряд по уменьшающейся степени гидратации и, следовательно, возрастающей способности адсорбироваться:
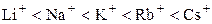 .
.
Для двухвалентных катионов это будет следующий ряд
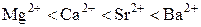 .
.
Одновалентные анионы по их возрастающей способности адсорбироваться располагаются в следующей последовательности:
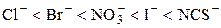 .
.
Из этого видно что, адсорбционная способность меняется обратно пропорционально степени гидратации ионов и прямо пропорционально их размерам.
Адсорбционная способность ионов весьма сильно зависит также от их валентности. Чем больше валентность иона, тем сильнее он притягивается противоположно заряженными микроучастками поверхности. Катионы различной валентности по из возрастающей адсорбционной способности можно расположить в следующий ряд:
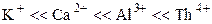 .
.
Особый интерес для геологов должна представлять адсорбция ионов поверхностью кристалла, в состав которого входят ионы той же природы. При этом адсорбцию можно рассматривать как кристаллизацию, т. е. как достройку кристаллической решетки адсорбирующимся ионом. Согласно Панету и Фаянсу, кристаллы достраиваются лишь теми ионами, которые входят в их состав, или изоморфными с ними. Например, кристаллы AgI, внесенные в раствор KI, адсорбируют на поверхности иодид–ионы. Если же кристаллы AgI внести в раствор AgNO3, то происходит адсорбция ионов серебра. Понятно, что силы, под влиянием которых происходит такая достройка, являются химическими и одновременно электростатическими, и ионы, достраивающие кристалл, адсорбируются в этом случае особенно прочно.
Если на поверхности адсорбента уже адсорбирован электролит, то при контакте этого адсорбента с другим электролитом почти всегда в той или иной степени протекает обменная адсорбция, или, правильнее, обмен ионов между двойным электрическим слоем адсорбента и средой. При обменной адсорбции адсорбент, поглощая определенное количество каких–либо ионов, одновременно выделяет в раствор эквивалентное количество других ионов того же знака, вытесненных с поверхности.
Обменная адсорбция имеет ряд особенностей:
1). Обменная адсорбция специфична, т. е. к обмену способны только определенные ионы.
2). Обменная адсорбция не всегда обратима.
3). Обменная адсорбция протекает достаточно медленно.
4). При обменной адсорбции может изменяться рН среды, если ионом, обмениваемым адсорбентом, является водородный или гидроксильный ион.
|
|
|
|
Дата добавления: 2013-12-13; Просмотров: 1498; Нарушение авторских прав?; Мы поможем в написании вашей работы!