
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные понятия
|
|
|
|
Титриметрический (объемный) анализ.
Химические титриметрические методы анализа
Титриметрический, или объёмный, анализ - метод количественного анализа, основанный на измерении объема (или массы) реагента Т, затраченного на реакцию с определяемым веществом X. Другими словами титриметрический анализ - это анализ, основанный на титровании.
Титрование - процесс определения вещества X постепенным прибавлением небольших количеств вещества Т, при котором каким-либо способом обеспечивают обнаружение точки (момента), когда все вещество X прореагировало. Титрование позволяет найти количество вещества X по известному количеству вещества Т, прибавленного до этой точки (момента), с учетом того, что соотношение, в котором реагируют X и Т, известно из стехиометрии или как-то иначе.
Титрант - раствор, содержащий активный реагент Т, с помощью которого проводят титрование.
Титрование проводят, прибавляя титрант из калиброванной бюретки в колбу для титрования, в которую перед титрованием вносят аликвотную долю анализируемого раствора.
Аликвотная доля (аликвота) - это точно известная часть анализируемого раствора, взятая для анализа. Она отбирается калиброванной пипеткой и её объём обычно обозначается символом Vn.
Точка эквивалентности (ТЭ) - такая точка (момент) титрования, в которой количество прибавлённого титранта Т эквивалентно количеству титрируемого вещества X.
Конечная точка титрирования (ККТ) - (момент) титрования, в которой некоторое свойство раствора (например, его окраска) оказывает заметное (резкое) изменение. ККТ может как как совпадать, так и не совпадать с ТЭ.
Индикатор — вещество, которое проявляет видимое изменение в ТЭ. В идеальном случае индикатор присутствует в достаточно малой концентрации, чтобы в интервале его перехода не затрачивалось существенное количество титранта Т. Резкое видимое изменение индикатора (например, его окраски) соответствует КТТ.
Интервал перехода окраски индикатора - область концентрации ионов водорода, металла или других ионов, в пределах которой глаз способен обнаружить изменение в оттенке, интенсивности окраски, флуоресценции или другого свойства визуального индикатора, вызванное изменением соотношения двух соответствующих форм индикатора. Эту область обычно выражают в виде отрицательного логарифма концентрации (например, рН = -lg c(H3O+)). Для окислительно-восстановительного индикатора интервал перехода представляет собой соответствующую область окислительно-восстановительного потенциала.
Степень оттитрованности f - отношение объема V (Т) добавленного титранта к объёму V(ТЭ) титранта, соответствующему ТЭ:
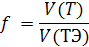
То есть, степень оттитрованности раствора — это отношение количества оттитрованного вещества к его исходному количеству в анализируемом растворе.
Уровень титрования - это порядок (10-x) концентрации используемого раствора титранта, например 10-1, 10-2, 10-3 и т. д.
Кривая титрирования – графическое изображение зависимости изменения концентрации с(Х) определяемого вещества Х, или некоторого связанного свойства системы (раствора) от объема V (Т) прибавленного титранта Т. Величина с(Х) в ходе титрования изменяется на несколько порядков, поэтому кривая титрования часто строится в координатах lgc(X)-V(T).
По оси абсцисс откладывают объем прибавляемого титранта V(T) или степень оттитрованности f.
Если по оси ординат откладывать равновесную концентрацию с(Х), или интенсивность пропорционального ей свойства, то получают линейную кривую титрования.
Если по оси ординат откладывать lg c(X), то получают логарифмическую кривую титрирования.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1188; Нарушение авторских прав?; Мы поможем в написании вашей работы!