
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Равновесия в водных растворах ЭДТУК
|
|
|
|
Комплексоны — это чаще всего многоосновные аминополикарбоновые кислоты и их соли, анионы которых, выступая в роли полидентатных хелатообразующих лигандов, способны образовывать со многими катионами металлов устойчивые растворимые комплексы — комплексонаты.
Комплексоны.
При комплексонометрическом титровании в результате реакции между катионом металла и комплексоном образуется комплексонат металла.
Как правило, комплексонаты металлов содержат один сложный циклообразующий лиганд, приходящийся на один катион металла-комплексообразователя, или, как говорят, комплекс имеет состав 1:1.
Известно большое число комплексонов, например, комплексоны I—IV, перечисленные ниже.
Комплексон I, или нитрилотриуксусная кислота N(CH2COOH)3.
Комплексон II, или этилендиаминтетрауксусная кислота (ЭДТУК)
(HOOCCH2)2N – CH2CH2 - N(CH2COOH)2,
имеющая бетаиновое строение (два протона связаны с атомами азота):

 -OOCH2C H+ H+ CH2COO-
-OOCH2C H+ H+ CH2COO-
 N – CH2 – CH2 – N
N – CH2 – CH2 – N
 HOOCH2C CH2COOH
HOOCH2C CH2COOH
Эту четырехосновную кислоту, как уже отмечалось выше, часто сокращенно обозначают символом Н4Y; такое обозначение мы будем использовать в дальнейшем.
Комплексон III, Na2H2Y·2H2O – двунатриевая соль ЭДТУК; этот комплексон часто называют также ЭДТА (этилендиаминтетраацетат), трилон Б, хелатон III и т.д. Комплексонаты металлов, образованные катионами металлов с ЭДТА, называют также «эдетеатами», в отличии от комплексов с другими комплексонами.
Комплексон IV - диаминциклогексантетрауксусная кислота
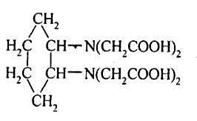
В титриметрическом анализе наиболее широко применяется комплексон III; остальные комплексоны, а их известно несколько десятков, применяются в титриметрии реже.
Комплексон H4Y — четырехосновная кислота. В сильно кислых растворах при рН < 1,6 она протонируется: протоны присоединяются к молекуле ЭДТУК образуя протонированные формы (катионы) H5Y+ и H6Y2+:



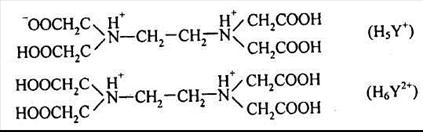
Кислотная диссоциация H6Y2+ протекает ступенчато:
H6Y2+ = H+ + H5Y+, pK1 = 0,9,
H5Y+ = H+ + H4Y, pK2 = 1,6,
H4Y = H+ + H3Y-, pK3 = 2,00,
H3Y- = H+ + H2Y2-, pK4 = 2,67,
H2Y2- = H+ + HY3-, pK5 = 6,16,
HY3- = H+ + Y4-, pK6 = 10,26.
В водных растворах сосуществуют и находятся в равновесии все 7 форм ЭДТУК, однако, в зависимости от кислотности среды, доминирует та или иная форма в интервалах ∆рН изменений рН раствора:
 рН раствора доминирующая форма
рН раствора доминирующая форма

 <0,7 H6Y2+
<0,7 H6Y2+
|
~1,6-1,8 H4Y – нейтральная молекула
 ~1,9-2,6 H3Y-
~1,9-2,6 H3Y-
|
 2,8-6,1 H2Y2-
2,8-6,1 H2Y2-
6,2-10,2 HY3-
>10,5 Y4-
Максимальная относительная концентрация каждой формы соответствует приблизительно середине соответствующего интервала изменения рН.
Общая концентрация с(Y) всех незакомплексованных (не связанных в комплексах) равновесных форм ЭДТУК в растворе равна сумме концентраций всех форм:
С(Y) = [H6Y2+] + [H5Y+] + [H4Y] + [H3Y-] + [H2Y2-] + [HY3-] + [Y4-].
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2546; Нарушение авторских прав?; Мы поможем в написании вашей работы!