
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Розпад та перетворення амінокислот
|
|
|
|
Денатурація білків
Вплив інших факторів на структуру білків
Температурна обробка білків
Розпад та перетворення амінокислот
Денатурація білків
Біохімічні перетворення білків у технологічному процесі
Лекція №14
Зміст:
Будь-яка зміна умов середовища в технологічному процесі виробництва харчових продуктів впливає на не ковалентні зв’язки молекулярної структури і призводить до порушення четвертинної, третинної і вторинної структури білка. Порушення нативної структури призводить до втрати біологічної активності (ферментативної, гормональної) і називається денатурацією білка. Це відбувається без зміни первинної структури.
Більшість білків денатурують у присутності кислот, лугів, нагріванні і охолодженні, обробці ПАР, важкими металами(Ag, Pb, Hg), органічними розчинниками (етанол, метанол, ацетон). Ця властивість білків застосовується для їх виділення з харчової сировини, а фактори, які впливають на денатурацію (присутність інших речовин) використовуються для підвищення або зниження активності ферментів.
Більшість білків денатурує при 60-80°С, але є і такі: ферменти термофільних мікроорганізмів, лактоглобулін молока. Така властивість термостійких білків пояснюється наявністю в молекулі великої кількості дисульфід них зв’язків. Теплова денатурація білка – основний процес, що відбувається у процесі випікання хліба, печива, бісквітів, сушіння макаронних виробів, одержання сухих сніданків, варіння і смаження овочів, риби, м’яса, стерилізації молока і т.д.
Цей процес прискорює травлення білків у шлунково-кишковому тракті, так як полегшує доступ до них ферментів і обумовлює органолептичні і споживчі властивості харчових продуктів, наприклад пористу структуру хліба і м’якість м’яса.
Але ступінь денатурації може бути різною – до повного порушення структури і утворення нових пептидних і дисульфідних зв’язків. Засвоєння таких полімерів погіршується. Так, переварене яйце, пересмажене м’ясо засвоюються гірше.
Продукти гідролітичного розпаду білків – амінокислоти є джерелом живлення мікроорганізмів. Токсичні продукти можуть утворюватися при мікробному псуванні білкових продуктів. Розщеплення білків і їх похідних, викликане мікроорганізмами одержало назву гниття.
Найчастіше розпад амінокислот йде шляхом окислювального дезамінування, в результаті утворюються аміак і α-кетокислоти.
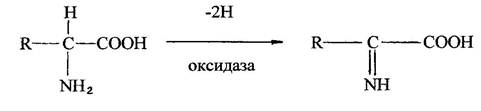
Потім амінокислота приєднуючи воду розпадається на кетокислоту і аміак:
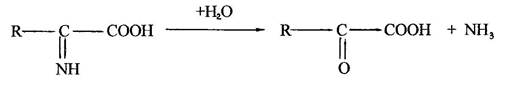
Також гідролітичне дезамінування 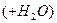 утворює оксикислоти, а відновлення
утворює оксикислоти, а відновлення 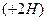 - жирні кислоти. При розкладі амінокислот по схемі так званого внутрішньо-молекулярного дезамінування утворюються ненасичені жирні кислоти і аміак:
- жирні кислоти. При розкладі амінокислот по схемі так званого внутрішньо-молекулярного дезамінування утворюються ненасичені жирні кислоти і аміак:
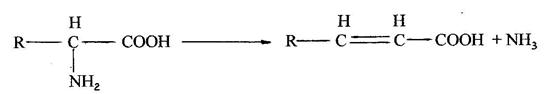
Деякі кетокислоти і оксикислоти можуть надалі перетворюватись, при каталітичній дії декарбоксилаз в альдегіди і вуглекислий газ:
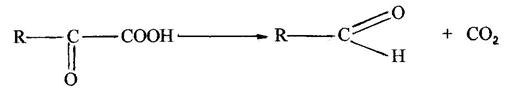
а оксикислоти у спирти і вуглекислий газ:
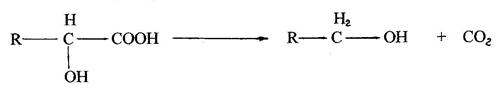
У більшій кількості утворюються оцтова і масляна, а потім мурашина і пропіонова кислота, які надають продуктам неприємний запах.
Розповсюдженим процесом розпаду амінокислот під дією декарбоксилаз мікроорганізмів, являється утворення вуглекислого газу і відповідного аміну. З гістидину утворюється гістамін, з тирозину – тирамін, з лізину – кадаверін, з орнітину – путресцин, які мають сильну фармакологічну дію.
Інші бактеріальні ферменти викликають специфічні перетворення ряду амінокислот. Так, при розпаді триптофану утворюється індол і скатол, постуаово руйнується боковий ланцюг, залишаючи цілою кільцеву структуру.
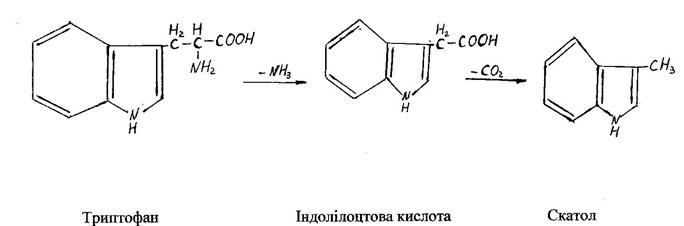
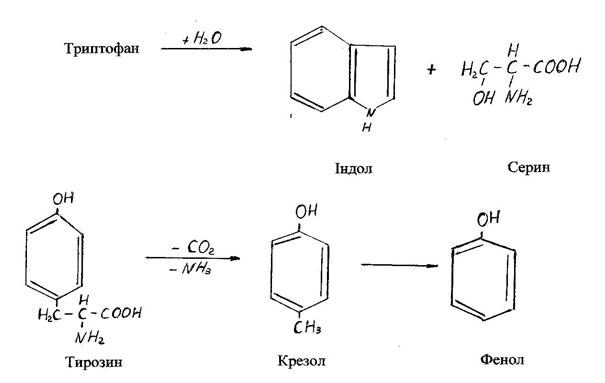
Специфічні перетворення тіоамінокислот під дією ферментів мікроорганізмів ведуть до утворення сірководню і меркаптанів.
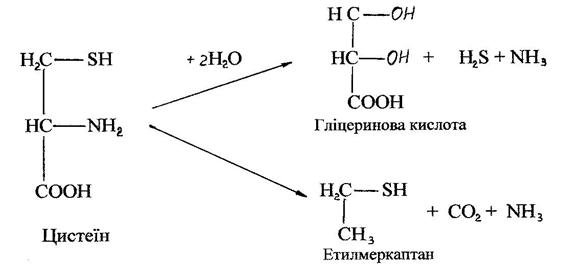
Індол, скатол, крезол, сірководень і меркаптан – отруйні і з неприємним запахом речовини.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2310; Нарушение авторских прав?; Мы поможем в написании вашей работы!