
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Удаление фосфора (дефосфорация)
|
|
|
|
Влияние фосфора на свойства можно определить из диаграммы состояния Fe-P. Растворимость фосфора в a-Fe снижается при температуре меньше 1050 оС, то есть в условиях низкой диффузионной способности. Это приводит к образованию метастабильных растворов в стали, к напряжению решетки железа и снижению пластичности (особенно в областях низких температур).
При нагревании метастабильные растворы распадаются с выделением Fe3P по границам зерен металла, которые обладают повышенной хрупкостью. Пластические свойства металла при этом ухудшаются. Такое явление называется отпускная хрупкость или хладноломкость металла.
Фосфор является склонным к перераспределению по объему слитка в процессе кристаллизации. Это явление называется ликвационной способностью.
В стали обычного качества содержание фосфора не должно превышать 0,045 % в любом месте слитка. Следовательно, с учетом ликвационной способности, в жидком металле содержание фосфора должно быть меньше 0,01- 0,015 %.
Дефосфорация металла заключается в переводе фосфора из металла в шлак. Этот перевод в чистых сплавах Fe-P при отсутствии примесей можно осуществить по реакции
2[P] + 5(FeO) = (P2O5) + 5[Fe]. (7.1‑21)
При наличии углерода в металле, углерод будет восстанавливать фосфор из оксида, т.к. обладает большим сродством к кислороду, чем фосфор, то есть углерод окисляется за счет кислорода (Р2О5) по реакции
(P2O5) + 5[С] = 2[P] + 5{CO}. (7.1‑22)
Единственный путь удаления фосфора – связывать его в прочное химическое соединение тетрафосфат кальция (4CaO× P2O5)
(P2O5) + 4(CaO) = (4CaO × P2O5). (7.1‑23)
Таким образом, дефосфорация протекает в две стадии:
1. Окисление фосфора металла кислородом (FeO) по реакции (7.1-21) и переход (P2O5) в шлак.
2. Перевод (P2O5) в прочное химическое соединение (4CaO× P2O5) по реакции (7.1-23).
Суммируя первую и вторую стадии получаем
2[P] + 5(FeO) + 4(CaO) = (4CaO × P2O5) + 5[Fe]. (7.1‑24)
Тепловой эффект реакции (7.1-24) составляет 1370 кДж/моль. Полнота протекания процесса характеризуется коэффициентом дефосфорации
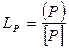 . (7.1‑25)
. (7.1‑25)
В нашем случае 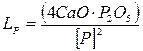 . (7.1‑26)
. (7.1‑26)
Чем полнее прошла дефосфорация, тем выше коэффициент дефосфорации. Зависимость LP от состава шлака и температуры можно установить из уравнения суммарной реакции (7.1-24)
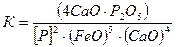 . (7.1‑27)
. (7.1‑27)
Видно, что в выражение (7.1-27) входит выражение (7.1-26). Следовательно
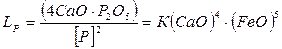 . (7.1‑28)
. (7.1‑28)
Полнота протекания реакции (коэффициент дефосфорации) зависит от состава шлака и температуры и возрастает с ростом основности шлака ( СаО), с ростом окисляющей способности шлака ( FeO), с увеличением константы равновесия, следовательно, с понижением температуры (для экзотермических реакций с ¯ t оС, К). Таким образом, дефосфорация происходит на начальных стадиях сталеварения.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 2513; Нарушение авторских прав?; Мы поможем в написании вашей работы!