
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Работа на газовом хроматографе
|
|
|
|
Определение нитрогеназной активности симбиотических азотфиксирующих бактерий
При определении нитрогеназной активности на интактных клубеньках в пенициллиновый флакон помешают отмытые и просушенные фильтровальной бумагой корни бобового растения с клубеньками. Шприцем вводят ацетилен (10% избыточного давления ацетилена) и после экспозиции в течение 1 ч в условиях теплицы или других помещений (в зависимости от целей эксперимента) реакцию останавливают введением 1 — 5 мл реактива Несслера, который связывает оставшийся ацетилен. Образцы можно хранить в холодильнике при 4°С длительное время до анализа на хроматографе.
При определении нитрогеназной активности и интактной бобово-ризобиальной системы осторожно извлекают растение с клубеньками из почвы или другого субстрата. Очищают клубеньки, стряхивая почву с корней, и помешают растение до корневой шейки в полиэтиленовый пакет. Пакет закрывают резиновой пробкой, предварительно разрезанной вдоль на две половины и имеющей отверстие для стебля растения. Растение размещают так, чтобы надземная часть была расположена над пробкой, а корневая система — в пакете. Щели между отверстием в пробке и стеблем заделывают замазкой.
Воздух из пакета откачивают. Через специальное отверстие в пробке шприцем вводят в пакет 50 см3 газовой смеси (15% ацетилена, 20% кислорода и 65% аргона). Газовую смесь готовят непосредственно перед опытом в газометре, представляющем собой сосуд, заполненный 30%-ным раствором NaCl, объем которого равен объему вводимых газов. Через 10— 15 мин шприцем отбирают из газовой смеси образец в 5 мл и переносят его в закрытый шприц-сборник для анализа методом газовой хроматографии.
В полевых условиях при определении азотфиксирующей активности бобово-ризобиальной системы методом «колпаков» цилиндр не следует углублять в почву более чем на 10 см, так как основная масса клубеньков локализована в верхнем слое. Колпаки проверяют на герметичность водой. Для обеспечения концентрации ацетилена, равной 5—10%, на колпак высотой 60—70 см рекомендуется вносить 35—40 г карбида кальция и 20 мл пропана.
Количество образовавшегося в ходе определения азотфиксирующей активности помпы этилена определяют при помощи пламенно-ионизационного детектора на газовых хроматографах любой марки.
Для разделения газов используют сорбенты ACM, TЗK-M и др. Газами-носителями служат инертные газы аргон, гелий или азот. Количество восстановленного этилена определяют по стандартным пикам, для чего готовят стандартный раствор этилена.
Пример расчёта. В случае, если разведение стандартного раствора 1:1000, 1 мл 100%-ного этилена разводят в герметичной емкости на 1 л. Исходя из закона Авогадро, 1 моль газа этилена занимает объем 22,4 л. Рассчитаем, сколько молей занимает интересующий нас объем (0.001 л):
1 моль этилена занимает объем 22,4 л
 Х этилена 0,001 л
Х этилена 0,001 л
Х = 1·0,01 ׃ 22,4 = 44,6 ·10-9(моль) = 44,6 (нмоль).
Вводя в хроматограф данное количество стандартного этилена (1 мл) с известной размерностью (44,6 · 10 -9 моль), получаем величину стандартной пробы в сантиметрах, относительно которой рассчитывают опытные пробы.
Пробы из опытных образцов вводят в хроматограф и получают величины пиков в миллиметрах на разных шкалах чувствительности хроматографа, которые впоследствии приводят к размерности стандартной пробы и к единому объему вводимой пробы.
Для сравнительной оценки активности бобово-ризобиальной системы ацетиленовым методом данные вычисляют с помощью следующей формулы (в нмолях восстановленного этилена за 1 ч в расчете на одно растение):

где А - количество этилена (С2Н2) в нмолях на реакционный флакон (аптечный флакон на 30 мл) в единицу времени; Р2 — пик диаграммы пробы из реакционного флакона в см (при наличии примеси этилена и исходном ацетилене пик фона вычитают): Р1 — усредненный пик диаграммы пробы стандарта в см; К1 — калибровка (чувствительность) прибора при анализе пробы стандарта; К2 — калибровка прибора при анализе пробы из флакона; V1 — объем пробы стандарта в см3; V2 — объем испытуемой пробы из флакона в см3; V3 — объем реакционного флакона в см3; t — время экспозиций в ч; n — число корней во флаконе; 44,6 — количество С2Н2 (нмоль в 1 см3) в пробе стандарта.
Работу следует нести при одинаковой калибровке (чувствительности) прибора при анализе проб из флакона и стандарта, тогда К2 / К1 = 1. Лучше, если объемы проб из стандарта и флакона равны, например составляют 0,5 мл. Тогда V1 / V2 = 1. В каждый флакон следует «водить ацетилен в количестве, равном 5% объема флакона (так, во флакон на 30 мл вводят 2 см3 ацетилена, на 130 мл— 6 см3 ацетилена). Время экспозиции — 1 ч. Для этих условий формула (1) приобретает вид:
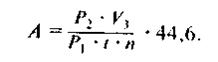 (2)
(2)
Вследствие того что в каждой анализируемой партии образцов величины V3 (объем флакона) и Р1 (средняя величина пиков стандарта для всех определений) одни и те же, число корней также равное, формула еще более упрощается:
 (3)
(3)
Таким образом, для определения количества С2Н4 в нмолях, образовавшегося во флаконе за 1 ч в расчете на 1 растение, пик диаграммы пробы из каждого флакона умножают на коэффициент С, рассчитанный предварительно.
Пример расчета. К1 = К2 = 20 · 10-10; V1 = V2 = 0,5 см3; V3 = 43 см3; t = 1 ч; n = 1; отдельные показатели Р1 составляют 11,4; 11,5; 11,4; средний Р1 — 11,4 см. Отсюда:

Флакон № 1: Р2 = 16,2 см; А1 = 16,2 • 168,2 = 2725 (нмоль С2Н4 /растение /ч).
Флакон № 2: Р2 = 15,8 см; А2 = 15,8 · 168,2 = 2658 (нмоль С2Н4/растение/ч) и т. д.
Если результаты хотят выразить в мкг фиксированного азота за 1 ч на 1 растение (мкг N/растение/ч), проводят пересчет: количество этилена в нмоль С2Н4/растение/ч умножают на 0,0093 (28 / 3 • 10 -3), где 28 — молекулярная масса азота; 10 -3 — множитель для пересчета нмоль в мкг, так как 1 нмоль = 10 -9 моль, а 1 мкг = 10 -6 г; 3 — коэффициент (см. 12.4.2).
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 723; Нарушение авторских прав?; Мы поможем в написании вашей работы!