
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Водородная связь
|
|
|
|
Водородная связь (Н-связь) – это связь, образуемая протонированным атомом водорода с сильноэлектроотцательным атомом той же или другой молекулы. В обычных условиях валентность водорода равна 1, и он способен обобществлять с другими атомами одну электронную пару, образуя ковалентную связь: атом водорода может присоединять электрон, образуя гидрид-ион Н+.
Атом водорода обладает особенностью, отличающей его от всех остальных атомов: отдавая свой электрон, он остается в виде ядра без электронов, т.е. в виде частицы, диаметр, которой в тысячи раз меньше диаметра остальных атомов. При отсутствии электронов ион Н+ не отталкивается электронными оболочками других атомов или ионов, а наоборот, притягивается; он может близко подходить к другим атомам, взаимодействовать с их электронами и даже внедряться в их электронные оболочки. В жидкостях Н+-ионы большей частью не сохраняется в виде самостоятельной частицы, а связываются с молекулами двух веществ: в воде с молекулами воды, образуя ион Н3О+-ион гидроксония; с молекулой аммиака – NH4+-ион аммония.
Будучи связанным с атомом одного из наиболее электроотрицательных элементов: с атомом фтора, кислорода, хлора и азота, атом водорода приобретает относительно высокий положительный заряд, не превышающий единицу. Так как этот заряд сосредоточен на чрезвычайно малом атомном остове, он сильно приближается к другому атому, несущему отрицательный заряд. Это вызывает образование довольно сильной диполь-дипольной связи с энергией 20-30 кДж/моль и больше. Водородная связь возникает в результате междипольного взаимодействия двух сильно полярных связей, принадлежащих различным молекулам или одной и той же молекуле. Она слабее обычной ковалентной связи, энергия которой составляет приблизительно 125-420 кДж/моль и может усиливаться вследствие взаимной поляризации связей, обусловленной указанными особенностями водородного атома. Водородная связь (Н-связь) обозначается Х-Н××××Х.
Атом водорода, участвующий в водородной связи, может располагаться точно посередине между двумя сильноотрицательными атомами – симметричное расположение или же смещаться ближе к тому из них, который имеет большую электроотрицательность – несимметричное расположение.
Энергии водородной связи достаточно, чтобы при обычных и пониженных температурах вызывать заметную диссоциацию молекул. Фтористый водород даже вблизи температуры кипения имеет средний состав (HF)4. Ассоциация приводит к аномально высоким температурам плавления и кипения фтороводорода. Существование димера H2F2 объясняет образование кислых солей типа KHF2×NaHF2. Тот факт, что фтористоводородная кислота, в отличие от хлористоводородной, бромистоводородной и иодистоводородной, представляет собой слабую кислоту (Кд = 7×10-4) – тоже является следствием ассоциации молекул HF из-за водородных связей.
При наличии несимметричной водородной связи, которая возникает в соединениях кислорода и азота, водород располагается немного ближе к одному из двух соседствующих атомов, здесь межмолекулярная Н-связь. Каждая молекула Н2О участвует в образовании двух Н-связей, так что атом кислорода оказывается связанным с четырьмя атомами водорода. Ассоциированные молекулы воды образуют ажурную пространственную структуру, где каждый атом кислорода располагается в центре тетраэдра, а в углах находятся атомы водорода.
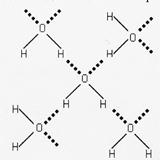
Ажурная пространственная структура воды
Ажурной структурой льда объясняется его меньшая плотность, чем воды. При плавлении часть Н-связей рвется и увеличивается плотность воды, т.к. молекулы располагаются более плотно. Рентгеновское исследование показало, что для большей части молекул в жидкой воде сохраняется также тетраэдрическое окружение: расположение соседних молекул почти такое же, как и в кристалле льда, а в последующем слое повторяется
некоторое отклонение от указанной упорядоченности; отклонение увеличивается по мере удаления от взятой молекулы. Для воды характерно наличие «ближнего порядка» как и для других жидкостей, и в меньшей степени, по сравнению с другими жидкостями, наличие «дальнего порядка». Этим объясняется наличие кристаллической структуры в воде.
Свойства воды такие как, большие значения теплоемкости и теплоты испарения, аномально высокие температуры плавления и кипения, высокая диэлектрическая проницаемость – из-за связанности молекул воды водородными связями. Без Н-связей tпл.воды = -100 оС, tкип.воды = -80 оС.
Водородные связи присутствуют в жидком аммиаке. Водородный атом, связанный с углеродом, может приобрести способность образовывать водородную связь, если остальные валентности углерода насыщаются сильно электроотрицательными атомами или соответствующими атомными группами, например, хлороформ (СНСl3), пентахлорэтан (CCl3-CHCl2), т.е. соседство электроотрицательных атомов может активировать образование водородной связи у атомов СН-групп, хотя электроотрицательность атомов С и Н почти одинакова. Этим объясняется возникновение Н-связей между молекулами в жидких HCN, CHF3 и др.
Водородная связь свойственна любым агрегатным состояниям вещества. Она образуется между одинаковыми и между различными молекулами, между различными частями одной и той же молекулы – внутримолекулярная водородная связь. Наиболее распространенной является Н-связь между молекулами, содержащими гидроксильные группы ОН-.
Простые эфиры даже с большей молярной массой более летучи, чем спирты, так как в эфирах все атомы водорода связаны с атомами углерода и не способны образовывать Н-связи.
Велика роль Н-связи в биохимических системах. Свойства белков и нуклеиновых кислот в значительной степени обусловлены наличием водородной связи. Н-связь играет большую роль в процессах растворения. Особенно распространены водородные связи в молекулах белков, нуклеиновых кислот и других биологически важных соединений, поэтому эти связи играют важную роль в химии процессов жизнедеятельности.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 535; Нарушение авторских прав?; Мы поможем в написании вашей работы!