
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Применение их соединений в медицине. Биологическая роль d-элементов IБ-группы
Биологическая роль d-элементов IБ-группы.
Медь Сu — необходимый микроэлемент живых организмов. Серебро Аg и золото Аu — примесные микроэлементы. Их соединения применяют в медицине.
Медь — биогенный элемент, содержится в тканях животных и растений. Общая масса меди в организме взрослого человека примерно 100 мг, что составляет около 0,0001%. Примерно 30% этого количества содержится в мышцах. Печень и мозг также богаты медью. Металлическая медь и ее соединения токсичны.
Наиболее важными с физиологической точки зрения являются медьсодержащие белки — цитохромоксидаза и супероксиддисмутаза.
Цитохромоксидаза — один из компонентов дыхательной цепи, локализованной в мембранах митохондрий. Обеспечивает клеточное дыхание, восстанавливая кислород до воды на конечном участке дыхательной цепи.
Цитохромоксидаза (М, = 200 000) состоит из семи белковых субъединиц и четырех связанных с ними активных центров: двух молекул тема, связывающих ионы железа, и двух ионов меди, непосредственно связанных с белковыми субъединицами. Такая структура цитохромоксидазы обеспечивает передачу четырех электронов из дыхательной цепи и осуществление реакции
О2 + 4Н+ + 4е~ →Цитохромоксидаза→ 2Н2О
При неполном восстановлении кислорода в дыхательной цепи образуется анион пероксида:
О2 + е~ -> О2-
Взаимодействие этого аниона с органическими соединениями клетки приводит к образованию радикалов и нарушению нормального развития клетки.
Повреждающее действие аниона предотвращается медьсодержащим ферментом супероксиддисмутазой (СОД). Этот фермент катализирует реакцию
О2- + О2- + 2Н+ → Н2О2 + О2
Образующийся при этом водородпероксид разлагается каталазой. В результате совместного действия содержание радикалов в клетке поддерживается на безопасном уровне.
Интересно, что переносчиком кислорода у моллюсков и членистоногих является не гемоглобин, а гемоцианин (от греч. кианос — лазурный). Кровь этих животных имеет голубой цвет.
Гемоцианин в зависимости от биологического вида имеет различную молекулярную массу (у омара Мг = 825000) и состоит из большого числа белковых субъединиц (Мг от 25000 до 35000). Каждая субъединица имеет центры связывания кислорода. Эти центры представляют собой медьпротеиновые комплексы кислорода (биокластеры) с двумя ионами меди. Каждая такая пара связывает одну молекулу кислорода.
Ежедневно организму требуется 2,5—5,0 мг меди. При недостатке в организме меди может развиваться болезнь — медьдефицитная анемия. Медь необходима для усвоения железа, в частности, при синтезе цитохромоксидазы, которая содержит и железо, и медь. При дефиците меди нарушается нормальное развитие соединительных тканей и кровеносных сосудов.
Широкое применение меди и ее соединений в промышленности и сельском хозяйстве повышает риск отравления этими веществами. Отравления обычно связаны со случайной передозировкой инсектицидов, вдыханием порошка металла, заглатыванием растворов солей меди. Большую опасность представляют напитки, хранящиеся в медных сосудах без защитного покрытия стенок.
Токсическое действие соединений меди обусловлено тем, что ионы меди взаимодействуют с тиольными —SН-группами (связывание) и аминогруппами —NH2 (блокирование) белков. При этом могут образовываться биокластеры хелатного типа:
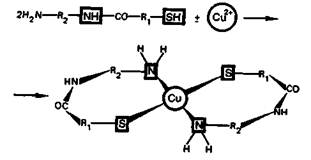 Вследствие таких взаимодействий белки становятся нерастворимыми, теряют ферментативную активность. В результате нарушается нормальная жизнедеятельность.
Вследствие таких взаимодействий белки становятся нерастворимыми, теряют ферментативную активность. В результате нарушается нормальная жизнедеятельность.
В качестве наружного средства применяют 0,25%-ный водный раствор сульфата меди СuSО4 при воспалении слизистых оболочек и конъюнктивитах. Малые дозы этого препарата могут применяться во время приема пищи для усиления эритропоэза при малокровии.
Серебро и золото. В организме взрослого человека обнаруживается около 1 мг серебра, т.е. примерно 10-6% (1 ч. на миллион), и до 10 мг золота, т.е. примерно 10-5% (10 ч. на миллион).
Антисептические свойства растворимых солей серебра известны с древних времен. Священнослужители давно знали, что вода («святая») при хранении в серебряных сосудах долго не портится, т.е. не подвергается микробному загрязнению. В настоящее время это свойство «серебряной» воды используется моряками в дальних плаваниях.
Сильные токсические проявления у взрослого человека наблюдаются при приеме внутрь 7 г АgNO3.
Токсическое действие соединений серебра, как и в случае меди, обусловлено главным образом тем, что ионы серебра взаимодействуют с тиольными серо- и азотсодержащими группами белков, нуклеиновых кислот и других биоорганических веществ.
В водном растворе существуют только комплексные соли золота, например, Nа3[Аu(S2О3)2] и различные тиоловые бионеорганические комплексы.
Механизм токсического действия соединений золота аналогичен механизму токсического действия соединений меди и серебра. В соответствии с общим правилом для тяжелых металлов одной группы токсичность возрастает с увеличением атомного номера в ряду: Сu Аg Аu.
В медицине издавна используются такие препараты, как кристаллический серебро нитрат АgNО3 (ляпис) и его водные растворы. Давно известны также препараты коллоидного металлического серебра протаргол (8% Аg) и колларгол (70% Аg), которые представляют собой мелкодисперсные порошки с металлическим блеском. Каждая частица таких порошков представляет собой кристаллик восстановленного металлического серебра размером менее 1 мкм с белковой оболочкой из альбумина (протаргол) или коллагена (колларгол). Белковая оболочка защищает кристаллики серебра от слипания и обеспечивает их переход в водную среду (солюбилизирует).
Препараты серебра применяют как противовоспалительные, антисептические и вяжущие средства.
В качестве эффективных противовоспалительных средств применяют также препараты золота. Наиболее известны кризанол (от греч. хризос — золото), с 30%-ным содержанием благородного металла, и коллоидное золото. Главный компонент кризанола — комплекс золота с тиоловым органическим соединением Аu—S—СН2СН(ОН)СН2-SО3.
|
Дата добавления: 2014-01-04; Просмотров: 3164; Нарушение авторских прав?; Мы поможем в написании вашей работы!