
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Фосфор. Ортофосфатна кислота
|
|
|
|
Р – світлоносець:
- білий фосфор
- червоний
- чорний
Отримання – електротермічний метод
Сa3(PO4)2+ 3 SiO2 + 5C = 3 CaSiO3 + 2P + 5 CO
Фосфор – активний неметал і він взаємодіє з:
1) металами: 2 Са + 2 Р = Са3Р2
2) неметалами: 4P + 5 O2 = 2 P2O5, 2P + 5S = P2S5, 2P + 3S = P2S3, 2P + 5Cl2 = 2 PCl5
3) кислотами: P + 5 HNO3(k) = H3PO4 + 5 NO2 + H2O
4) лугами: 4P + 3 NaOH + 3 H2O = 3 Na2H2PO2 + PH3
H3PO4 – ортофосфатна кислота – середньої сили електроліт
H3PO4 = H+ + H2PO4-
H2PO4- = H+ +HPO42-
HPO42- = H+ + PO43-
Отримання H3PO4
Екстракційний метод: Сa3(PO4)2+ H2SO4 = 3CaSO4 + H3PO4

 Термічний метод: P P2O5 H3PO4
Термічний метод: P P2O5 H3PO4
Лабораторні методи: PCl5 + 4H2O = H3PO4 + 5 HCl; P + 5HNO3 + 2 H2O = H3PO4 + 5 NO
H3PO4 реагує із:
1) металлами: 3Mg + H3PO4 = Mg3(PO4)2 + 3 H2
2) оксидами: 3 CaO + 2 H3PO4 = Ca3(PO4)2 + 2 H2O
3) гідроксидами: 3 NaOH + H3PO4 = Na3PO4 + 3 H2O
4) аміаком: 3 NH3 + H3PO4 = (NH4)3PO4
Застосування H3PO4
- для підкислення лимонаду
- в зубопротезній техніці
- для отримання фосфорних добрив
- в аналітичній хімії
5. Важливі сполуки р-елементів та їх застосування
| Формула | Назва | Застосування |
| HNO3 | Нітратна кислота | Для одержання барвників, вибухових речовин, добрив |
| NaNO3 | Натрій нітрат | При виробництві скла, у харчовій промисловості |
| KNO3 | Калій нітрат | Як мінеральне добриво, для отримання пороху |
| NH4NO3 | Амоній нітрат | Як добриво |
| H3PO4 | Ортофосфатна к-та | Для отримання добрив |
| Ca3(PO4)2 | Кальцій ортофосфат | Для отримання добрив |
| CaH2PO4 | Кальцій дигідрогенфосфат | Як добриво |
| NH4H2PO4 | Амоній дигідро-генортофосфат | Як добриво |
Питання для самоконтролю
1. Які сполуки нітрогену та фосфору поширені в природі?
2. Наведіть рівняння реакцій одержання вільного азоту із відповідних сполук.
3. Які ангідриди відповідають таким кислотам: HNO3, HNO2, H3PO4, H3PO3, H4P2O7?
4. Виконайте такі перетворення:




 NH3 N2 NO NO2 HNO3 NH4NO3
NH3 N2 NO NO2 HNO3 NH4NO3
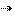
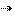
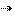
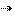 P P2O3 P2O5 Ca3(PO4)2 H3PO4
P P2O3 P2O5 Ca3(PO4)2 H3PO4
5. Закінчить рівняння реакцій та складіть схеми електронного балансу:
NO + KMnO4 =
NO2 + Ca(OH)2 =
Zn + HNO3(k)
CuO + NH3 =
KMnO4 + NH3 =
PH3 + O2 =
Zn+ KNO3 + KOH =
6. Скільки тон HNO3 можна отримати із 17,5 м3 (н.у.) аміаку?
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 1004; Нарушение авторских прав?; Мы поможем в написании вашей работы!