
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Энергия Гиббса как критерий самопроизвольности процесса
|
|
|
|
В химических системах энтропийному фактору ΔS, действующему в направлении разъединения частиц и рассеяния вещества, противостоит энтальпийный фактор ΔH, действующий в направлении объединения частиц, образовании химической связи и межмолекулярного взаимодействия, сведения запаса энергии системы к минимуму.
Разность между энтальпийным и энтропийным факторами:

позволяет судить о возможности самопроизвольного протекания химического процесса в данном направлении. Данное математическое выражение называется объединенный закон термодинамики.
Величину G = Н - TS принято называть энергией Гиббса в честь американского физика Д. У. Гиббса - одного из основоположников современной химической термодинамики. До недавнего времени для величину G было принято называть изобарно-изотермический потенциал, а в медицинской литературе употребляется термин свободная энергия. Если величина 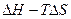 имеет отрицательный знак (
имеет отрицательный знак ( <О), то это неопровержимо доказывает, что данный процесс принципиально осуществим и абсолютное значение разности
<О), то это неопровержимо доказывает, что данный процесс принципиально осуществим и абсолютное значение разности 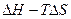 определяет движущую силу этого процесса. Если же
определяет движущую силу этого процесса. Если же  положительна, то в условии, для которых были измерены
положительна, то в условии, для которых были измерены 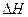 и
и 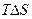 , данная реакция протекать не может. Осуществимой же окажется обратная реакция, для которой
, данная реакция протекать не может. Осуществимой же окажется обратная реакция, для которой  будет иметь отрицательное значение. Если
будет иметь отрицательное значение. Если  =0, то система находится в равновесии.
=0, то система находится в равновесии.
Для определенной химической реакции величину ΔG можно вычислить по формуле:
Δ Gр-ции = ΣпΔG0 прод. - ΣпΔG0 исх.,
где: Δ Gр-ции – энергия Гиббса данной реакции
ΔG0 – стандартная энергия Гиббса веществ, значение которой являются постоянными и приводятся в справочной литературе.
Человеческий организм является открытой термодинамической системой. Основным источником энергии для него является химическая энергия, заключенная в пищевых продуктах, часть которой расходуется на совершение работы внутри организма, связанной с дыханием, кровообращением, нагреванием вдыхаемого воздуха, воды и пищи, и совершением внешней работы, связанной со всеми перемещениями человека и его трудовой деятельностью.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 391; Нарушение авторских прав?; Мы поможем в написании вашей работы!