
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Неидеальные растворы и азеотропные смеси
|
|
|
|
Реальные смеси не подчиняются закону Рауля. А газовая фаза не подчиняется уравнению Менделеева – Клапейрона (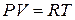 ). В идеальном газе мольная доля равна объемной, так как мольный объем одинаков для всех компонентов (1 моль газа – 22,4 л).
). В идеальном газе мольная доля равна объемной, так как мольный объем одинаков для всех компонентов (1 моль газа – 22,4 л).
Равновесие в некоторых неидеальных смесях может быть описано уравнением:
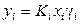 . (5.15)
. (5.15)
Коэффициент активности 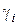 зависит от энергии взаимодействия между молекулами и их размера, т.е. от их объема и поверхности.
зависит от энергии взаимодействия между молекулами и их размера, т.е. от их объема и поверхности. 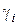 может быть больше или меньше 1 (для идеальных смесей
может быть больше или меньше 1 (для идеальных смесей 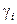 =1). Это называют отрицательным или положительным отклонением от закона Рауля.
=1). Это называют отрицательным или положительным отклонением от закона Рауля.
Однако, неидеальность большинства реальных систем настолько велика, что равновесие в них не может быть описано уравнением (5.15) и другими аналитическими уравнениями. Для таких смесей равновесные данные приводятся в справочниках в виде таблиц зависимости равновесных составов паров и жидкости.
Отклонения от идеальности бывают настолько большими, что получаются азеотропные и расслаивающиеся смеси.
Азеотропная – такая смесь, у которой при некотором составе жидкости равновесный пар имеет такой же состав, то есть в точке азеотропа 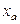 =
= 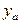 (рисунок 5.5).
(рисунок 5.5).
До точки азеотропа низкокипящий компонент является ЛЛК, при этом 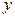 >
>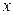 . После точки азеотропа низкокипящий компонент – ТЛК,
. После точки азеотропа низкокипящий компонент – ТЛК, 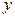 <
<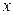 . В точке азеотропа
. В точке азеотропа 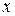 =
= 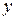 и разделение смеси невозможно ни перегонкой, ни ректификацией.
и разделение смеси невозможно ни перегонкой, ни ректификацией.
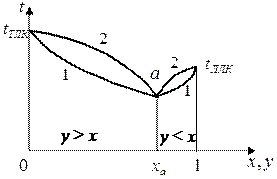 |
Рисунок 5.5 – Диаграмма 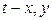 для азеотропной смеси:
для азеотропной смеси:
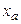 – состав смеси, соответствующий точке азеотропа
– состав смеси, соответствующий точке азеотропа 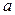 , в которой
, в которой 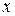 =
= 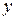 .
.
Диаграмма 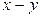
Задаваясь различными температурами из диаграммы 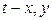 определяют множество значений соответствующих
определяют множество значений соответствующих 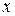 и
и 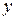 . Наносят точки с координатами (
. Наносят точки с координатами (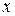 ;
;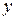 ) на диаграмму
) на диаграмму 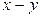 и соединяем их плавной кривой. Полученная кривая 1 – равновесная кривая системы «пар–жидкость»
и соединяем их плавной кривой. Полученная кривая 1 – равновесная кривая системы «пар–жидкость» 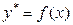 .
.
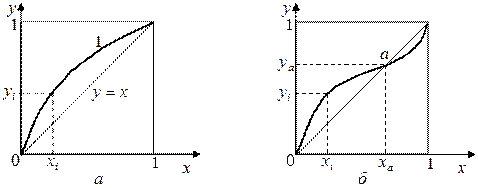 |
Рисунок 5.6 – Диаграмма 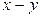 для идеальной смеси (
для идеальной смеси (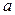 ) и азеотропной смеси (
) и азеотропной смеси (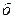 ).
).
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 717; Нарушение авторских прав?; Мы поможем в написании вашей работы!