
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Произведение растворимости
|
|
|
|
Большинство веществ малорастворимо в воде, поэтому очень часто имеют дело с системами, в которых в состоянии равновесия находится осадок и насыщенный раствор электролита. Это равновесие носит динамический характер, вследствие чего скорость процесса растворения должна совпадать со скоростью его кристаллизации. При растворении электролита в воде, например, соли, в раствор переходят не молекулы, а ионы. Поэтому равновесие в насыщенном растворе устанавливается между твердой солью и перешедшими в раствор ионами.
Равновесие в насыщенном растворе электролита АmBn можно представить так:
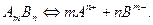
Прямой процесс - это растворение осадка, а обратный процесс – это кристаллизация осадка из насыщенного раствора.
Выражение константы равновесия для этого процесса имеет вид
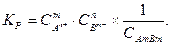
Концентрация твердой соли 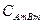 является постоянной величиной и поэтому её можно ввести в константу равновесия Кр. Таким образом, получаем
является постоянной величиной и поэтому её можно ввести в константу равновесия Кр. Таким образом, получаем
Кр =  .
.
В насыщенном растворе электролита произведение концентраций его ионов есть величина постоянная при данной температуре. Данная величина количественно характеризует способность электролита растворяться. Данную величину называют произведением растворимости
ПР =  (13).
(13).
Следует иметь в виду, что произведение растворимости, вычисленное без учета коэффициента активности, является постоянной величиной только для малорастворимых электролитов и при условии, что концентрации других ионов, находящихся в растворе, малы.
Произведение растворимости зависит от природы растворенного вещества и растворителя, а также от температуры и не зависит от активности ионов малорастворимого электролита в растворе.
Произведение растворимости для большинства электролитов рассчитано и содержится в таблицах. Зная произведение растворимости, можно вычислить, выпадает ли в данных условиях вещество в осадок. Условием образования осадка малорастворимого электролита является превышение произведения активностей ионов этого электролита в растворе над табличной величиной произведения растворимости.
|
|
|
Если активность или концентрация одного из ионов малорастворимого электролита увеличится, то равновесие сместится, и, соответственно, активность или концентрация другого иона уменьшится.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 321; Нарушение авторских прав?; Мы поможем в написании вашей работы!