
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Термодинамика. Внутренняя энергия газа
|
|
|
|
Термодинамика – это наука о тепловых явлениях. В противоположность молекулярно-кинетической теории, которая делает выводы на основе представлений о молекулярном строении вещества, термодинамика исходит из наиболее общих закономерностей тепловых процессов и свойств макроскопических систем. Выводы термодинамики опираются на совокупность опытных фактов и не зависят от наших знаний о внутреннем устройстве вещества, хотя в целом ряде случаев термодинамика использует молекулярно-кинетические модели для иллюстрации своих выводов.
Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновесия. Важным свойством термодинамически равновесной системы является выравнивание температуры всех ее частей.
Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное состояние. Такой переход называется термодинамическим процессом. Если процесс протекает достаточно медленно (в пределе бесконечно медленно), то система в каждый момент времени оказывается близкой к равновесному состоянию.
Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении.
Молекулярно-кинетическая теория приводит к следующему выражению для внутренней энергии U идеального одноатомного газа (гелий, неон и др.), молекулы которого совершают только поступательное движение:
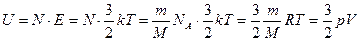 , (8.1)
, (8.1)
где E – средняя кинетическая энергия поступательного движения молекул газа; m – масса газа; M – молярная масса газа; NA – число Авогадро; R – универсальная газовая постоянная; Т – абсолютная температура газа; p – давление газа; V – объем газа.
Таким образом, внутренняя энергия U идеального газа однозначно определяется макроскопическими параметрами p V и Т, характеризующими состояние газа. Она не зависит от того, каким путем было реализовано данное состояние. Принято говорить, что внутренняя энергия является функцией состояния. Внутренняя энергия газа зависит только от массы газа (количества вещества) и температуры газа. Нельзя говорить, что внутренняя энергия зависит от давления и объема газа. Эти параметры газа могут меняться, но внутренняя энергия газа при этом может оставаться постоянной (например, в изотермическом процессе). Изменение внутренней энергии идеального газа, равное
 , (8.2)
, (8.2)
определяется температурами начального и конечного состояния газа и не зависит от процесса.
У реальных газов, жидкостей и твердых тел средняя потенциальная энергия взаимодействия молекул не равна нулю, ее необходимо учитывать при определении полной внутренней энергии тела. Средняя потенциальная энергия взаимодействия молекул газа зависит от среднего расстояния между молекулами, а значит, от объема газа. Следовательно, внутренняя энергия реального газа зависит не только от массы и температуры, но и от объема газа.
|
|
|
|
|
Дата добавления: 2014-01-04; Просмотров: 472; Нарушение авторских прав?; Мы поможем в написании вашей работы!