
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Характеристика основных фаз в сплавах
|
|
|
|
МЕТАЛЛИЧЕСКИЕ СПЛАВЫ И ДИАГРАММЫ СОСТОЯНИЯ
Аморфизация сплавов
При охлаждении жидкого расплава с высокими скоростями (105…107 К/с) зародыши кристаллов образовываться не успевают и в твердом состоянии фиксируется структура, характерная для жидкости. Такие структуры получили название аморфных. В настоящее время аморфные состояния получены как для чистых металлов (Pb, Sn, Al, Ni и др.), так и для многочисленных сплавов. Чистые аморфные металлы получают, как правило, осаждением из парогазовой фазы на холодную подложку. Для получения аморфных сплавов чаще используют методы центробежного разбрызгивания капель, расплющивания на быстровращающемся диске или между валками, лазерного расплавления поверхностных зон. Легче аморфизуются сплавы, в которых содержится высокая концентрация неметаллических элементов (Fe80B20, Fe70Cr10B20, Ni75Si8B17, Co75Si15B10, Pd80Si20 и др.). Если же сплав состоит только из металлических элементов, то легче аморфизуются сплавы, когда входящие в них элементы сильно различаются размерами атомов и их электроотрицательностью (Ni35Nb65, Ni55Ta45, Cu50Zr50, Co60Zr40 и др.). Аморфизация сталей в настоящее время пока затруднена, потому что, как показывают теоретические оценки, для этого нужно реализовать скорости охлаждения порядка 109- 1010 К/с. Чугуны же (например, Fe + 4,5 % С) удалось аморфизировать при скорости охлаждения 108 K / c.
Аморфные материалы - изотропны, обладают очень высокой прочностью, особенно удельной прочностью, высоким сопротивлением коррозии и рядом других свойств.
Уже сейчас аморфные материалы используют в качестве различных термодатчиков, для магнитных головок записи, для упрочнения режущих инструментов. Предполагается, что в ближайшее время их будут использовать в качестве пружинных материалов, антикоррозионных покрытий, в качестве металлокорда в автомобильной промышленности. Применение аморфных материалов подробнее рассмотрено во II части данного курса лекций.
Контрольные вопросы к главе 1
1. Какие тела называют металлами?
2. Какие характеристики описывают кристаллическое строение металлов?
3. Какие типы дефектов кристаллического строения металлов принято считать основными?
4. Каковы причины различий в скоростях диффузии атомов в объеме зерна и по границам?
5. Что такое энергия активации диффузии?
6. Какова размерность коэффициента диффузии?
7. Что такое переохлаждение при кристаллизации и чем оно обусловлено?
8. От каких факторов зависит размер зерна в литом сплаве?
9. Что такое модификаторы?
Глава 2
Чистые металлы применяют довольно редко, так как они обладают низкой прочностью и ограниченным разнообразием свойств.
В технике широкое применение получили металлические сплавы – вещества, полученные сплавлением двух или более компонентов.
Компонентами называют элементарные (металлические или неметаллические) вещества или устойчивые химические соединения, входящие в состав сплава.
В отношении взаимной растворимости компонентов возможны два предельных случая:
1. Компоненты сплава неограниченно растворяются друг в друге, как в жидком, так и в твердом состояниях. При этом в твердом состоянии в кристаллической решетке одного металла (называемого растворителем) собственные атомы замещаются атомами второго компонента, образуется гомогенный (однородный) сплав, называемый твердым раствором. Кристаллическая решетка твердого раствора такая же, как у металла растворителя.
2. Компоненты сплава практически нерастворимы друг в друге в твердом состоянии, т.е. практически не образуют твердых растворов. В этом случае сплав состоит из смеси кристаллов практически чистых компонентов. Такую смесь часто называют механической, но правильнее называть ее гетерогенной смесью кристаллов. Примером могут служить сплавы системы Pb - Cu.
На практике чаще всего проявляются не эти два крайних случая, а промежуточные, когда один компонент частично растворяется в другом, причем в результате взаимодействия компонентов могут образовываться новые фазы или соединения, кристаллическая решетка которых может не совпадать с решетками ни одного из входящих в сплав компонентов, но может и совпадать.
Полная взаимная растворимость может проявляться только при сплавлении элементов с кристаллическими решетками одного и того же типа, причем размеры атомов компонентов не должны отличаться более чем на 15 %. Непрерывный ряд твердых растворов образуется в системах Ni - Cu, Ag - Au, Au - Pt, Mo – V, Mo – W и др. У образующихся твердых растворов кристаллические решетки не отличаются от исходных компонентов только по типу (ОЦК, ГЦК, ГПУ), периоды же решеток в твердом растворе будут непрерывно меняться в зависимости от концентрации того или другого металла.
Но, кроме двух отмеченных выше условий (типа решетки и размеров атомов), для образования ряда непрерывных растворов должно выполнятся еще одно ограничение, обусловленное химическим взаимодействием между компонентами, образующими сплав: это взаимодействие не должно быть велико.
Если взаимодействие слишком велико, то образуется не неограниченный твердый раствор, а химическое соединение. Так, например, алюминий по размеру атомов почти совпадает с медью и золотом, имеет такую же ГЦК решетку, но в системах Au - Al, Cu - Al образуются не непрерывные твердые растворы, а интерметаллические соединения.
Твердые растворы могут быть трех типов: 1) замещения, 2) внедрения, 3) вычитания.
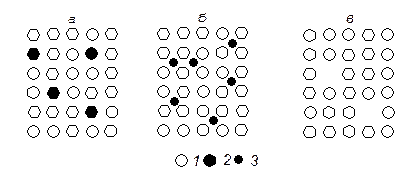
Рис. 16. Схемы расположения атомов в твердых растворах:
а – замещения; б – внедрения; в – вычитания
В случае твердых растворов замещения атомы растворенного вещества статистически случайно занимают узлы решетки растворителя (рис. 16, а).
Твердые растворы внедрения образуются в том случае, когда атомы растворенного вещества внедряются в межузельные промежутки решетки растворителя (рис. 16, б).
Твердые растворы вычитания, являющиеся по существу растворами с дефектной решеткой, образуются лишь при сильном химическом взаимодействии между компонентами. В этих растворах некоторые позиции решетки оказываются незанятыми (рис. 16, в).
Твердые растворы замещения образуются между металлами, а так же между металлами и неметаллами с достаточно большими радиусами атомов.
Твердые растворы внедрения образуются, чаще всего, при растворении таких атомов, как H, C, O, N, B (атомные радиусы которых меньше 0,1 нм) в металлах переходных групп. Примером является твердый раствор углерода в g - Fe (аустенит). Атомы железа в нем расположены в узлах ГЦК решетки, а атомы углерода внедрены в некоторые из межузельных промежутков («поры»).
В ГЦК решетках наиболее удобными местами расположения «посторонних» атомов являются октаэдрические поры (с координатами ½, ½, ½).
При образовании твердых растворов внедрения кристаллическая решетка всегда расширяется, параметры решетки возрастают.
Если исходить только из геометрических размеров атомов, то следовало бы ожидать, что и кислород (атомный радиус которого равен 0,06 нм) при растворении в решетках металлических элементов должен давать металлические твердые растворы. Но это наблюдается, как правило, лишь при малых концентрациях кислорода в растворе. Исключением является твердый раствор кислорода в титане, в котором металлические свойства титана сохраняются и в растворах, содержащих до 30 % кислорода. Обычно при растворении кислорода в металле образуется оксид, не сохраняющий металлических свойств. Причиной этого служит сильная электроотрицательность кислорода, в результате которой, при захвате электронов из «электронного» газа, образуются ионы кислорода. Электроотрицательностью атома называют величину, пропорциональную энергии его связи с дополнительным электроном.
Следует отметить, что чем больше разность электроотрицательностей растворителя и растворяемых элементов, тем в большей степени сохраняется область существования твердого раствора и увеличивается тенденция к образованию интерметаллических соединений и промежуточных фаз.
На взаимную растворимость компонентов оказывает влияние также и валентность входящих элементов. Металлы с более низкой валентностью предпочтительнее растворяют металлы с более высокой валентностью, но не наоборот. Так, Au растворяет 20…30 % (ат) Мg, но магний (валентность 2) растворяет менее 0,2 % (ат) Аu (валентность 1). Если к одному и тому же растворителю добавлять атомы различных компонентов, то их растворимость снижается с ростом валентности растворяемого элемента.
Твердые растворы многокомпонентных веществ могут образовываться так, что-либо атомы всех растворяемых элементов замещают узлы решетки растворителя, либо все внедряются в междоузлия, либо одни элементы размещаются путем замещения узлов растворителя, а другие - путем внедрения. Примером твердых растворов последнего типа является марганцовистая сталь, в которой атомы марганца замещают узлы решетки железа, а атомы углерода внедряются в междоузлия.
Твердые растворы вычитания (в которых не все узлы кристаллической решетки заняты) часто образуются в карбидах (TiC, NbC, MoC и др.). Пустыми в них оказываются некоторые места, которые должны бы быть заняты атомами углерода. В твердых растворах FeO вакантными оказываются узлы, в которых должны располагаться атомы железа.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 881; Нарушение авторских прав?; Мы поможем в написании вашей работы!