
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Закономерности управления химико-технологическими процессами
|
|
|
|
Лекция № 2
Управлять ХТП – это означает, меняя технологические параметры процесса (температуру, давление, состав сырья, катализатор, скорость перемешивания, конструкцию реактора, схему соединению реакторов и т.д.) добиваться максимальной эффективности процесса. Для этого нужно знать функциональную зависимость выбранного критерия эффективности от величины технологических параметров. Изучением этих зависимостей и занимается наука ОХТ.
При изучении общих закономерностей мы используем метод декомпозиции, то есть рассмотрим особенности функционирования отдельных подсистем ХТС. Главной подсистемой ХТС является подсистема химического превращения. В подсистеме химического превращения происходит превращение исходных реагентов в продукты в специальных аппаратах, которые называют реакторами. При этом протекают следующие процессы:
1) химические - разрушение связей и образование новых;
2) массообменные (диффузионные) – движение молекул внутри фаз и через границу раздела фаз;
3) гидродинамические – перемещение потоков внутри реактора;
4) тепловые – теплообмен между отдельными частями реакционной смеси или между реакционной смесью и окружающей средой.
Три последние группы процессов являются физическими, они сопровождают химический процесс, оказывая в той или иной степени влияние на эффективность протекания всего ХТП в целом.
Упрощая задачу, рассмотрим сначала только химические процессы, то есть непосредственно химические реакции, лежащие в основе ХТП, и найдем закономерности управления ими.
В основе ХТП могут лежать разные реакции. Используем метод моделирования и сведем все многообразие химических реакций к нескольким достаточно простым моделям и для каждой модели определим критерий эффективности протекания этой реакции и зависимость этого критерия от технологических параметров.
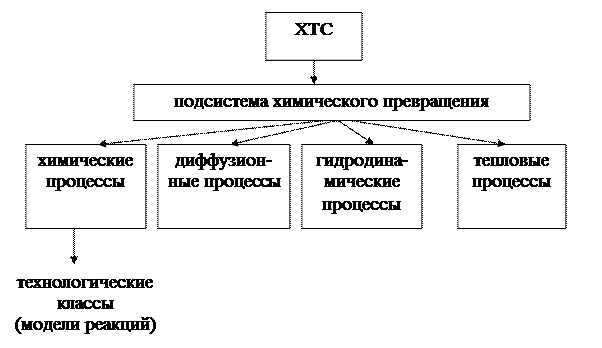
Технологическая классификация химических процессов (модели реакций)
Разработка любой химической технологии начинается с технологической классификации химического процесса, то есть с определения основных признаков, определяющих выбор объектов и инструментов его управления, конструкции реактора и т.д.
Существует ряд признаков, по которым можно классифицировать химические процессы.
1) Процессы могут быть простые и сложные.
Простые процессы описываются одним стехиометрическим уравнением.
А → С или А + В → С + D
В сложных процессах наряду с целевой реакцией протекают побочные реакции, и для описания процесса требуется несколько уравнений.
Сложные процессы могут быть:
- последовательные (консекутивные) А + В → R
R → S
- параллельные А + В → R
А + C → S
- смешанные А + В → R
А + R→ S
2) Процессы могут быть необратимые и обратимые.
Обратимые процессы в отличие от необратимых протекают одновременно в прямом и обратном направлении.
3) Процессы могут быть экзо - и эндотермические, то есть протекать соответственно, с выделением или поглощением тепла. Различают также процессы с большим тепловым эффектом и процессы с малым тепловым эффектом.
4) Процессы могут быть гомогенные и гетерогенные. В первом случае все участники реакции находятся в одной фазе; во втором - одной из стадий процесса является переход через границу раздела фаз.
5) Процессы бывают каталитические и некаталитические.
Совершенно очевидно, что каждая конкретный процесс обладает признаками разных классов. Например, процесс синтеза аммиака
N2 (г) + 3 H2 (г) ↔ NH3 (г), ∆Н < 0
является простым, обратимым, экзотермическим, каталитическим (катализатор – металлическое железо), гомофазным, но гетерогенным, так как газообразные реагенты взаимодействуют между собой на поверхности твердого катализатора.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 680; Нарушение авторских прав?; Мы поможем в написании вашей работы!