
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Активности и коэффициенты активности ионов
|
|
|
|
Термодинамическая теория растворов сильных электролитов
Недостатки теории Аррениуса.
Физические причины, которые приводят к диссоциации электролитов, в теории Аррениуса не рассматриваются. Предполагается, что ионы в растворе ведут себя подобно молекулам идеального газа, т. е. не взаимодействуют друг с другом. Не обсуждался также и вопрос о том, почему заряженные частицы, на которые должны были бы распространяться законы электростатики, не взаимодействуют друг с другом в растворах. Позднее пришлось пересмотреть и некоторые количественные выводы из теории Аррениуса в ее первоначальной форме. Возникла необходимость внести поправки при описании свойств концентрированных растворов слабых электролитов. Вместе с тем, самые основы теории остались неизменными.
Теория Аррениуса наиболее точно выполняется в присутствии избытка постороннего электролита (фона), не принимающего участия в изучаемых ионных равновесиях. Это показывает, что основной причиной неточного выполнения положений теории является взаимодействие ионов друг с другом и с молекулами растворителя.
Для сильных электролитов процесс диссоциации является полным, и закон действующих масс неприменим. Попытки Аррениуса найти следы недиссоциированных молекул в сильных электролитах и использовать свою теорию для описания их свойств оказались безуспешными.
Растворы электролитов содержат ионы – заряженные частицы, которые взаимодействуют как между собой (ион-ионное взаимодействие), так и с молекулами растворителя (сольватация, гидратация). Поэтому в растворах электролитов наблюдаются более значительные отклонения от идеальности, чем в растворах неэлектролитов той же концентрации. Для них необходимо вводить понятия активности и коэффициентов активности.
|
|
|
1. Формальный прием согласования опытных данных с рассчитываемыми - введение вместо концентрации с в соответствующие соотношения для идеальных растворов – активности а = γс, где γ – коэффициент активности.
2. Термодинамическая константа равновесия: вместо K = c+c-/cKA
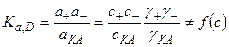
Особенно большие отклонения от свойств идеальных растворов наблюдаются для растворов сильных электролитов вследствие их полной диссоциации на ионы.
Связь активности электролита с активностями ионов
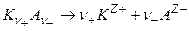
1. В соответствии с принципом электронейтральности 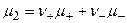
2. Выражения для химического потенциала электролита в целом и отдельных ионов
а) для электролита
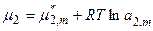 ,
,
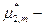 хим. потенциал 2 го компонента в стандартном состоянии (2-м компонентом считается растворенное вещество, 1-й компонент – растворитель).
хим. потенциал 2 го компонента в стандартном состоянии (2-м компонентом считается растворенное вещество, 1-й компонент – растворитель).
Стандартное состояние – некоторое гипотетическое состояние 2 го компонента компонента в одномоляльном растворе, в котором он сохраняет те же свойства, что и в предельно разбавленном растворе.
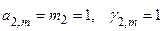 , реально
, реально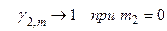
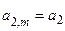 ,
, 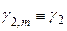 - практический (моляльный) коэффициент активности
- практический (моляльный) коэффициент активности
б) для ионов
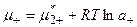
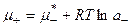
3. Подставляя данные соотношения в уравнение п.1, имеем:
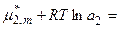
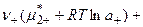
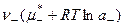
4. Раскрывая скобки, получаем
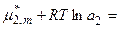
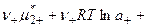
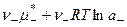
5. В стандартном состоянии
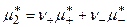
6. Тогда 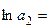
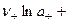
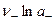 , откуда (после потенцирования):
, откуда (после потенцирования):
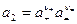
Индивидуальные 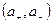 и средние ионные активности
и средние ионные активности 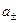
и коэффициенты активностей 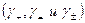 .
.
1. Индивидуальные 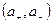 и средние ионные активности
и средние ионные активности 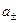 . Связь.
. Связь.
Условно принимают, что: 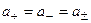
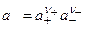
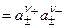
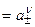 , где
, где 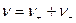
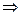
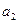 - экспериментально определяемая величина.
- экспериментально определяемая величина.
2. Средняя ионная активность 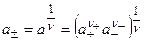
3. Связь активностей, моляльностей и коэффициентов активности
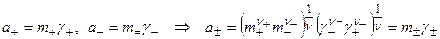 , где
, где 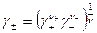
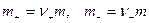
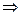
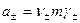 ,
, 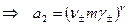 .
.
4. Принцип определения 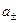 и
и 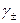 :
: 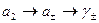 .
.
5. Пример: 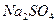 ,
, 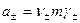
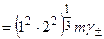 ,
, 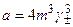
Экспериментальные величины коэффициентов активностей
электролитов. Правило ионной силы.
1. Независимость 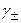 от природы электролита в пределах данного валентного типа в разбавл. растворах
от природы электролита в пределах данного валентного типа в разбавл. растворах
|
|
|
Зависимость 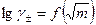 для электролитов типа 1-1
для электролитов типа 1-1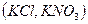 .
.
2. 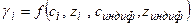 . Суммарное влияние смеси электролитов на коэффициент активности каждого из присутствующих в растворе ионов определяется величиной ионной силы раствора:
. Суммарное влияние смеси электролитов на коэффициент активности каждого из присутствующих в растворе ионов определяется величиной ионной силы раствора: 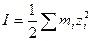 .
.
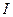 - мера электростатического взаимодействия между всеми ионами раствора
- мера электростатического взаимодействия между всеми ионами раствора
3. Правило «ионной силы» 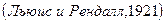 ,
, 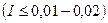 .
.
В разбавленных растворах средний коэффициент активности электролита зависит лишь от величины ионной силы раствора и не зависит от природы других ионов, находящихся в растворе
Теория сильных электролитов Дебая и Хюккеля (1923г.)
1. Задача – теоретический расчет коэффициента активности.
2. Исходные положения: полная диссоциация, отклонения от идеальности связаны с электростатическим взаимодействиями между ионами, последние рассматриваются как взаимодействия между ионом и ионной атмосферой.
3. Реальная ионная атмосфера – статистическое, динамическое образование из ионов, возникающее в р-ре вокруг центрального иона.
а) распределение ионов вокруг центрального иона (силы эл.-ст. взаим-я и тепловое движение).
б) избыточная плотность зарядов противоположного знака,
в) каждый ион является одновременно и центральным ионом и входит в состав ионной атмосферы сферы других ионов.
4. Условная ионная атмосфера - равномерно заряженная сфера определенного радиуса, оказывающая на ц. ион такое же воздействие, что и реальная ионная атмосфера
(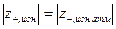 ).
).
5. Уравнение для электрического потенциала ионной атмосферы.
а) Потенциал эл. поля в любой точке пространства вокруг ц. иона:
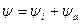 .
.
б) Потенциал ц. иона по законам электростатики:
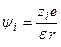 , где
, где 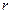 - расстояние от центрального иона
- расстояние от центрального иона
в) Суммарный потенциал внутри условной ионной атмосферы – функция плотности эл. заряда в данной точке.
1) уравнение Пуассона: 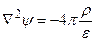 , где
, где 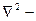 оператор Лапласа,
оператор Лапласа,
2) решение уравнения: 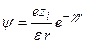 ,
,
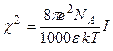
6. Радиус ионной атмосферы.
а) Потенциал ионной атмосферы:
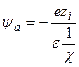
б) Радиус ионной атмосферы:
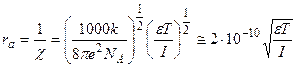
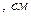
Связь индивидуальных и средних ионных коэффициентов активности с ионной силой раствора.
а) Энергия эл.-ст. взаимодействия ц. иона с ионной атмосферой.
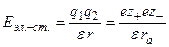 ;
;
на 1 моль: 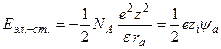
б) 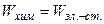
в) Химическая работа как переход из неид. в идеальное состояние
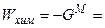
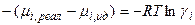
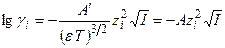
г) Связь 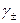 и
и 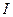 . Предельный закон Дебая-Хюккеля.
. Предельный закон Дебая-Хюккеля.
1) 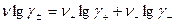 ,
,
2) 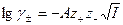 , где
, где 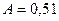 .
.
Сопоставление теории Дебая-Хюккеля с экспериментом.
|
|
|
1. Закон Д.-Х. - теоретическое обоснование правила “ионной силы”.
2. Теоретические и экспериментальные зависимости 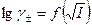 .
.
3. Область применения закона Дебая-Хюккеля 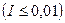 .
.
Причины отклонений от закона Дебая-Хюккеля.
1. Допущения в исходных положениях теории (учет только эл.-ст.
взаимодействий, условная ионная атмосфера, отождествление ионов с точечными зарядами, пренебрежение ион-дипольными вза-
имодействиями)
2. Допущения и упрощения при выводе уравнения (диэлектрическая проницаемость, непрерывность распределения зарядов, разложе-ния в ряд и т.д.).
Закон независимого движения ионов. Подвижности ионов.
1. Сила тока через сечение 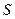 определяется:
определяется: 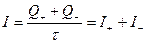
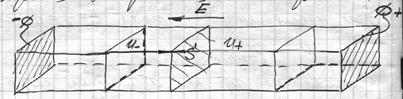 |
2. Схема, поясняющая механизм переноса эл. nока
3. Подсчет тока, переносимого катионами и анионами, 
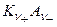
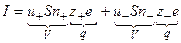
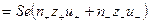 ,
, 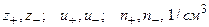
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 3796; Нарушение авторских прав?; Мы поможем в написании вашей работы!