
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Удельная и эквивалентная электропроводности
|
|
|
|
ЭЛЕКТРОПРОВОДНОСТЬ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
Электропроводность растворов электролитов, т.е. способность их проводить электрический ток, зависит от природы электролита и растворителя, концентрации, температуры и некоторых других факторов. Различают удельную и эквивалентную электропроводности. Удельная электропроводность раствора электролита æ (каппа) - это электропроводность столбика раствора длиной 1 см и сечением 1 см. Таким образом, удельная электропроводность представляет собой величину, обратную удельному сопротивлению.
æ = 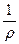 .
.
Удельное сопротивление определяется по уравнению
R = r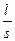 ;
;
æ = 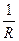
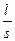 =
= 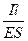 ,
,
где R -общее сопротивление проводника, ом;
S -поперечное сечение проводника, см2;
l -длина прoводника, см.
Размерность – ом-1 см-1 = См/м.
Повышение температуры на 1° увеличивает удельную электропроводность примерно на 2-2,5%. Это объясняется понижением вязкости раствора и уменьшением гидратации ионов, а для растворов слабых электролитов увеличением их степени диссоциации.
При изучении электропроводности растворов целесообразно пользоваться эквивалентной электропроводностью l, которая равна проводимости раствора, содержащего один грамм-эквивалент растворенного электролита, помещенного между электродами, отстоящими друг от друга на 1 см. Для слабых электролитов изменение эквивалентной электропроводности от концентрации раствора связано в основном со степенью диссоциации и для сильных электролитов - межионным взаимодействием.
Удельная и эквивалентная электропроводности связаны между собой соотношением
l = Vэæ;
Vэ = 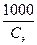 ;
;
l = 1000 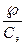 ,
,
где Vэ - число миллилитров раствора, содержащих 1 г-экв электролита;
С э - концентрация электролита в растворе, г-экв/л.
Размерность - ом-1 см2 г-экв-1
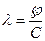 .
.
Размерность - См м2 кг-экв-1.
Кроме эквивалентной электропроводности в электрохимии используется иногда также мольная электропроводность, когда раствор содержит 1 моль растворенного вещества.
Эквивалентная электропроводность с уменьшением концентрации раствора увеличивается и при С® 0 стремится к некоторому максимальному значению l¥ которое называется эквивалентной электропроводностью при предельном разбавлении.
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 4325; Нарушение авторских прав?; Мы поможем в написании вашей работы!