
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Величина рН может служить критерием силы кислоты или основания
|
|
|
|
В ряду кислот более сильной будет та, у которой при одинаковой молярной концентрации активность ионов водорода выше (рН ниже).
Для оснований подобная зависимость имеет обратный характер.
Водородный показатель играет важную роль в жизнедеятельности организма, так в норме рН сыворотки крови равен 7,40 + 0,05, слез -7,4 ± 0,1, слюны - 6,35 - 6,85, желудочного сока - 0,9 - 1,1 Отклонение рН от нормальных значений приводит к расстройству жизнедеятельности организма.
Существенное влияние на урожайность оказывает рН почвы, на экологию водоема - рН воды.
Пример 1:
Определить концентрацию [OH-] в растворе, если рН = 2, при t=250С
pH = - lg [H+]; [H+]= 10-2
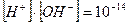
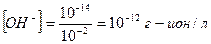
Пример 2. Определите концентрацию ионов ОН- в 0,01 М NH4OH. Рассчитайте рН этого раствора при 295 К.
Решение. Гидроксид аммония - слабый электролит и диссоциирует обратимо:
NH4OH =NH4+ + ОН-.
В соответствии с законом Оствальда константа диссоциации Кравна
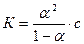 ; К= 1,8 10 -5 (табличное значение)
; К= 1,8 10 -5 (табличное значение)
Подставляя значение К, получаем:
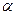 =4,24 10 -2
=4,24 10 -2
Равновесная концентрация ионов ОН- равна
[ОН -] = 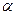 с = 4,24 · 10 -2 · 10 -2 = 4,24 · 10 - 4 г-ион/л.
с = 4,24 · 10 -2 · 10 -2 = 4,24 · 10 - 4 г-ион/л.
Можно считать, что в растворе слабого электролита активность ионов равна их концентрации, тогда:
р [ОН-] = -lg [ОН-] = -lg 4,24 · 10 -4 = 3,37.
Соответственно рН = 14 - 3,37 = 10,63.
Пример 3. Рассчитайте рН раствора, содержащего 0,01 моль/л НС1 и 0,01 моль/л СаС12.
Решение. Так как НСl и СаСl2 сильные электролиты, они диссоциируют полностью:
НС1 = Н+ + С1- , СаС12 = Са2+ + 2С1-
Соответственно рН раствора определяем по формуле
pH = -lg а=-lg f [H+].
Для расчета коэффициента активности необходимо определить ионную силу раствора:
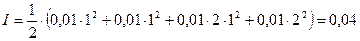
На основании табличных данных при ионной силе раствора I= 0,04 f = 0,86, следовательно:
рН = -lg (0,86 · 0,01) = 2,07.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 731; Нарушение авторских прав?; Мы поможем в написании вашей работы!