
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Зависимость линейной скорости горения от физико-химических факторов
|
|
|
|
Уравнение (15) показывает, что нормальная скорость распространения пламени зависит от теплофизических свойств газопаровоздушной смеси. Но в еще большей степени скорость распространения зависит от ее физико-химических свойств - скорости и температуры реакции горения.
Из уравнения видно, что:
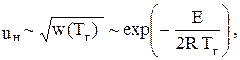 (19)
(19)
т.е. uн пропорциональна скорости реакции окисления и обратно пропорциональна температуре горения.
Определяющим параметром здесь, безусловно, будет скорость реакции.
Запишем уравнение скорости химической реакции горения:
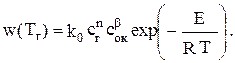 . (20)
. (20)
Рассмотрим, как будет меняться скорость реакций окисления для смесей с разным соотношением горючего и воздуха (рис.2).
Из графика видно, что для смеси стехиометрического состава коэффициент избытка воздуха a = 1, скорость реакции окисления максимальна:
w(Tг) = wстех (21).
При увеличении содержат концентрации горючего в смеси, когда a становится <1, воздух находится в недостатке, и горючее сгорает не полностью, а частично. Поэтому меньше выделится теплоты Qгор, а значит Tг снизится.

Рис.2. Зависимость скорости горения от концентрации
горючего в смеси
Скорость реакций окисления по сравнению со стехиометрической уменьшится, причем из-за снижения сразу и концентрации окислителя О2, и температуры горения. То есть при последовательном снижении a (что эквивалентно увеличению концентрации Сгор в смеси) скорость реакций окисления w(Tг) будет последовательно снижаться. На графике представленном на рис.2 при Cгор > Сгстех кривая становится нисходящей. Значит при a >1 скорость реакций окисления также снижается, и в целом на графике получается парабола.
Именно такая зависимость скорости реакции горения от концентрации горючего компонента в исходной смеси предопределяет параболический вид зависимости многих параметров процесса горения от состава смеси:
· температуры самовоспламенения и минимальной энергии зажигания, рассмотренных ранее;
· концентрационных пределов распространения пламени.
Вид параболы имеет также и зависимость uн от Сг (рис.3).

Рис.3. Зависимость uн от концентрации пропана в воздухе
Согласно теории uнмах должна соответствовать стехиометрической концентрации. Однако экспериментальные ее значения несколько сдвинуты в сторону богатых смесей (a<1).
Таким образом с учетом вышеизложенного КПР связаны с критической скоростью распространения пламени, которая, в свою очередь, зависит от скорости реакции, температуры горения и т.д.
Следовательно, КПР зависят от:
· химических,
· теплофизических свойств,
· параметров состояния горючего вещества и окислителя.
Основными параметрами состояния горючего и окислителя являются:
|
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 880; Нарушение авторских прав?; Мы поможем в написании вашей работы!