
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Причины разрушения оксидных пленок в процессе их роста
|
|
|
|

- образование пузырей (прочность пленки на разрыв великаЖ адгезия к поверхности металла мала)
Адгезия (прилипание) -две фазы сцепляются.
Когезия -сцепление внутри одной фазы
- при недостаточной прочности пленок появляются пузырьки, что делает пленку газопроницаемой (незашищенной), а под пузырем образуется новая оксидная пленка.
- возникновение газонепроницаемых микропузырей, которые препятствуют диффузии ионов металла и тормозят процесс окисления, контролируемыйэтой диффузией, что может привести от параболического закона роста пленки к степеному или логарифмическому.
- отслаивание пленки на поверхности металла
- растрескивание при сдвиге (характерно для пленок, обладающих большой адгезией к металлам и малой прочностью).
- Растрескивание на узлах и крутых изгибах поверхности приводит к интенсивному окислению острых выступов и служит началом началом разрушения оксидных пленок отслаиванием
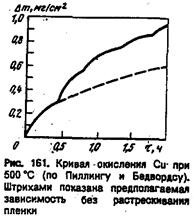 При окислении металла переменной валентности (Fe, Co) в условиях, допускаюших образование нескольких различных окислов, пленки могут иметь многослойную структуру.
При окислении металла переменной валентности (Fe, Co) в условиях, допускаюших образование нескольких различных окислов, пленки могут иметь многослойную структуру.
7. Ионно-электронный механизм окисления Ме (т. Вагнера)

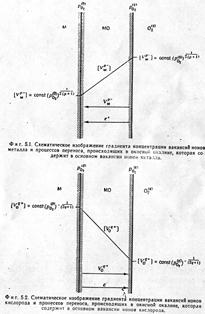
Ионно электронный механизм окисления Ме (т. Вагнера)
Скорость окисления Ме определяеца скоростью диффузии Ме и окисления. Диффузия Ме (катионов Ме) и кислорода (анионов) в слое твердого защитного окисла может осуществляеца по 1 из 2 возможных механизмов
- движение ионов в междоузлиях пространственной кристалической решетки
- движение ионов по пустым узлам решетки
Схема механизма в защитных окислах
Эти механизмы имеют место при росте защитных пленок 1 –для ZnO,CdO,BeO,Al2O3 Образование пленок с катионными(2) или анионными(3) узлами
Диффузия катионов в защитной пленке для соблюдения эл. нейтральности сопр-ся одновременным перемещением в том же напр. эквивалентного числа ê в междоузлиях (при 1) и по дыркам (при 2)
Объемная диффузия, т.е. диффузия через решеку реагирующих ионов или соотв. точ. дефектов, либо перенос ê через растущую окисную пленку опред. скорость всей реакции
Т.к. контролирующим фактором являеца диффузия, считается, что реакция на границе фаз протекает быстро и устанавливаеца термодин. Равновесие между окислом и газообразным О2 на пов-ти раздела МеО/О и междк Ме и окислом на фазовой границе Ме/МеО.
Движущей силой реации явл. Измерение свободной энергии, связанное с образованием в окисной пленке grad концентрации компонентов.
На границе МеО/О2 парц. давление О2 равно давлению О2 в газовой фазе, а на границе Ме/МеО оно равно равновесному давлению диссоциации окисла (упругости диссоциации в контакте с Ме).
На границе Ме/МеО концентр. катионов макс. и они диффундируют наружу к границе МеО/О2. На границе МеО/О2 продиффундировавшие через слой окисла катионы очень быстро реагируют с О2. Диффузия в данном случае являеца ограничивающим фактором.
В связи с недостатком катионов при образовании решетки окисла в ней образуюца катионные V. На границе Ме/МеО концентрация анионов мала и при образование окисла обр-ся анионные вакансии.
Итак, концентрация анионов О2 и кислородных V max-на на границе Ме/О2 и min-ма на границе Ме/МеО, т.к. давление О2 (газ) больше упругости диссоциации. На границе МеО/О2 непрерывно образуются V ионов Ме
Концентрация катионов и анионых вакансий max на грание Ме/МеО и min на границе МеО/О2
Из за grad C от границы Ме/МеО к границе МеО/О2 идет диффузия катионов и анонных V. А от границы МеО/О2 к гр. Ме/МеО - диффузия анионов О2 и катионны V. Электроны за счет тоннельного эффекта мигрируют от гр. Ме/МеО к гр. МеО/О2. Скорость роста пленки опр-ся grad и скоростями диффузии компонентов. Такой механизм приводит к окислению по параболич. закону. Подвижности к коэф. диффузии катионов, анионов и их V и ês не одинаковы. Это приводит к разделению зарядов в растуще окисной пленке.
Результирующий простр заряд создает в окисной пленке эл. поле, противодействующиее дальнейшему разделению зарядов. Этимдостигается стац. сост., при котором через окалину никакого раз-го тока не течет.
 Перемещение ионов, ês и V через окисную пленку объясняеца
Перемещение ионов, ês и V через окисную пленку объясняеца
- диффузией, обусл. эл. потенциалом
- миграцией, обусл. эл. потенциалом, т.е. ионной и ê-ой проводимостью окисла.
Т Вагнера для относительно толстых слоев относится к пленкам толщиной > 1мкм. Она предполагает установление grad концентрации в окисле кот. явл. решающим фактором, контролирующим скорость роста. В этом случае получаем параболический з-н окисления.
|
|
|
|
Дата добавления: 2014-01-05; Просмотров: 1546; Нарушение авторских прав?; Мы поможем в написании вашей работы!