
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Количественный структурно-фазовый анализ сплава
|
|
|
|
Пользуясь диаграммой состояния можно для любого сплава при любой температуре определить не только число фаз, но и их состав и количественное соотношение. Для этого используется правило отрезков.
Для проведения количественного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы ограничивающими данную двухфазную область (ликвидус, солидус или оси компонентов).
Правило отрезков может быть использовано только для тех областей диаграммы, в которых сплавы находятся в двухфазном состоянии.
Первое положение правила отрезков — определение состава фаз.
Необходимо определить состав фаз для сплава в точке m:
Через точку m проводим горизонтальную линию (коноду) до пересечения с ближайшими линиями диаграммы - это линии ликвидус и солидус.
Точки пересечения с и d проецируют на ось концентраций.
Проекция точки с – точка с ' покажет состав твердой β-фазы (твердая фаза содержит ≈11%В и 89%А).
Проекция точки d – точка d ' покажет состав жидкой фазы (жидкая фаза содержит ≈ 44%В и 56%А).
Состав жидкой фазы изменяется по линии ликвидуса, а состав твердой фазы – по линии солидуса.
С понижением температуры состав фаз изменяется в сторону увеличения содержания компонента В.
Пользуясь вторым положением правила отрезков, можно определить количественное соотношение фаз также для любой температуры
Необходимо определить количественное соотношения жидкой и твердой фазы при заданной температуре (в точке m):
Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды.
Количество всего сплава (Qсп) определяется отрезком cd.
Если принять, что отрезок cd выражает количество (Qсп) всего сплава, то
- количеству выделившихся кристаллов β- твердого раствора (Qтв) соответствует отрезок md,
- количеству жидкой фазы (Qж) - отрезок cm.
Для определения относительного количества фаз пользуются отношениями:
- относительное количество твердой фазы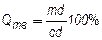 ;
;
- относительное количество жидкой фазы 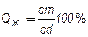 .
.
Лекция 5. Диаграммы состояния двухкомпонентных сплавов
5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (сплавы твердые растворы с неограниченной растворимостью)
Полная взаимная растворимость металлов в твердом состоянии возможна лишь для изоморфных металлов. При их сплавлении образуется непрерывный ряд твердых растворов замещения (Cu-Ni).
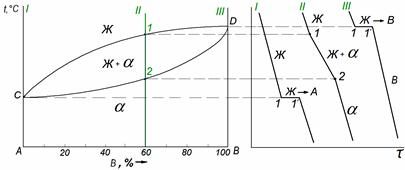
Рис.5.1 Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (а); кривые охлаждения типичных сплавов (б)
Анализ диаграммы
1. Количество компонентов: К = 2 (компоненты А и В).
2. Число фаз: Ф = 2 (жидкая фаза Ж, кристаллы твердого раствора α)
3. Основные линии диаграммы:
· C1D – линия ликвидус, выше этой линии сплавы находятся в жидком состоянии;
· C2D – линия солидус, ниже этой линии сплавы находятся в твердом состоянии.
4. Характерные сплавы системы:
а) Чистые компоненты А и В кристаллизуются при постоянной температуре (кривые охлаждения сплавов I и II).
Кривая I (рис. 53) получена при охлаждении компонента А. Выше температуры 1 металл находится в жидком состоянии. Кристаллизация начинается при температуре в точке 1 и заканчивается через какое-то определенное время, зависящее от количества металла в тигле, в точке 1'.
Согласно правилу фаз С = К - Ф + 1 имеем: компонент 1 (металл А) фазы 2 (жидкий металл и образующиеся кристаллы А), следовательно, С = 1-2+1=0, т. е. кристаллизация должна происходить при постоянной температуре. Ниже температуры 1ʹ происходит только охлаждение кристаллов компонента А. Аналогично происходит охлаждение и кристаллизация компонента В (сплав III).
б) Остальные сплавы кристаллизуются аналогично сплаву II.
Процесс кристаллизации сплава I:
- При температурах выше т. 1 сплав находится в состоянии однородного жидкого раствора.
- При температуре, соответствующей т. 1, жидкий раствор становится насыщенным по отношению к α -фазе, начинают образовываться центры кристаллизации твердого раствора α. На кривой охлаждения отмечается перегиб (критическая точка 1), связанный с уменьшением скорости охлаждения затвердевающего сплава вследствие выделения скрытой теплоты кристаллизации.
- В интервале температур т.1–2 продолжается процесс кристаллизации, протекающий при понижающейся температуре. Согласно правилу фаз число степеней свободы С = 2-2+1=1 т.к. К=2, Ф=2 (жидкая и кристаллы твердого раствора α), поэтому кристаллизация сплавов должна происходить в интервале температур.
- При достижении температуры соответствующей т. 2, кристаллизация заканчивается и ниже этой температуры охлаждается насыщенный твердый раствор α без каких-либо превращений.
- При дальнейшем понижении температуры охлаждается сплав в твердом состоянии, состоящий из однородных кристаллов твердого раствора α.
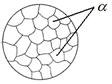 Рис. 5.2. Схема микроструктуры сплава – однородного α -твердого раствора
Рис. 5.2. Схема микроструктуры сплава – однородного α -твердого раствора
5.2 Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (механические смеси)
Сплавы таких компонентов при переходе из жидкого состояния в твердое образуют механическую смесь зерен чистых металлов. К числу таких систем относятся Рb - Sb и немногие другие.
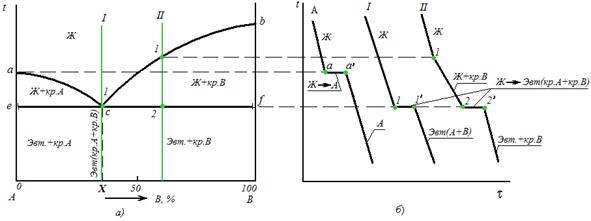
Рис. 5.3. Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (а) и кривые охлаждения сплавов (б)
Анализ диаграммы состояния.
1. Количество компонентов: К = 2 (компоненты А и В);
2. Число фаз: Ф = 3 (кристаллы компонента А, кристаллы компонента В, жидкая фаза).
3. Основные линии диаграммы:
· линия ликвидус acb, состоит из двух ветвей, сходящихся в одной точке;
· линия солидус ecf, параллельна оси концентраций стремится к осям компонентов, но не достигает их;
4. Типовые сплавы системы:
- сплав, состоящий из чистого компонента А;
- сплав, состоящий из чистого компонента В;
- эвтектический сплав – сплав, соответствующий концентрации компонентов в точке с (сплав I).
Эвтектика – механическая смесь двух (или более) разнородных кристаллов, одновременно кристаллизующихся из жидкости при постоянной, самой низкой для рассматриваемой системы, температуре (от греческого эв-тэо — легкоплавящаяся).
При образовании сплавов механических смесей эвтектика состоит из кристаллов комп. А и В:
Эвт. = кр. А + кр. В
- доэвтектические сплавы - сплавы, лежащие левее сплава I (содержащие менее Х% компонента В);
- заэвтектические сплавы (например, сплав II) - лежащие правее сплава I (содержащие более Х% компонента В).
5. Кристаллизация типовых сплавов системы.
а) Чистые компоненты, кристаллизуются при постоянной температуре - участок а-а' на кривой охлаждения компонента А (рис 5.3, б).
б) Кривая охлаждения эвтектического сплава I, аналогична кривым охлаждения чистых металлов.
Процесс кристаллизации сплава эвтектического состава (сплав I):
- до точки 1 охлаждается сплав в жидком состоянии.
- при температуре, соответствующей точке 1, начинается одновременная кристаллизация двух разнородных компонентов (кр.А и кр.В). На кривой охлаждения отмечается температурная остановка, т.е. процесс идет при постоянной температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии трех фаз (жидкой и кристаллов компонентов А и В) число степеней свободы будет равно нулю (С = 2 – 3 + 1 = 0).
- в т. 1' процесс кристаллизации завершается. Ниже точки 1' охлаждается сплав, состоящий из дисперсных разнородных кристаллов компонентов А и В.
в) Процесс кристаллизации заэвтектического сплава II ( рис 5.3,б):
- до точки 1 охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1, начинают образовываться центры кристаллизации избыточного компонента В. На кривой охлаждения отмечается перегиб (критическая точка 1), связанный с уменьшением скорости охлаждения вследствие выделения скрытой теплоты кристаллизации.
- на участке 1–2 идет процесс кристаллизации компонента В, протекающий при понижающейся температуре, так как согласно правилу фаз в двухкомпонентной системе при наличии двух фаз (жидкой и кристаллов компонента В) число степеней свободы будет равно единице (С = 2 – 2 + 1 = 1). При охлаждении состав жидкой фазы изменяется по линии ликвидус до эвтектического.
- на участке 2–2’ кристаллизуется эвтектика Ж→Эвт. (кр. А + кр. В).
Ниже точки 2’ охлаждается сплав, состоящий из кристаллов первоначально закристаллизовавшегося избыточного компонента В и эвтектики.

Рис. 5.4. Схема микроструктур сплавов: а – доэвтектического, б – эвтектического, в – заэвтектического
При проведении количественного структурно-фазового анализа, конода, проведенная через заданную точку, пересекает линию ликвидус и оси компонентов, поэтому состав жидкой фазы меняется по линии ликвидус, а состав твердой фазы - 100% компонента А (для доэвтектических сплавов), или 100% компонента В (для заэвтектических сплавов).
5.3 Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии
В зависимости от взаимодействия указанных трех фаз возможны два вида диаграмм: диаграмма с эвтектикой и диаграмма с перитектикой.
Диаграмма состояния с эвтектикой (рис. 5.5).
1. Количество компонентов: К = 2 (компоненты А и В);
2. Число фаз: Ф = 3 (жидкая фаза Ж, α и β фазы, где α - твердый раствор атомов компонента В в кристаллической решетке компонента А, а β - твердый раствор атомов компонента А в кристаллической решетке компонента В.
3. Основные линии диаграммы:
- линия ликвидус ЕСР, состоит из двух ветвей, сходящихся в одной точке С;
- линия солидус ЕDСКF, состоит из трех участков;
- DМ – линия предельной растворимости компонента В в компоненте А;
- КH – линия предельной растворимости компонента А в компоненте В.
4. Типовые сплавы системы.
Кристаллизация сплава I. Выше точки 1 сплав находится в жидком состоянии. В точке 1 начинается, а в точке 2 заканчивается кристаллизация сплава, образуются кристаллы твердого раствора α. Состав жидкой фазы изменяется по линии ликвидуса (1 - h), состав α -фазы по линии солидуса (n - 2). При дальнейшем понижении температуры никаких фазовых превращений в этом сплаве не происходит.
Охлаждение сплава II. При температуре 1 начинается кристаллизация твердого раствора β, которая заканчивается по достижении температуры, соответствующей горизонтали DСК (точка 2) эвтектической реакцией Жc ↔ (α + β). После окончательного охлаждения структура сплава состоит из избыточных кристаллов β и эвтектики (α+β).

Рис.5.5. Диаграмма состояния сплавов с ограниченной взаимной растворимостью компонентов в твердом состоянии с эвтектикой
Кристаллизация сплаваIII аналогична кристаллизации сплава I, но заканчивается образованием кристаллов твердого раствора β.
Сплав с концентрацией компонентов, соответствующей точке с, является эвтектическим сплавом. Сплав состоит из мелкодисперсных кристаллов твердых растворов α и β, образующих эвтектику (кр. тв. р-ра α + кр. тв. р-ра β). Кристаллы компонентов в чистом виде ни в одном из сплавов не присутствуют.
Диаграмма состояния с перитектикой - разновидность диаграммы состояния с ограниченной растворимостью компонентов в твердом состоянии (рис. 5.6).
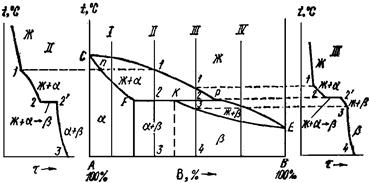
Рис.5.6. Диаграмма состояния сплавов с ограниченной взаимной растворимостью компонентов в твердом состоянии с перитектикой
Линия СРЕ — линия ликвидуса, линия СFКЕ— солидуса. Кристаллизация сплавов I и IV происходит аналогично ранее разобранным. Иначе происходит кристаллизация сплавов, по составу расположенных между точками F и Р.
При кристаллизации сплава с концентрацией компонентов, соответствующей точке К, из жидкости выпадают и растут кристаллы α -твердого раствора. В точке К произойдет перитектическое (перитектос (греч.) — структура окружения) превращение: кристаллы α-твердого раствора взаимодействуют с жидкостью, образуя новую фазу — твердый раствор β: ЖР+ αF ↔ βК. При этом С = 2 - 3 + 1 = 0, т. е. реакция идет при постоянной температуре.
В сплавах, расположенных левее точки К, например в сплаве II, в точке 2 также происходит перитектическое превращение, приводящее к образованию твердого раствора β располагающегося по границам зерен α-фазы. После окончания кристаллизации структурой сплава будут зерна α-фазы, окруженные β-фазой.
В сплавах, расположенных правее точки К, например в сплаве III, количество выделившейся α-фазы невелико, она вся будет израсходована на перитектическое превращение. При дальнейшем понижении температуры от точки 2 до точки 3 будут образовываться и расти зерна β-твердого раствора. Затвердевший сплав имеет структуру, состоящую из зерен твердого раствора β.
5.4 Диаграмма состояния сплавов, компоненты которых образуют химические соединения
При сплавлении компонентов, имеющих большое различие в размерах атомов, кристаллическом строении и свойствах, возможно образование химических соединений АnВm. Химическое соединение такого вида может быть устойчивым и неустойчивым.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 4341; Нарушение авторских прав?; Мы поможем в написании вашей работы!