
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Расчет равновесного состава химического равновесия
|
|
|
|
Результаты вычислений
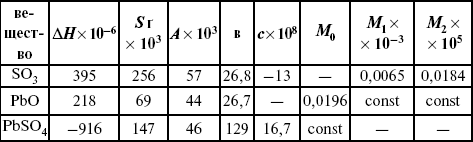
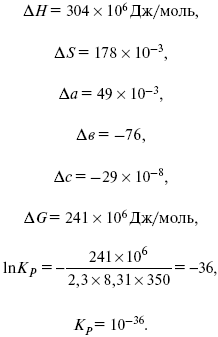
Равновесный состав можно рассчитать только для газовой системы
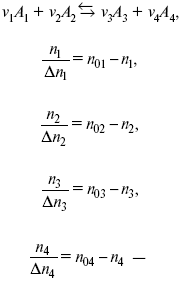
равновесная концентрация.
Исходная концентрация всех компонентов

Изменение каждого компонента по числу молей (или стехиометрическому коэффициенту):

ξγ – (пробег реакции) – химическая переменная.
Она показывает изменение количества вещества по числу молей. Если реакция не началась, то ξγ = 0. Если количество исходных веществ превратилось в такое же количество продуктов реакции, то ξγ = 1.
3H2 + N2 = 2NH3; ξγ= 1,
1,5H2 + 0,5N2 = NH3; ξγ= 0,5,
v 1 А 1 + v 2 А 2 = v 3 А 3+ v 4 А 4, – газовая реакция.
Рассчитать равновесный состав по третьему компоненту при условии, что А = а моль/л; В = в моль/л.
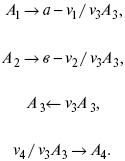
Рассчитываем по 4 компоненту:
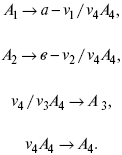
Задача.
Газообразные вещества реагируют по уравнению:

Общее давление в газовой смеси – Р общ, общий объем – V об. Рассчитать KP и Kс.
Найти парциальное давление каждого компонента.
Вещества А и В превращаются в С в количестве Х. Исходные вещества А= 2 моль, В= 1 моль.
Для того, чтобы найти парциальное давление, мы должны Р об умножить на мольную долю. Мольная доля определяется отношением числа молей каждого компонента, отнесенного к общему числу молей всех компонентов.

где En – общее число молей, участвующих в этой газовой смеси.
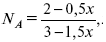
где NA – мольная доля А.
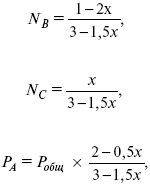
где РА – парциальное давление.

Расчет Kc:
Δ v = l – 0,5 – 2 = – 1,5,
где Δ v – изменение количества молей.

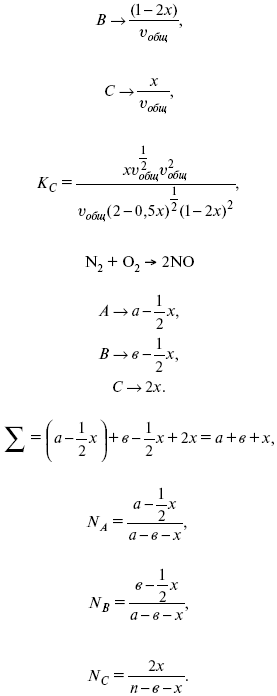
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 624; Нарушение авторских прав?; Мы поможем в написании вашей работы!