
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Ионная связь. Ионные кристаллы
|
|
|
|
Связь называется ионной, если она осуществляется путем электростатического взаимодействия разноименно заряженных ионов, образовавшихся при смещении электронов от одного атома к другому.
Ее можно рассматривать как предельный случай ковалентной полярной связи. Ионная связь может возникать только в том случае, если различия в электроотрицательности взаимодействующих атомов достаточно велики.
Если разность относительных электроотрицательностей взаимодействующих атомов Dх равна 0, то образуется ковалентная неполярная связь; если 0<Dх<2 - ковалентная полярная; если Dх > 2– ионная связь.
Поскольку электростатическое поле иона имеет сферическую симметрию, то ионная связь не обладает направленностью.
Взаимодействие двух заряженных ионов не приводит к полной компенсации их полей, поэтому ионная связь не обладает насыщаемостью.
Для ионной связи эффективные заряды атомов»1. Химическая связь не может быть на 100% ионной. Долю ионного характера связи называют степенью ионности, которая количественно характеризуется эффективными зарядами атомов в молекуле.
Таким образом, природа химической связи едина, и существующее различие между видами связи имеет количественный характер.
Кристаллические решетки кристаллов этого типа состоят из чередующихся положительно и отрицательно заряженных ионов, между которыми действуют электростатические силы притяжения.
Ионные кристаллы образуются при взаимодействии атомов, имеющих большую разность электроотрицательностей. Примерами ионных кристаллов являются галогениды щелочных (NaСl, KF) или щслочно-земельных (СаF2) металлов. В состав ионных кристаллов могут входить и сложные ионы:  .
.
|
|
|
Энергия кристаллической решетки достигает высоких значений (для NaСl: 770 кДж/моль); это, в свою очередь, обусловливает следующий набор физических свойств: высокую твердость, хрупкость. высокие температуры плавления и кипения, высокие теплоты плавления. Подобные свойства определены не только значительной энергией кристаллической решетки, но и структурой каркаса ионного кристалла.
Многие ионные кристаллы относят к классу диэлектриков; при комнатной температуре их электропроводность на 20 порядков ниже, чем электропроводность металлов. С увеличением температуры электропроводность ионных кристаллов возрастает.
Во многих ионных кристаллах наряду с электростатическим притяжением действуют ковалентные связи, а также силы Ван-дер-Ваальса, причем присутствие ковалентной связи вызывает определенные отклонения в физико-химических свойствах кристаллов этого типа, которые не объясняются электростатической моделью.
Наименьшее влияние ковалентности наблюдается для кристаллов галогенидов щелочных металлов.
Так как ионная связь не имеет направленного характера, а многим ионам можно приписать сферическую форму, то структура большинства ионных кристаллов тождественна структурам плотнейшей упаковки.
Вещества ионной природы с многоатомными ионами также образуют ионные кристаллы. Это наблюдается даже для таких ионов,
как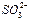 , которые имеют тригональную симметрию.
, которые имеют тригональную симметрию.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 394; Нарушение авторских прав?; Мы поможем в написании вашей работы!