
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кондуктометрическое титрование
|
|
|
|
Кондуктометрическое титрование - метод определения концентрации вещества, основанный на изменении удельной проводимости раствора при титровании. Изменение k связано с изменением концентраций ионов с различной подвижностью, происходящим при химических реакциях в титруемом растворе. Кондуктометрическое титрование можно проводить в окрашенных или мутных растворах. При нём не следует опасаться перетитровать раствор, более того, для нахождения точки эквивалентности это даже необходимо. Кривые титрования, представляющие собой зависимость k от объёма V титранта, добавляемого к исследуемому раствору, имеют излом в точке эквивалентности, причём форма кривых зависит от природы титранта и титруемого вещества.
При кондуктометрическом титровании наиболее широко используются реакции кислотно-основного взаимодействия. При этом возможны следующие типичные случаи.
1) Титрование раствора сильной кислоты раствором сильного основания. Кривая титрования имеет вид, показанный на рис. 9.4, а.
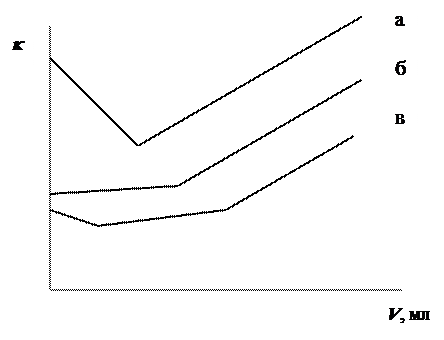 |
Рис. 9.4. Кривые кондуктометрического титрования
а – сильной кислоты сильным основанием,
б – слабой кислоты сильным основанием,
в – смеси сильной и слабой кислот сильным основанием
При постепенном добавлении к раствору кислоты (например, HCl) раствора основания (например, NaOH) концентрация ионов водорода уменьшается из-за связывания их гидроксид-ионами с образованием воды. Одновременно в растворе появляются ионы Na+, концентрация которых всё время увеличивается. Как было показано в п. 9.5, подвижность ионов Н+ намного больше подвижности ионов Na+. Поэтому проводимость раствора заметно уменьшается вплоть до точки эквивалентности, при которой достигается минимальное значение k. После связываания всех ионов Н+, когда в титруемом растворе появляются всё новые ионы ОН-, а вместе с ними и ионы Na+, проводимость начинает увеличиваться. Благодаря этому на кривой титрования в точке эквивалентности появляется излом. По его положению определяется точный объём титранта, пошедший на титрование.
Следует обратить внимание на то, что наклон второй ветви кривой титрования менее крут, чем первой, так как подвижность ионов ОН- меньше, чем подвижность ионов Н+. При титровании раствора основания раствором кислоты соотношение наклонов ветвей кривой будет обратным.
2) Титрование раствора слабой кислоты раствором сильного основания. Кривая титрования имеет вид, показанный на рис. 9.4, б. В этом случае при добавлении раствора сильного основания (например, NaOH) к раствору слабой кислоты (например, СН3СООН) концентрация ионов водорода вплоть до точки эквивалентности будет оставаться практически постоянной, так как титруются только свободные ионы Н+, возникающие при диссоциации слабой кислоты. Проводимость при этом будет несколько возрастать за счёт увеличения концентрации ионов Na+. После достижения точки эквивалентности зависимость проводимости от объёма титранта будет иметь такой же характер, как и предыдущем случае.
2) Титрование смеси растворов сильной и слабой кислот раствором сильного основания. Общий вид кривой титрования показан на рис. 9.3, в. Из-за присутствия в растворе сильной кислоты диссоциация слабой подавляется и вначале в реакцию нейтрализации будут вступать только ионы водорода, принадлежащие сильной кислоте. После того, как вся она будет оттитрована, начнётся диссоциация и последующая нейтрализация слабой кислоты и на кривой титрования появится первый излом, отвечающий объёму титранта, необходимому для полной нейтрализации сильной кислоты. Далее кривая титрования подчиняется тем же закономерностям, что и в случае 2.
На практике ветви кривых титрования могут получаться нелинейными, что связано с разбавлением раствора при добавлении титранта. Во избежание этого следует применять растворы титранта, значительно более концентрированные, чем титруемые растворы (обычно в 10 раз).
ГЛАВА 10
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 3701; Нарушение авторских прав?; Мы поможем в написании вашей работы!