
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Влияние водородного показателя на скорость коррозии
|
|
|
|
ВЫВОД: коррозия (окисление) металла всегда анодный процесс, а на катоде происходит восстановление среды.
Многие концентрированные кислоты пассивируют (блокируют, резко уменьшают скорость коррозии) многие металлы. Так концентрированная серная кислота пассивирует железо: на поверхности образуется плотная тонкая пленка FeSO4, которая препятствует проникновению серной кислоты.
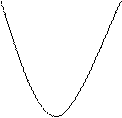
График 1 для металлов Al, Zn, Sn, Pb. Эти металлы устойчивы в нейтральной среде за счет амфотерности (стоят между истинными металлами и неметаллами в таблице Менделеева) и продукты коррозии реагируют и с кислотами и со щелочами. Таким образом, необходимо подготавливать воду для работы с теплообменниками из алюминия (поправка: Al устойчив при рН=7; Pb при рН=8; Sn при рН=9; характер кривой тот же).
скорость V КОР
коррозии

 V КОР
V КОР
 |  | ||

 | |
| |
0 7 pH 0 7 pH
График 1. График 2.
На графике 2 представлена кривая для железа: он устойчив в сильнощелочных средах.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 489; Нарушение авторских прав?; Мы поможем в написании вашей работы!