
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Структура ядра
|
|
|
|
Ядерная физика
Лекция № 14
Физика ядра и частиц
Строение ядра. Энергия связи. Радиоактивность. a, b, g - распад. Законы сохранения барионного и лептонного зарядов. Ядерные реакции. Ускорители. Их использование в медицине. Превращения элементов. Деление ядер. Ядерный синтез. Атомная и водородная бомба. Физический принцип действия ПЭТ-томографа, γ-ножа, кибер-ножа.
В начале ХХ века после открытия структуры атома для физиков представляла интерес проблема: обладает ли атомное ядро структурой, и какой эта структура могла бы быть? Экспериментальные исследования показали, что ядро обладает свойством испускать α, β и γ-лучи[1]. К тому же под действием этих лучей на ядра из них вылетали и другие частицы, то есть происходили ядерные реакции. Позднее был открыт нейтрон, который, как и протон, находится внутри ядра в виде частицы. Между ними существует сильное взаимодействие, которое примерно на два порядка интенсивнее электромагнитного. В отличие от электромагнитного взаимодействия сильные взаимодействия не являются центральными, а имеют сложный характер. Их взаимодействие можно интерпретировать как притяжение двух частиц не по прямой линии, соединяющей центры этих частиц. К тому же они зависят и от квантовых характеристик ядер.
Оказалось, что ядро достаточно сложно, и в его структуре остается много неясного и по настоящее время. Тем не менее, в начале 30-х годов была предложена модель атомного ядра, которая по-прежнему остается общепризнанной. Согласно этой модели, атомное ядро состоит из двух элементарных частиц – протонов и нейтронов [2].
Протон представляет собой ядро простейшего атома – водорода. Он имеет положительный заряд е+=+1.6×10-19 Кл и массу
|
|
|
mp=(1.672623±0.000008) ×10-27 кг = 1.007276470 а.е.м.
= 938.2723 МэВ/с2.
Нейтрон, существование которого было установлено Джеймсом Чедвиком в 1932 году, электрически нейтрален, что и объясняет его название. Его масса оказалась несколько больше массы протона:
mp=(1.674929±0.000009) ×10-27 кг = 1.008664904 а.е.м.
= 939.5656 МэВ/с2.
В свободном состоянии (то есть вне ядра) нейтрон живет примерно десять минут, а затем распадается. Внутри ядра нейтрон стабилен.
Атомная единица массы ядра (1а.е.м.) составляет 931.5 МэВ. Для ее определения предполагается, что ядро углерода весит 12 а.е.м.
Протоны и нейтроны объединяют общим наименованием нуклонов. Различные типы ядер называют нуклидами.
Каждое ядро атома характеризуется двумя числами: зарядом Z и массовым числом А. Заряд ядра Z равен числу протонов в ядре и совпадает с порядковым номером химического элемента в периодической системе. Массовое число А, равное числу нуклонов в ядре, то есть сумме числа протонов и нейтронов.
N=A-Z – число нейтронов, находящихся в ядре. Обычно атомное ядро обозначают символом 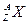 , где Х – символ химического элемента, А – массовое число, Z – атомный номер.
, где Х – символ химического элемента, А – массовое число, Z – атомный номер.
Пример 14.1. 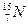 означает ядро атома азота, содержащее 7 протонов и 8 нейтронов, то есть всего 15 нуклонов.
означает ядро атома азота, содержащее 7 протонов и 8 нейтронов, то есть всего 15 нуклонов.
Пример 14.2. В ядрах углерода число протонов всегда равно 6, а число нейтронов может быть равно 5, 6, 7, 8, 9 или 10 (для ядер углерода 
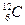 ,
, 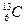 ,
, 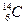 ,
, 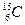 и
и 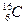 ).
).
Ядра, содержащие одинаковое число протонов, но различное число нейтронов, называются изотопами[3]. В ядрах одного химического элемента число нейтронов может быть различным, а число протонов всегда одно и то же. В природе разные изотопы распространяются неравномерно. Так распространенность в природе ядер 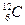 составляет 98.9%, а ядер
составляет 98.9%, а ядер 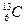 - 1.1%.
- 1.1%.
Ядра имеют примерно сферическую форму. Их размер, как уже отмечалось, впервые определил Резерфорд. Более точные измерения размеров ядер были осуществлены позднее в экспериментах по рассеянию быстрых электронов. Их радиус удобно определять по приближенной формуле:
|
|
|
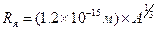 (14.1.1)
(14.1.1)
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 1215; Нарушение авторских прав?; Мы поможем в написании вашей работы!