
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Удельная и молярная электрические проводимости
|
|
|
|
ЭЛЕКТРИЧЕСКАЯ ПРОВОДИМОСТЬ РАСТВОРОВ ЭЛЕКТРОЛИТОВ
Количественной характеристикой способности растворов проводить электрический ток служит электрическая проводимость.
Растворы электролитов – это проводники второго рода. В них электрический ток обусловлен перемещением ионов под действием приложенной разности потенциалов.
Электрическая проводимость растворов электролитов, т. е. способность их проводить электрический ток, зависит от природы электролита и растворителя, концентрации, температуры и некоторых других факторов. Различают удельную и молярную электрическую проводимости.
Удельная электрическая проводимость раствора электролита c – это электрическая проводимость объема раствора, заключенного между двумя параллельными электродами, имеющими площадь по одному квадратному метру и расположенными на расстоянии одного метра друг от друга.
Удельная электрическая проводимость является величиной, обратной дельному сопротивлению r:
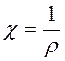
Удельное сопротивление определяется по уравнению
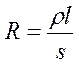
где R — общее сопротивление проводника, Ом; l – длина проводника, м; s – поперечное сечение проводника, м2. Из уравнения имеем
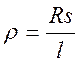
Полученное выражение показывает, что размерность, т.е. единица удельного сопротивления, выражается величиной [r] = Ом × м.
зависит от многих факторов: природы электролита, его концентрации и температуры.
Повышение температуры на 1 К увеличивает удельную электрическую проводимость примерно на 2–2,5 %. Это объясняется понижением вязкости раствора и уменьшением гидратации ионов, а для растворов слабых электролитов увеличением их степени диссоциации.
Удельная электрическая проводимость максимальна у растворов сильных кислот, несколько меньше у растворов сильных оснований, что объясняется полной диссоциацией этих электролитов. При снижении концентрации электролита до очень малых значений (при с ® 0) электрической проводимости растворов стремится к электрической проводимости чистой воды.
При изучении электрической проводимости растворов целесообразно пользоваться молярной электрической проводимостью l.
Молярная электрическая проводимость – равна удельной электрической проводимости его раствора с концентрацией 1 моль/м3.
Удельная и молярная электрические проводимости связаны между собой соотношением:
l = c Vm = c / cm
где Vm – число кубометров раствора, содержащего 1 г/моль электролита, cm – концентрация электролита, выраженная в моль/м3.
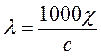
где с – молярная концентрация в моль/л.
Для слабых электролитов изменение молярной электрической проводимости от концентрации раствора связано в основном со степенью диссоциации, для сильных электролитов – с межионным взаимодействием.
Молярная электрическая проводимость с уменьшением концентрации раствора увеличивается и при с ® 0 стремится к некоторому предельному максимальному значению l¥, которое называется молярной электрической проводимостью при предельном (бесконечном) разбавлении
При бесконечном разбавлении каждый сорт ионов, присутствующих в растворе, переносит электричество независимо от других ионов и вносит в суммарную электрическую проводимость раствора определенный и постоянный вклад, пропорциональный заряду, подвижности и концентрации ионов.
Предельная молярная электрическая проводимость иона – общее количество электричества, переносимое 1 моль ионов данного сорта в бесконечном разбавленном растворе в однородном электрическом поле проходящее напряженность 1 В/м через поперечное сечение раствора площадью 1 м2 за 1 секунду.
Абсолютной скоростью движения иона называется его скорость при единичном градиенте потенциала в 1 В м-1.
Произведение абсолютной скорости движения иона на постоянную Фарадея называется подвижностями ионов; их размерность [lи] = См м2 моль-1.
Для предельно разбавленного раствора a = 1, поэтому
L¥ = l¥+ + l¥–
где l+ и l– – подвижности ионов при предельном разведении. Уравнение справедливое как для сильных, так и для слабых электролитов, называется законом Кольрауша, согласно которому молярная электрическая проводимость при предельном разведении равна сумме подвижностей ионов при предельном разведении.
По закону Кольрауша можно рассчитать степень диссоциации слабого электролита в растворе, константу диссоциации, коэффициент электрической проводимости сильного электролита в растворе.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 9477; Нарушение авторских прав?; Мы поможем в написании вашей работы!