
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Реакции аминов с кислотами
|
|
|
|
Амины, подобно аммиаку, являются основаниями. Они реагируют с разбавленными кислотами с образованием солей:
R-NH2 + HCl → R-NH3+Cl-
Эти соли при взаимодействии с водными растворами оснований выделяют амины.
В водных растворах амины подобно аммиаку существуют в виде гидратов:
СН3NH3+OH- (СН3)2NH2+OH- (СН3)3NH+OH-
Основность аминов определяется легкостью, с которой амин отщепляет протон от воды. Константа равновесия этой реакции называется константой основности Кb амина:
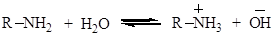

Увеличение Кb означает повышение основности (см. табл. 26.1).
Таблица 26.1
Константы основности аммиака и некоторых аминов
| Вещество | Кb |
| Аммиак | 1,8·10-5 |
| Метиламин | 4,5·10-4 |
| Этиламин | 5,1·10-4 |
| Диэтиламин | 10,0·10-4 |
| Триэтиламин | 5,6·10-4 |
Как видно из этого примера, замена атомов водорода на алкильные группы увеличивает основность азота. Это согласуется с электронодонорной природой алкильных групп, стабилизирующих сопряженную кислоту амина R3NH+ и тем самым повышающим его основность. Дополнительная стабилизация сопряженной кислоты амина происходит за счет эффекта сольватации молекулами растворителя. Триэтиламин обладает несколько меньшей основностью, чем диэтиламин. Полагают, что это вызвано уменьшением эффекта сольватации. Поскольку пространство вокруг атома азота занято алкильными группами, стабилизация на нем положительного заряда молекулами растворителя затруднена. В газовой фазе, где нет влияния молекул растворителя, триэтиламин обладает большей основностью, чем диэтиламин.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 506; Нарушение авторских прав?; Мы поможем в написании вашей работы!