
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Уравнение состояния идеального газа
|
|
|
|
Идеальным считается газ, который можно рассматривать как систему невзаимодействующих материальных точек, упруго сталкивающихся друг с другом и со стенками сосуда.
Уравнение состояния представляет собой функциональную зависимость, связывающую между собой термодинамические параметры:  .
.
Экспериментально установлено, что для 1 моля идеального газа выполняется уравнение Клапейрона (уравнение состояния 1 моля идеального газа) 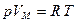 , (2.1.3)
, (2.1.3)
где 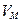 – молярный объем (объем 1 моля) газа;
– молярный объем (объем 1 моля) газа; 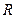 – универсальная газовая постоянная. Универсальность
– универсальная газовая постоянная. Универсальность 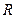 вытекает из закона Авогадро, согласно которому при одинаковых давлениях и температурах молярные объемы различных газов одинаковы. Подставив в это уравнение значения
вытекает из закона Авогадро, согласно которому при одинаковых давлениях и температурах молярные объемы различных газов одинаковы. Подставив в это уравнение значения 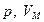 и
и  , соответствующие нормальным условиям, получим значение универсальной газовой постоянной
, соответствующие нормальным условиям, получим значение универсальной газовой постоянной 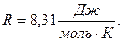
От уравнения состояния 1моля легко перейти к уравнению для любой массы 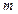 газа. При одинаковом давлении и температуре
газа. При одинаковом давлении и температуре 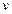 молей газа будут занимать в
молей газа будут занимать в 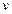 раз больший объем, чем один моль:
раз больший объем, чем один моль:  . Умножив обе части уравнения Клапейрона на
. Умножив обе части уравнения Клапейрона на 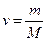
(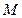 – молярная масса газа) и заменив
– молярная масса газа) и заменив 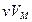 на
на 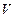 , получим уравнение состояния идеального газа (уравнение Менделеева – Клапейрона)
, получим уравнение состояния идеального газа (уравнение Менделеева – Клапейрона) 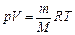 . (2.1.4)
. (2.1.4)
Разделим обе части уравнения Клапейрона на число Авогадро 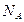 (число частиц, содержащихся в 1 моле)
(число частиц, содержащихся в 1 моле) 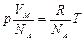 или
или 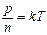 ,
,
где 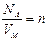 – концентрация молекул (число частиц газа, содержащихся в единичном объеме);
– концентрация молекул (число частиц газа, содержащихся в единичном объеме); 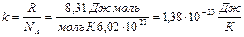 – постоянная Больцмана.
– постоянная Больцмана.
Следовательно, при постоянной температуре давление газа прямо пропорционально концентрации его молекул 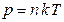 . (2.1.5)
. (2.1.5)
Это еще одна форма записи уравнения состояния идеального газа.
Выясним физический смысл универсальной газовой постоянной 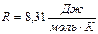 .
.
 Рис.1.1
Рис.1.1
|
Пусть в цилиндре под поршнем находится 1 моль газа, с параметрами состояния 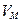 ,
, 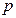 и
и  . При нагревании на
. При нагревании на  газ, изобарически расширяясь, сдвинет поршень на расстояние
газ, изобарически расширяясь, сдвинет поршень на расстояние 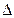
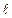 . Следовательно, сила
. Следовательно, сила 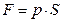 , действующая на поршень с площадью поперечного сечения
, действующая на поршень с площадью поперечного сечения  , совершит работу
, совершит работу 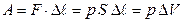 , (2.1.6)
, (2.1.6)
где 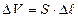 – изменение объема газа.
– изменение объема газа.
После нагревания газ займет объем  давление его не изменится. Запишем уравнения состояния 1 моля газа до нагревания и после него:
давление его не изменится. Запишем уравнения состояния 1 моля газа до нагревания и после него:
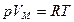 и
и  .
.
Вычтем из второго уравнения первое:  . (2.1.7)
. (2.1.7)
Выражения (2.1.5) и (2.1.7) совпали. Следовательно, универсальная газовая постоянная численно равна работе, которую совершает 1 моль идеального газа изобарически расширяясь при нагревании на  .
.
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 318; Нарушение авторских прав?; Мы поможем в написании вашей работы!