
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Лекция 15. 1. Количество независимых величин, с помощью которых задается положение системы называется числом степеней свободы
|
|
|
|
Основные выводы.
1. Количество независимых величин, с помощью которых задается положение системы называется числом степеней свободы. Положение материальной точки полностью задается тремя координатами, т.е. число степеней свободы равно 3. Для твердого тела необходимо дополнительно задать его ориентацию относительно центра масс, определяемую тремя углами, т.е. число степеней свободы равно 6. В случае двухатомных молекул (H2, O2 и др.) вращение вокруг оси, соединяющей атомы не учитывается, т.е. число степеней свободы равно 5.
2. Закон равномерного распределения энергии:
На каждую степень свободы молекулы в среднем приходится одинаковая кинетическая энергия, равная 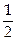 kT.
kT.
Поэтому средняя кинетическая энергия одноатомных газов равна < Ek > = 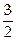 kT, а газов, имеющих двухатомные молекулы она равна < Ek > =
kT, а газов, имеющих двухатомные молекулы она равна < Ek > = 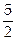 kT.
kT.
3. Распределение скоростей молекул газа описывается формулой, полученной Д. Максвеллом:
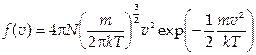 .
.
Распределение Максвелла для данного газа зависит только от абсолютной температуры, при этом с повышением температуры появляется больше молекул с более высокими скоростями.
Среднее значение скорости молекул: 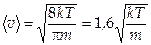 .
.
Средне квадратичное значение скорости молекул: 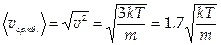 .
.
Наиболее вероятное значение скорости молекул: 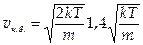 .
.
В процессе испарения жидкости часть молекул переходит в газовую фазу. Некоторая часть их из газовой фазы переходит в жидкость (конденсация). При равенстве этих чисел наступает динамическое равновесие или насыщение. Давление пара в этом случае называется давлением насыщенного пара. При росте температуры давление насыщенного пара растет.
Когда температура достигает величины, при которой давление насыщенного пара равно внешнему давлению, начинается процесс кипения жидкости.
8. Для оценки содержания паров воды в воздухе используется величина, которая называется относительной влажностью. Парциальное давление паров воды при данной температуре зависит от количества молекул воды в газовой фазе и может меняется от нуля до давления насыщенного пара. Относительная влажность определяется следующим образом:
| Относительная влажность = | Парциальное давление Н 2 О | × 100%. |
| Давление нас. пара Н 2 О |
Если парциальное давление превосходит давление насыщенного пара происходит конденсация, в результате чего может образоваться роса, туман, облака.
|
|
|
|
|
Дата добавления: 2014-01-06; Просмотров: 241; Нарушение авторских прав?; Мы поможем в написании вашей работы!