
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Значение коэффициента распределения kp некоторых загрязняющих веществ между экстрагентами и водой при комнатной температуре
|
|
|
|
| Экстрагируемое из воды вещество | Экстрагент | kp |
| Анилин | Бутилацетат | |
| Толуол | 8—19 | |
| Бензойная кислота | Диэтиловый эфир | 71—91 |
| Бутилацетат | ||
| Толуол | 6—12 | |
| Муравьиный альдегид | Амиловый спирт | |
| Пикриновая кислота | Толуол | 1,7-8,7 |
| Бензол | 0,7—5,3 | |
| Хлороформ | 1,2—2,6 | |
| Пиридин | Толуол | 1,4—9,3 |
| Салициловая кислота | Ацетон | |
| Толуол | 1,7—2,5 | |
| Бензол | 1,7—4,5 | |
| Хлороформ | 2,9—4,3 | |
| л-Толуидин | Бензол | 51—60 |
| Фенол | Бутилацетат | |
| Амиловый спирт | 14—16 | |
| Толуол | 1,7—9,4 | |
| Бензол | 2,3—12,5 | |
| Хлороформ | 3,4—12,5 | |
| Хлоруксусная кислота | Амиловый спирт | 3,6 |
Очистка сточных вод методом экстракции может быть осуществлена тремя способами: одно- или многократной обработкой одного и того же объема воды свежими порциями экстрагента; перемешиванием воды и экстрагента в одном аппарате по принципу противотока с последующим распределением жидкости; перемешиванием воды и экстрагентов в нескольких аппаратах, работающих по принципу противотока.
Конечная концентрация извлекаемого вещества в воде может быть вычислена по уравнению
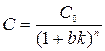 , (2)
, (2)
где С0 – начальная концентрация вещества в воде; n – число экстракций; b – удельный расход экстрагента (в объемах на объем воды) для одной экстракции
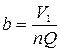 , (3)
, (3)
где V1 – общий объем экстрагента, затрачиваемый на экстракцию; Q – количество сточной жидкости, подвергаемой экстракции.
Анализ уравнения (2) показывает, что многократная экстракция малыми дозами экстрагента более эффективна, чем однократная большой дозой.
Экстракия может быть непрерывной или периодической (при очистке небольших количеств сточных вод
Экстрактор представляет собой колонку с насадкой, в которую подается вода и экстрагент. Если удельный вес экстрагента меньше удельного веса воды, экстрагент подают снизу, при обратном соотношении – сверху. Чтобы поддержать постоянный уровень жидкости, воду спускают из колонки через сифон, сообщающийся с ее верхней частью.
Материальный баланс процесса непрерывной экстракции может быть выражен уравнением
C0Q = CQ + xV (4)
где x – концентрация вещества в экстрагенте, г на 1 л экстрагента.
При максимальной насыщенности экстрагента
X= kC0. (5)
Подставив это выражение и произведение bQ вместо V в формулу (4) получим:
C= (1-bk) C0;
В том случае, когда концентрация вещества в очищенной воде задается заранее, а искомой величиной является удельный расход экстрагента b, последний определяют по формуле
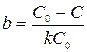 .
.
Высоту колонного экстрактора Н, достаточную для достижения необходимой степени очистки сточной жидкости, и диаметр d, обеспечивающий необходимую производительность, находят графоаналитическим методом по лабораторным исследованиям хода процесса экстракции для каждого растворенного вещества и экстрагента.
При многократной экстракции на противотоке уравнение для конечной концентрации имеет вид
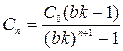
где n – количество экстракторов.
Число экстракций, необходимое для снижения концентрации с С0 до С, будет:
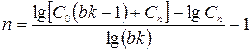 .
.
Для выделения загрязняющих веществ из сточных вод можно использовать следующие методы жидкостной экстракции, которые различают по схемам контакта экстрагента и сточной воды: перекрестноточные, ступенчато-противоточные и непрерывно-противоточные.
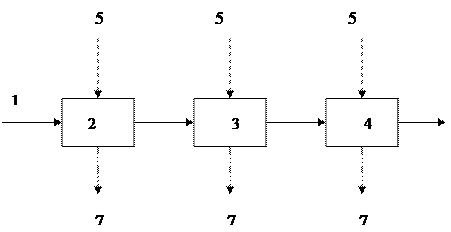
Рис. Схема процесса многоступенчатой перекрестноточной экстракции: 1-подача сточной воды; 2-4 – экстаркционные установки соответственно I, II и III ступеней; 5- подача чистого экстракта; 6- выпуск очищенной сточной воды; 7- отвод экстракта.
При этой схеме очистки на каждую ступень экстракции подают свежий экстрагент, что приводит к значительным его расходам. Поэтому практическое применение получили методы ступенчато-противоточной и непрерывно-противоточной экстракции.
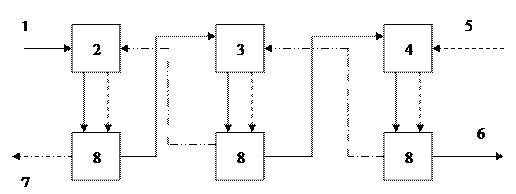
Рис. Схема ступенчато-противоточной экстракции: 1- подача сточной воды; 2-4 экстракционные установки соответственно I, II и III ступеней; 5- подача чистого экстрагента; 6- выпуск очищенной сточной воды; 7- отвод экстрагента; 8- отстойники или сепараторы.
Каждая ступень рассматриваемой схемы состоит из перемешивающего устройства для смешения фаз и отстойник для их гравитационного разделения, либо используются центробежные сепараторы, обладающие более высокой разделительной способностью по сравнению с гравитационными. Чистый экстрагент и обрабатываемая сточная вода поступают с противоположных концов системы, последовательно соединенных ступеней экстракции. Сточная воды и экстрагент движутся непрерывно через систему противотоком друг к другу, причем экстракт последующей ступени смешивается в смесителе с водной фазой предыдущей ступени. Ступенчато-противоточная экстракция может быть непрерывной или периодической (при малых расходах сточных вод).
Непрерывно-противоточная экстракция характеризуется тем, что вода и экстрагент движутся навстречу друг другу в одном аппарате, обеспечивающем диспергирование экстрагента в воде. Загрязняющие вещества из сточной воды переходят в экстрагент.
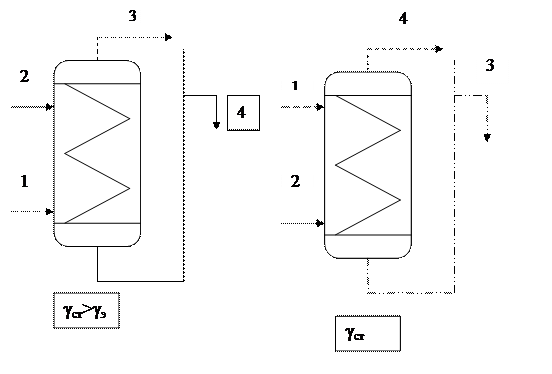
Рис. Схемы процесса непрерывной экстракции: 1,2- подача соответственно экстрагента и сточной воды; 3,4- отвод соответсвенно отработанного экстрагента и очищенной воды (γст- плотность сточной воды, γэ – плотность экстрагента).
4.3. СОРБЦИЯ
Представляет собой один из наиболее эффективных методов глубокой очистки сточных вод. Сорбенты способны извлекать из воды многие органические вещества, в том числе и биологически жесткие, не удаляемые из нее другими методами. При использовании высокоактивных сорбентов воду можно очистить от загрязняющих веществ (сорбатов) до практически нулевых остаточных концентраций. Кроме того, сорбенты могут извлекать вещества из воды при любых концентрациях, в том числе и очень малых, когда другие методы очистки оказываются неэффективными.
Сорбцию следует применять в тех случаях, когда необходима особенно глубокая очистка сточной жидкости, например, при сбросе ее в водоем на особо охраняемых участках или при направлении ее в систему промышленного водоснабжения бессточных предприятий.
В качестве сорбентов практически могут служить все мелкодиспесные твердые вещества, обладающие развитой поверхностью – опилки, зола, торф, различные глины, коксовая мелочь и др. Наиболее эффективными сорбентами являются активные угли (АУ) различных марок.
Активные угли являются пористыми материалами, поры которых по своему размеру могут быть подразделены на четыре вида: макропоры размером 1000-20000 Ǻ, переходные поры – 40-1000 Ǻ, супермикропоры – 16-40 Ǻ и микропоры – не более 16 Ǻ. Эффективность АУ обуславливается наличием в них микропор, а также в определенной степени супермикропор.
Растворенные органические вещества имеют размер менее 10 Ǻ. Они заполняют объем микропор сорбента, полная удельная вместимость, см3/г, который соответствует поглощающей способности сорбента. Поэтому объем микропор W01 является одной из важнейших характеристик и приводится в спецификациях соответствующих марок активных углей. Известную сорбционную активность проявляют и супермикропоры; в характеристике АУ приводится и их объем W02. Сорбционная активность макропор и переходных пор проявляется лишь сорбцией вещества поверхностью стенок и количество сорбированного на них вещества значительно меньше, чем в микропорах. Поэтому макропоры и переходные поры служат главным образом путями подвода сорбата к микропорам.
Другой важной характеристикой АУ является структурно-энергетическая константа В, град-2. Она может также приводиться для микропор и супермикропор (В01 и В02).
Характеристиками АУ являются также их насыпной удельный вес, г/см3; механическая прочность, %; диаметр зерен, мм; цена за 1 т и др.
Сорбция в статических условиях осуществляется путем интенсивного перемешивания обрабатываемой воды с сорбентом в течение определенного времени t и последующего отделения сорбента от воды в результате отстаивания, отфильтровывания и т.п. Если в отделенную от сорбента воду внести новую порцию чистого сорбента и перемешивать воду с сорбентом в течение того же времени, то концентрация загрязняющего вещества в воде еще уменьшится. Последовательным введением чистых порций сорбента в очищаемую воду можно очистить ее от загрязняющего вещества до любой заданной концентрации Cn.
При однократном введении сорбента в количестве m г на 1 л обрабатываемой воды исходным расчетным уравнением является уравнение баланса вещества:
m a + QC = QC0,
где a – удельная сорбция; Q – количество обрабатываемых сточных вод; C – концентрация вещества, устанавливающаяся в воде после перемешивания воды и сорбента в течение времени t; С0 – концентрация вещества в исходной воде.
Используя уравнение баланса можно определить расход сорбента при заданном значении концентрации вещества в очищаемой воде, концентрацию очищенной жидкости при принятом количестве сорбента.
При достаточно длительном перемешивании воды с сорбентом (например, в течение нескольких часов) значения С и а будут равновесными:
аравн= kадсСравн.
Однако фактическое время перемешивания t может быть принято значительно меньше tравн при котором достигается практически равновесное состояние. В этом случае соотношение между С и а будет:
а = k C
При этом значение k будет меньше, чем kравн, и а меньше, чем аравн.
Величины а и аравн связаны между собой зависимостью
 ,
,
где α и t0 – кинетические параметры, устанавливаемые по экспериментально измеренным С1 и С2 после контакта воды с сорбентом в течение t1 и t2.
Таким образом, для расчета установок по статической сорбции в распоряжении проектировщика должны быть изотерма сорбции (график зависимости а от С) и два значения текущих концентраций сорбата С1 и С2 соответствующих времени перемешивания воды с сорбентом t1 и t2. По этим данным вычисляются необходимые вспомогательные величины α и t0, а также определяются значения С, а и k.
При применении многоступенчатой сорбционной очистки с последовательным введением в воду сорбента расчет следует выполнять по формулам:
концентрация сорбата после n-й ступени введения сорбента
 ;
;
и этом случае задаются дозой сорбента вводимой в воду на каждой ступени, и числом ступеней n;
доза сорбента, вводимого на каждой ступени установки
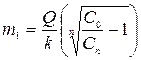 ;
;
здесь задаются концентрацией сорбата Сn после n-ой ступени и числом ступеней n;
число ступеней
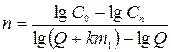 ;
;
в данном случае задаются концентрацией сорбата Cn в очищенной воде и дозой сорбента m1, вводимого на каждой ступени установки.
Общий расход сорбента
mоб = n m1.
При использовании адсорбционных установок, работающих в статических условиях, используют активный уголь в виде частиц 0,1 мм и меньше.
Статическая одноступенчатая адсорбция нашла применение в тех случаях, когда адсорбент очень дешев или является отходом производства. Более эффективно (при меньшем расходе адсорбента) процесс протекает при использовании многоступенчатой установки.
В динамических условиях процесс очистки проводят при фильтровании сточной воды через слой адсорбента. Скорость фильтрования зависит от концентрации растворенных веществ и колеблется от 2-4 до 5-6 м3/(м2 . ч). Вода в колонне движется снизу вверх, заполняя все сечение. Адсорбент применяется в виде частиц размером в пределах 1,5-5 мм. При более мелких зернах возрастает сопротивление фильтрованию жидкости. Уголь укладывают на слой гравия, расположенного на решетке. Во избежание забивки адсорбента сточная вода не должна содержать твердых взвешенных примесей.
В одной колонне при неподвижном слое угля процесс очистки ведут периодически до проскока, а затем адсорбент выгружают и регенерируют. При непрерывном процессе используют несколько колонн. По такой схеме две колонны работают последовательно, а третья отключена на регенерацию.
В момент проскока в колонне появляется слой адсорбента, который не работает, этот слой называют «мертвым» слоем. Если одновременно выводить из колонны «мертвый» слой и вводить в нее такой же слой свежего адсорбента, то колонна будет работать непрерывно. Для подачи адсорбента имеются специальные дозаторы.
Установки с псевдоожиженным слоем (периодического или непрерывного действия) целесообразно применять при высоком содержании взвешенных веществ в сточной воде. Размер частиц адсорбента при этом должен быть равным 0,5 – 1 мм. Скорость потока для частиц указанных размеров находится в пределах 8-12 м/ч
В аппаратах с псевдоожиженным слоем отношение Н/Н0 (Н0 – высота неподвижного слоя адсорбента; Н высота псевдоожиженного слоя) рекомендуется поддерживать в пределах 1,4-1,6. Применяются адсорберы различных типов
Регенерация адсорбента. Важнейшей стадией процесса адсорбционной очистки является регенерация активного угля. Адсорбированные вещества из угля извлекают десорбцией насыщенным или перегретым водяным паром либо нагретым инертным газом. Температура перегретого пара при этом (при избыточном давлении 0,3-0,6 МПа) равна 200-300ºС, а инертных газов 120-140ºС. Расход пара при отгонке легколетучих веществ равен 2,5-3 кг на 1 кг отгоняемого вещества, для высококипящих – в 5-10 раз больше. После десорбции пары конденсируют и вещество извлекают из конденсата.
Для регенерации углей может быть использована и экстракция органическими низкокипящими и легко перегоняющимися с водяным паром растворителями. При регенерации органическими растворителями (метанолом, бензолом, толуолом, дихлорэтаном и др.) процесс проводят при нагревании или без нагревания. По окончании десорбции остатки растворителей из угля удаляются острым паром или инертным газом.
В некоторых случаях перед регенерацией адсорбированное вещество путем химического превращения переводят в другое вещество, которое легче извлекается из адсорбента. В том случае, когда адсорбированные вещества не представляют ценности, проводят деструктивную регенерацию химическими реагентами (окислением хлором, озоном или термическим путем).
Термическую регенерацию проводят в печах различной конструкции при температуре 700-800ºС в бескислородной среде. Регенерацию ведут смесью продуктов горения газа или жидкого топлива и водяного пара. Она связана с потерей части адсорбента (15-20%). Разрабатываются биологические методы регенерации углей, при которых адсорбированные вещества биохимически окисляются. Этот способ регенерации значительно удлиняет срок использования сорбента.
4.4. ионный обмен
Ионообменная очистка применяется для извлечения из сточных вод металлов (цинка, меди, хрома, никеля, свинца, ртути, кадмия, ванадия, марганца и др.), а также соединений мышьяка, фосфора, цианистых соединений и радиоактивных веществ. Метод позволяет рекуперировать ценные вещества при высокой степени очистки воды. Ионный обмен широко распространен при обессоливании в процессе водоподготовки.
Природные и синтетические иониты. Иониты (катиониты и аниониты) бывают неорганические (минеральные) и органические. Это могут быть природные вещества или вещества, полученные искусственно.
К неорганическим природным ионитам относятся глинистые минералы, полевые шпаты, различные слюды и др.
К неорганическим синтетическим ионитам относятся силикагели, пермутиты, труднорастворимые оксиды и гидроксиды некоторых металлов.
Органические природные иониты – это гуминовые кислоты почв и углей. Они проявляют слабокислотные свойства. Для усиления кислотных свойств и обменной емкости угли измельчают и сульфируют в избытке олеума. К недостаткам таких ионитов следует отнести их малые химическую стойкость и механическую прочность зерен, а также небольшую обменную емкость, особенно в нейтральных средах.
К органическим искусственным ионитам относятся ионообменные смолы с развитой поверхностью. Они приобрели наибольшее практическое значение для очистки сточных вод.
В зависимости от степени диссоциации катионобменные смолы бывают сильно- и слабокислотные, а анионобменные – сильно и слабоосновные. Иониты, содержащие одинаковые активные группы, называются многофункциональными, а иониты, которые содержат функциональные группы различной химической природы, - полифункциональными. Они могут обладать смешанными сильно и слабоосновными свойствами.
В маркировке смол для катионитов употребляют букву К, для обозначения анионитов – А. Буква В – (после А) записывается для высокоосновных анионитов, буква Н – для низкоосновных анионитов. Числовое обозначение указывает порядковый номер производственной серии. Например, КУ – катионит универсальный; КФ – катионит фосфорнокислый; АВ – анионит высокоосновный; АН – анионит низкоосновный.
Смолы зарубежных стран часто имеют названия фирм изготовителей.
Регенерация ионитов. Катиониты регенерируют 2-8%-ми растворами кислот. При этом они переходят в Н- форму. Регенерационные растворы – элюаты содержат катионы. Затем после взрыхления и промывки катиониты заряжаются, например в Na – форму, путем пропускания через них раствора поваренной соли.
Отработанные аниониты регенерируются 2-6 %-ми растворами щелочи. Аниониты при этом переходят в ОН-форму. Элюаты содержат в концентрированном виде все извлеченные из сточных вод анионы.
Схемы ионообменных установок. Процессы ионообменной очистки сточных вод проводят на установках периодического и непрерывного действия. Первые состоят из аппаратов (фильтров или колонн) периодического действия, насосов, емкостей и контрольно- измерительных приборов. Установки различаются схемой подачи регенерационного раствора (эжектированием или дозированием). Цикл работы аппарата состоит из следующих стадий: 1) ионообмен; 2) отмывка ионита от механических примесей; 3) регенерация ионита; 4) отмывка ионита от регенерирующего раствора.
Работа установки может быть интенсифицирована путем использования аппаратов с кипящим слоем ионита. Скорость процесса в этом случае увеличивается в 2-3- раза. Взвешенный слой имеет меньшее гидравлическое сопротивление.
Для глубокой финишной очистки воды присоединяют установки со смешанным слоем анионитов и катионитов. В них иониты используют однократно или с внутренней или выносной регенерацией.
Недостатки установок периодического действия: большие объемы аппаратов, значительный расход реагентов, большая единовременная загрузка сорбента, сложность автоматизации процесса.
Непрерывный ионообмен дает возможность уменьшить затраты смолы, реагентов для регенерации, промывной воды, а также применять более компактное оборудование по сравнению с периодическим ионообменником..
Аппараты для ионного обмена классифицируются по различным признакам: 1) по организации процесса – на аппараты непрерывного, полунепрерывного и периодического действия; 2) по гидродинамическому режиму – на аппарат вытеснения, смешения и промежуточного типа; 3) по состоянию слоя ионита –с неподвижным, движущимся, пульсирующим, перемешиваемым и циркулирующим слоем; 4) по организации взаимного направления движения фаз на прямоточные, противоточные и со смешанным током; 6) по конструкции – на колонные и емкостные; 7) по способу подвода энергии – без подвода энергии извне (с гравитационным движением твердой фазы) и с подводом энергии извне (принудительное движение твердой фазы).
Ионообменные установки предназначены для обессоливания и очистки сточных вод от ионов металлов, а также других загрязнений до заданных концентраций.
Очистку производят с применением ионитов – синтетических ионообменных смол, выпускаемых в виде гранул размером 0,2-2 мм. Иониты представляют собой практически нерастворимые в воде полимерные вещества, имеющие подвижный ион (катион или анион), способный в определенных условиях вступать в реакцию обмена с ионами того же знака, находящимися в растворе.
При контакте с водой иониты набухают и увеличиваются в объеме (обычно в 1,5-2 раза). Большинство ионитов хранят во влажном состоянии или под слоем воды.
Различают сильно- и слабокислотные катиониты (в Н+ или Na+-форме) и сильно- и слабоосновные аниониты (в ОН- или солевой форме), а также иониты смешанного типа.
Выпускаемые иониты снабжаются паспортом, в котором указываются следующие основные характеристики: марка ионита, фракционный состав, мм; содержание рабочей фракции, %; содержание влаги, %; насыпная плотность товарного ионита, т/м3; удельный объем набухшего ионита, м3/т; средняя рабочая обменная емкость, г.экв/м3; полная обмененная емкость, г.экв/м3; допустимая температура воды при очистке, ˚С.
Ионообменную очистку производят последовательным фильтрованием через катиониты и аниониты. При контакте воды с Н-катионитом происходит обмен катионов растворенных в воде солей на Н+-ионы катионита по уравнению
n[K]H+Men+↔[K]nMe+nH+
где [K] – радикал, или “скелет” катионита; Ме – извлекаемый катион металла; n – валентность металла.
В результате Н-катионирования повышается кислотность воды.
При фильтровании ее через ОН-анионит происходит обмен анионов кислот на ОН—ионы анионита по уравнению
m[An]OH+Am↔[An]mA+mOH-,
где [An] – каркас, или «скелет» анионита; А – извлекаемый анион; m – валентность аниона.
При наличии в воде анионов сильных и слабых кислот анионирование производят в две ступени. Вначале извлекают анионы сильных кислот на слабоосновных анионитах, а затем анионы слабых кислот на сильноосновных анионитах.
Обменная емкость сильнокислотных катионитов и сильноосновных анионитов по отношению к различным ионам остается постоянной в широком интервале значений рН. Обменная емкость слабокислотных катионитов и слабоосновных анионитов в большой степени зависит от величины рН и максимальна для слабокислотных катионитов в щелочной среде (рН>?), а для слабоосновных анионитов в кислой среде. Иониты смешанного типа проявляют свойства смеси сильной и слабой кислот или сильного и слабого основания.
В процессе очистки иониты уплотняются. По мере насыщения ионитов их регенерируют. Перед регенерацией иониты взрыхляют очищенной водой с интенсивностью 3-5 л/(с.м2). Регенерацию катионитов осуществляют 2-8%-ными растворами кислот, анионитов – 2-6%-ными растворами щелочей. После регенерации производят отмывку ионитов.
Продуктами регенерации являются элюаты – растворы кислот и щелочей, содержащие извлекаемые из ионитов компоненты. Первые порции элюатов являются наиболее концентрированными по извлекаемым компонентам. Их нейтрализуют или обрабатывают с целью утилизации ценных продуктов. Нейтрализацию осуществляют смешением кислых и щелочных элюатов, а также дополнительным введением кислоты или щелочи.
В зависимости от состава исходной воды и требуемой степени очистки применяют различные схемы ионообменных установок.
Содержание взвешенных веществ в очищаемой воде и ее ХПК не должны превышать 8 мг/л. В противном случае в состав установки включают сооружения предварительной очистки с кварцевыми и сорбционными фильтрами. В ряде случаев для стабилизации рН очищенной воды и извлечения анионов слабых кислот вместо анионитовых фильтров второй ступени используют фильтры смешанного действия, загружаемые сильнокислотными катионитами и сильноосновными анионитами.
Необходимый объем ионита W, м3, определяют по формуле
W=24QΣu/nEраб,
Где Q – производительность установки, м3/ч; Σu – суммарная концентрация извлекаемых ионов, мг-экв/л; n – число регенераций в сутки4 Ераб – рабочая обменная емкость ионита, г-экв на 1 м3 ионита:
Ераб = αэЕполн - dg Σu,
Здесь αэ – коэффициент эффективности регенерации, принимается равным 0,8-0,9; g – удельный расход отмывочной воды, принимается 3-4 м3 на м3 ионита; d – коэффициент, учитывающий тип ионита: для катионов принимается равным 0,5, для анионитов – 0,8; Еполн – полная динамическая обменная емкость ионита, г.экв на 1м3 ионита.
Площадь рабочих фильтров F, м2, определяют по формуле
F = Q/v,
Где v – скорость фильтрования сточной воды, м/ч; принимается в зависимости от солесодержания обрабатываемой воды: не более 20, 15,10 и 8 м/ч при солесодержании соответственно до 5, 5-15, 15-20, 20 мг-экв/л и более.
Число работающих фильтров каждой ступени должно быть не менее двух. Число резервных фильтров определяется продолжительностью фильтроцикла, временем регенерации и требованиям непрерывной работы установки
Скорость фильтрования принимается от 5 до 25 м/ч. Потери напора в фильтрах в зависимости от режима фильтрования, размера зерен загрузки и высоты ее слоя составляют от 4 до10 м.
Н – катионитовые фильтры первой ступени служат для извлечения многовалентных ионов металлов, фильтры второй ступени – для извлечения ионов натрия, калия и аммония.
Расход технической кислоты на регенерацию одного фильтра Рк определяется по формуле
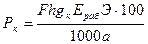 ,
,
где F – площадь фильтра, м2; h – высота слоя катионита в фильтре, м; gк – удельный расход кислоты, г-экв на 1 г-экв рабочей емкости; Э – эквивалентный вес кислоты; а – содержание чистой кислоты в товарном продукте, %.
Для взрыхления катионита перед регенерацией используют отмывочные воды; интенсивность взрыхления 3-4 л/(с.м2), продолжительность 0,25 ч. Отмывку катионита производят обессоленной водой со скоростью 6-8 м/ч и удельным расходом 2,5-3 м3 на 1 м3 катионита. Первые порции отмывочной воды используют на приготовление регенерирующих растворов, последующие – на взрыхление катионита.
Н-катионитовые фильтры второй ступени рассчитываются аналогично.
Анионитовые фильтры первой ступени применяют для удаления из воды анионов сильных кислот. Объем анионита для загрузки этих фильтров определяется по приведенной выше формуле.
Площадь анионитовых фильтров первой ступени F определяют по формуле
F = 24Q/nTv,
где v – принимаемая скорость фильтрования, равная 8-20 м/ч; Т – продолжительность работы каждого фильтра между регенерациями, ч;
T=24/n - t1 - t2 - t3,
t1 – продолжительность взрыхления анионита, равная 0,25 часа; t2 – продолжительность регенерации щелочью, равная 2,5-4 ч; t2 – продолжительность отмывки анионита после регенерации, равная 1-2 ч.
Для регенерации анионитовых фильтров первой ступени применяют 4-6%ные растворы едкого натра, кальцинированной соды или аммиака; удельный расход реагента на регенерацию – 2,5 г-экв и 1 г-экв поглощенных анионов.
Расчет фильтров смешанного действия (ФСД) выполняют по приведенным выше формулам, скорость фильтрования принимают до 50 м/ч. При регенерации ФСД иониты взрыхляют потоком воды снизу-вверх с разделением катионита (нижний слой) и анионита (верхний слой), после чего пропускают через анионит раствор едкого натра, а через катионит – серную кислоту и производят отмывку обессоленной водой.
Примеры ионообменной очистки. Извлечение ионов металлов зависит от концентрации их в воде, рН, обжей минерализации воды, а также от наличия и концентрации ионов кальция и железа. Ля рекуперации металлов используют катиониты как сильнокислотные (в водородной форме), так и слабокислотные (в натриевой форме).
Ионы цинка извлекают на сильнокислотном сульфокатионите КУ-2×8 в Н-форме или на карбоксильном катионите КБ-4 в Na-форме. Динамическая обменная емкость по Zn2+ катионита КУ-2 равна 2-3, а КБ-4 – 5 мг-экв/г. Сильнокислотные катиониты извлекают иониы цинка в широком диапазоне значений рН. Карбоксильные катиониты применяют при очистке нейтральных или слабощелочных сточных вод. Регенерацию сульфокатионитов производят 10%-м раствором серной кислоты; карбоксильные катиониты регенерируют 5%-м раствором Na2SO4. Концентрация цинка в элюатах составляет 6-9 г/л.
Ионы меди извлекают из сточных вод катионитом КУ-1 при рН=12-12,4. Сорбционная емкость их равна 37-50 г на 1 л набухшей смолы. Регенерацию проводят 5%-м раствором HCl. Концентрация меди в элюатах достигает 15-17 г/л. Из кислых сточных вод медь извлекают сильнокислотными катионитами. Их регенерируют 10-120%-м раствором серной кислоты.
Ионы никеля извлекают из воды на катионите КЧ-2×8, динамическая обменная емкость которого равна 63-70 г/кг катионита. Скорость фильтрования сточных вод 12-15 м/ч. Регенерацию проводят 20%-м раствором серной кислоты с скоростью 0,5 м/ч. Полученные при регенерации элюаты содержат 95 г/л никеля и их можно использовать при никелировании.
Для удаления из сточных вод катионов Cr3+ применяют Н-катиониты, а хромат-ионы CrO42- и бихромат-ионы Cr2O72- извлекают на анионитах АВ-17, АН-18-П, АН-25. Емкость анионитов по хрому не зависит от величины рН в пределах от 1 до 6 и значительно снижается с увеличением рН>:. При концентрации Cr6+ в сточной воде от 800 до 1400 моль экв/л обменная емкость анионита АВ-17-8 составляет 270-376 моль экв/ м3. Скорость фильтрования принимают равной 10-15 м/ч.
Регенерацию сильноосновных анионитов проводят 8-10%-м раствором едкого натра. Элюаты, содержащие 40-50 г/л шестивалентного хрома могут быть рекуперированы. Скорость регенерации составляет 1-1,5 м/ч.
При наличии в сточной воде нескольких катионов объем катионита рассчитывают по наименее сорбируемому иону. Расчетную концентрацию принимают равной сумме концентраций всех удаляемых катионов. Регенерируют катионит раствором серной кислоты или сульфата натрия. При высоком содержании в сточной воде ионов кальция во избежание загипсовывания слоя катионита для регенерации применяют соляную кислоту или хлорид натрия.
Элюаты от регенерации катионитов представляют собой кислые растворы смеси солей различных металлов. Переработка таких элюатов для выделения металлов трудоемка.
Простые и комплексные цианиды извлекаются на анионитах. Цианиды – соли цианистоводородной кислоты. В сточных водах присутствуют в виде простых (CN-) и комплексных Me(CN)nm анионов.
Сточные воды с щелочной реакцией обрабатываются анионитами в солевой форме, нейтральные и кислые воды – ионитами в гидроксидной и солевой форме. Сильноосновный анионит регенерируют 5-10%-м раствором едкого натра или хлоридом натрия. Регенерация происходит не полностью (простые цианиды десорбируются на 80-90%, комплексные на 42-78%). Для более полной регенерации требуется значительный расход регенерирующих растворов.
Фенолы из сточных вод можно извлекать анионитами (в ОН-форме) или катионитами. Катиониты применяют для обработки минерализованных кислых и нейтральных сточных вод, аниониты – для обезфеноливания слабоминерализованных сточных вод. Скорость фильтрования сточных вод принимают 8-10 м/ч при концентрации фенола до 1 г/л и 2-3 м/ч – при 3-15 г/л.
Регенерацию анионитов производят 4-10%-м раствором водным или водно - спиртовым (метанольным) растворами едкого натра при скорости фильтрования 0,5-0,8 м/ч. Концентрация фенола в элюате достигает 5% (об.). Элюаты используют в производстве сырого фенола. Для извлечения фенола на 60% при регенерации анионита ЭДЭ-10П требуется 10-кратный расход, а АВ-17 – 2,5 кратный расход NaОН по сравнению со стереометрическим.
Катиониты регенерируют метанолом при скорости фильтрования 0,3-0,5 м/ч. Расход метанола зависит от исходной концентрации фенола и составляет 15-20 л на 1 кг извлеченного фенола. После ректификации метанол используют повторно для регенерации катионитов, а фенолят натрия – для получения фенола.
4.5. ОБРАТНЫЙ ОСМОС И УЛЬТРАФИЛЬТРАЦИЯ
Обратным осмосом и ультрафильтрацией называют процессы фильтрования растворов через полупроницаемые мембраны под давлением превышающем осмотическое давление. Мембраны пропускают молекулы растворителя, задерживая растворенные вещества. При обратном осмосе отделяются частицы (молекулы, гидратированные ионы), размеры которых не превышают размеров молекул растворителя. При ультрафильтрации размер отдельных частиц dч на порядок больше. Условные границы применения этих процессов составляют:
| Процесс | Обратный осмос | Ультрафильтрация | Микрофильтрация |
| dч, мкм | 0,0001-0,001 | 0,001-0,02 | 0,02-10 |
Т.о., от обычной фильтрации такие процессы отличаются отделением частиц меньших размеров. Давление, необходимое для проведения процесса обратного осмоса (6-10 МПа), значительно больше, чем для процесса ультрафильтрации (0,1-0,5 МПа).
Обратный осмос широко используется для обессоливания воды в системах водоподготовки ТЭЦ и предприятий различных отраслей промышленности (полупроводников, кинескопов, медикаментов и др.); в последние годы начинает применяться для очистки некоторых промышленных и городских сточных вод.
Схема установки обратного осмоса
 1 – насос высокого давления
1 – насос высокого давления
2 – модуль обратного осмоса
3 - мембрана
4 – выпускной клапан
Достоинствами метода являются: отсутствие фазовых переходов при отделении примесей, что позволяет вести процесс при небольшом расходе энергии; возможность проведения процесса при комнатных температурах без применения или с небольшими добавками химических реагентов; простота конструкций аппаратуры. Недостатки метода: возникновение явления концентрационной поляризации, которое заключается в росте концентрации растворенного вещества у поверхности мембраны. Это приводит к уменьшению производительности установки, степени разделения компонентов и срока службы мембран; проведение процесса при повышенных давлениях, что вызывает необходимость специальных уплотнений аппаратуры.
Эффективность процесса зависит от свойств применяемых мембран. Они должны обладать следующими достоинствами: высокой разделяющей способностью (селективностью), большой удельной производительностью (проницаемостью), устойчивостью к действию среды, неизменностью характеристик в процессе эксплуатации, достаточной механической прочностью, низкой стоимостью.
Селективность φ (в %) процесса разделения определяют по формуле
φ = 100 (с0 - сф)/ с0,
где с0 и сф – концентрации растворенного вещества соответственно в исходной сточной воде и фильтрате.
Проницаемость определяется количеством фильтрата Vф, полученного в единицу времени с единицы рабочей поверхности:
Vф = k1 (ΔР – ΔР0),
Где ΔР – разность давлений воды до и после мембраны; ΔР0 – разность осмотических давлений; k1 – коэффициент пропорциональности, зависящий от проницаемости мембраны.
Таким образом, скорость обратного осмоса прямо пропорциональна эффективному давлению (разности между приложенным давлением и осмотическим). Эффективное давление значительно превосходит осмотическое. Осмотическое давление для растворов некоторых солей концентраций 1000 мг/л составляет:
| Соль NaCl Na2SO4 MgSO4 CaCl2 NHCO3 MgCl2 |
| Осмотическое давление, кПа 79 42 25 58 89 67 |
В процессе ультрафильтрации растворенные вещества задерживаются на мембране потому, что размер молекул их больше, чем размер пор, или вследствие трения молекул о стенки пор мембраны.
Для проведения процесса применяются непористые – динамические и диффузионные мембраны, представляющие собой квазигомогенные гели, и пористые мембраны в виде тонких пленок, изготовленные из полимерных материалов. Наибольшее распространение получили полимерные мембраны из ацетатцеллюлозы. Разрабатываются мембраны из полиэтилена, фторированного этиленпропиленового сополимера, политетрафторэтилена, пористого стекла, ацетобутирата целлюлозы и др.
Процесс мембранного разделения зависит от давления, гидродинамических условий и конструкции аппарата, природы и концентрации сточных вод, содержания в них примесей, а также от температуры. Увеличение концентрации раствора приводит к росту осмотического давления растворителя, повышению вязкости раствора и росту концентрационной поляризации, т.е. к снижению проницаемости и селективности.
Обратный осмос рекомендуется использовать при следующей концентрации электролитов: для одновалентных солей – не более 5-10%; для двухвалентных – 10-15%; для многовалентных – 15-20%. Для органических веществ указанные пределы несколько выше. Для уменьшения влияния концентрационной поляризации организуют рециркуляцию раствора и турбулизацию прилегающего к мембране слоя жидкости, применяя мешалки, вибрационные устройства и увеличение скорости.
Конструкция аппаратов для проведения процессов обратного осмоса и ультрафильтрации должна обеспечивать большую поверхность мембран в единице объема, простоту сборки и монтажа, механическую прочность и герметичность. По способу укладки мембран аппараты подразделяются на четыре основные типа: 1) типа фильтр-пресс с плоскопараллельными фильтрующими устройствами; 2) с трубчатыми фильтрующими элементами; 3) с рулонными или спиральными элементами; 4) с мембранами в виде полых волокон.
Используя обратный осмос и ультрафильтрацию, можно концентрировать и разделять растворенные совместно в сточной воде органические и неорганические вещества.
Блок-схема установки разделения органических и неорганических веществ.
 |
Основные параметры – концентрацию растворенных веществ в концентрате и фильтрате необходимо определять на единицу ширины мембраны при заданных ее длине и разделяющей способности при заданных давлении и расходах исходной воды, фильтрата и концентрата при начальной концентрации С0 по следующим зависимостям:
qф = BHL
qвых = q0-qф
Свых = С0(q0/qвых)φ,
где В – коэффициент проницаемости мембран, л/(м·с·Па); Н – давление, Па; L – длина мембраны, м; φ – разделяющая способность, %; q0, qф и qвых – расходы соответственно исходной воды, фильтрата и концентрата, л/с.
4.6. Десорбция, дезодорация и дегазация
Десорбция летучих примесей. Многие сточные воды загрязнены летучими неорганическими и органическими примесями, сероводородом, диоксидом серы, сероуглеродом, аммиаком, диоксидом углерода и др.
При пропускании воздуха или другого инертного малорастворимого в воде газа (азот, диоксид углерода, топочные дымовые газы и др.) через сточную воду летучий компонент диффундирует в газовую фазу. Десорбция обусловлена более высоким парциальным давлением[1] газа над раствором, чем в окружающем воздухе. Равновесное парциальное давление удаляемого газа находят по закону Генри. Количество вещества М, перешедшего из жидкой фазы в газовую, определяют по уравнению массопередачи:
М = Ку F Δср,
где Ку – коэффициент массопередачи (в данном случае он равен коэффициенту массоотдачи в газовой фазе βу); F – поверхность контакта фаз; Δср – средняя движущая сила процесса десорбции.
Процесс десорбции веществ из сточных вод инертными газами может быть проведен в тарельчатых, насадочных и распылительных колоннах. Наиболее интенсивно для тарельчатых колонн он протекает в пенном режиме, а для насадочных – в режиме эмульгирования. Для проведения процесса могут быть использованы колонны с колпачковыми, ситчатыми, клапанными, провальными и другими тарелками.
Степень удаления летучих веществ из сточных вод увеличивается с ростом температуры газожидкостной смеси, коэффициента массоотдачи и поверхности контакта фаз. Десорбируемое из воды вещество направляют на адсорбцию или каталитическое сжигание.
При небольших количествах отделяемого вещества и небольшой его стоимости, а также при условии трудного извлечения его из газовой фазы проводят каталитическое окисление. В этом случае воздух с парами извлекаемого вещества после колонны при температуре 280-350ºС пропускают через слой катализатора (пиролюзит, оксид хрома и др.). Большинство органических соединений в этом случае окисляется до СО2 и Н2О.
Дезодорация. В некоторых сточных водах содержатся меркаптаны, амины, аммиак, сероводород, альдегиды, углеводороды, которые придают им дурной запах. Для очистки дурнопахнущих сточных вод можно использовать различные способы: аэрацию, хлорирование. Ректификацию, дистилляцию, обработку дымовыми газами. Окисление кислородом под давлением, озонирование, экстракцию, адсорбцию и микробиологическое окисление. При выборе метода необходимо учитывать его эффективность и экономическую целесообразность.
Наиболее эффективным считается метод аэрации, который заключается в продувании воздуха через сточную воду. Для очистки на 85-90% необходимо иметь удельный расход 12-15 м3 на 1 м3 сточной воды.
На некоторых предприятиях дурнопахнущие сточные воды очищают продувкой острым паром. В целлюлозной промышленности воды загрязнены серосодержащими соединениями, а, кроме того, метанолом и скипидаром. Отдувка паром позволяет очищать воду и от этих веществ. Основным аппаратом для обработки сточных вод паром является колонна с колпачковыми или сетчатыми тарелками. Степень очистки от сероводорода и метилмеркаптана приближается к 100%, от других веществ – к 90%.
Промышленное применение имеет и хлорирование дурнопахнущих сточных вод. При этом происходит окисление хлором серосодержащих соединений.
Очистку сточных вод от сероводорода можно осуществлять окислением кислородом воздуха при атмосферном давлении в присутствии катализатора (железная стружка, графитовые материалы и др.), которую производят в аэрационном бассейне. Большая часть сероводорода при этом окисляется до элементарной серы, а другая отдувается воздухом. Вода очищается от серы, а воздух с сероводородом поступает на очистку в адсорбер с активным углем.
Для удаления запахов из сточных вод могут быть использованы процессы озонирования и адсорбции. Однако более эффективно происходит очистка при одновременном введении в воду озона или диоксида хлора и фильтровании воды через слой активного угля. Степень дезодорации зависит от их концентрации в сточной воде и изменяется от 80 до100%. Доза озона в этом случае снижается по сравнению с просто озонированием. Применение диоксида хлора вместо озона при тех же соотношениях обеспечивает степень дезодорации на 90-100%.
Дегазация. Присутствие в сточных водах растворенных газов затрудняет очистку и использование сточных вод, усиливает коррозию трубопроводов и аппаратуры, придает воде неприятный запах. Растворенные газы из воды удаляют дегазацией, которую осуществляют химическими, термическими и десорбционными (аэрационными) методами.
Для удаления из воды диоксида углерода используют методы аэрации, проводимые в пленочных, насадочных, барботажных и вакуумных дегазаторах.
Пленочные дегазаторы – колонны с различного типа насадками, работающие в условиях противотока дегазируемой воды и воздуха, подаваемого вентилятором.
Вакуумные дегазаторы – насадочные колонны, работающие под вакуумом, в которых вода равномерно распределяется по поверхности насадки. Наиболее полная дегазация достигается при разбрызгивании в вакууме и одновременном подогреве воды.
При термической дегазации воды от растворенного диоксида углерода или кислорода пропускают пар через воду и нагревают ее до температуры кипения при внешнем давлении.
Аммиак из сточных вод удаляют продувкой водяным паром или воздухом. Ионы аммония в воде находятся в равновесном состоянии с аммиаком и ионами водорода. При рН=7 в воде могут находиться ионы аммония в истинном растворе; при рН=12 – только растворенный аммиак, который можно выделить изводы. Для осуществления процесса отдувки аммиака из воды повышают рН воды до значений 10,8-11,5 и создают большую поверхность контакта между воздухом или паром и водой.
Химические методы дегазации применяют при низкой концентрации газов в воде или в случае нецелесообразности их использования, а также при условии, что продукты обработки не затрудняют дальнейшую очистку или использование воды. Методы связаны с проведением реакций, в результате которых происходит химическое связывание растворенных газов.
Для удаления кислорода ее фильтруют через легкоокисляющиеся стальные стружки. Время контактирования зависит от температуры и при 20-80ºС равно 25-30 мин. Образовавшиеся оксиды железа удаляют обратной промывкой.
При обработке воды сульфитом натрия образуется сульфат натрия. На 1 г О2 необходимо затратить 7,88 Na2SO3.
При обработке диоксида серы в качестве катализатора используют соли меди или кобальта в виде 0,01%-ных растворов. Для удаления 1 г О2 расходуется 4Г SO2.
Лучшим обескислороживающим воду реагентом является гидразин (N2Н4). Реакция протекает значительно быстрее, чем при окислении сульфита. Катализатором служит металлическая медь, стекло, активный уголь. На 1 г кислорода требуется 1 г гидразина. Однако гидразин отличается высокой стоимостью, поэтому метод является дорогим.
4.7. ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ
Для очистки сточных вод от различных растворимых и диспергированных примесей применяют процессы анодного окисления и катодного восстановления, электрокоагуляции, электрофлокуляции и электродиализа. Все эти процессы протекают на электродах при пропускании через сточную воду постоянного электрического тока. Электрохимические методы позволяют извлекать из сточных вод ценные продукты при относительно простой автоматизированной технологической схеме очистки, без использования химических реагентов. Основным недостатком этих методов является большой расход электроэнергии. Очистку сточных вод электрохимическими методами можно проводить периодически или непрерывно.
Эффективность электрохимических методов оценивается следующими факторами: плотностью тока, напряжением, коэффициентом полезного использования напряжения, выходом по току, выходом по энергии. Плотность тока – это отношение тока к поверхности электрода (А/м2, А/см2, А/дм2). Напряжение электролизера складывается из разности электродных потенциалов и падения напряжения в растворе.
Отношение ηнапр = (lа - lк)U называют коэффициентом полезного использования напряжения, где lа и lк – равновесные потенциалы анода и катода, U – напряжение электролизера.
Выход по току – это отношение теоретически необходимого количества электричества (находят по закону Фарадея), к практически затраченному, которое выражают в долях единицы или в процентах.
4.7.1. Анодное окисление и катодное восстановление
|
| ||||
 | |||||
Схема электролизера: 1- корпус; 2- анод; 3- катод; 4- диафрагма.
В электролизере на положительном электроде – аноде ионы отдают электроны, т.е. протекает реакция электрохимического окисления; на отрицательном электроде – катоде происходит присоединение электронов, т.е. протекает реакция восстановления.
Эти процессы разработаны для очистки сточных вод от растворенных примесей (цианидов, роданидов, аминов, спиртов, альдегидов, нитросоединений, азоткрасителей, сульфидов, меркаптанов и др.). В процессе электрохимического окисления вещества, находящиеся в сточных водах, полностью распадаются с образованием СО2, NH3 и воды или образуются более простые и нетоксичные вещества, которые можно удалять другими методами.
В качестве анодов используют электролитически нерастворимые материалы: графит, магензит, диоксиды свинца, марганца и рутения, которые наносят на титановую основу.
Катоды изготовляют из молибдена, сплава вольфрама с железом или никелем, из графита, нержавеющей стали и других металлов, покрытых молибденом, вольфрамом или их сплавами. Процесс проводят в электорлизерах с диафрагмой или без нее. Кроме основных процессов электроокисления и восстановления, одновременно могут протекать электрофлотация, электрофорез, и электрокоагуляция.
Сточные воды, содержащие цианиды, образуются на предприятиях машиностроения, приборостроения, черной и цветной металлургии, химической промышленности и др. В состав вод кроме простых цианидов (KCN, NaCN) входят комплексные цианиды цинка, меди, железа и других металлов, концентрация которых колеблется от 10 до 600 мг/л. Обычно рН таких стоков колеблется в пределах 8-12.
Анодное окисление цианидов протекает по реакциям
+ 2OH—2e → CNO- + Н2О,
CNO- + 2 Н2О → NH4 + СО32-.
Окисление может быть проведено и с образованием азота:
2CNO-+4OH- - 6e → CO2 + N2 + 2 Н2О.
|
|
 |
 |
Принципиальная схема установки для электрохимической очистки сточных вод от цианистых соединений: 1 – подача сточной воды; 2 – сборный резервуар-усреднитель; 3 – бак для приготовления концентрированного раствора хлорида натрия; 4 – электролитическая ванна; 5 – подача воздуха; 6 – регулировочный реостат; 7 – источник постоянного электрического тока; 8 – сброс в канализацию; 9 – обводная линия для подачи воды на повторную очистку.
Роданиды разрушаются по схеме
CNS- + 10 OH- - 8e→ CNO- SO42- + 5Н2О
Сульфид- ионы при рН=7 окисляются до сульфатов. При меньших значениях рН может образоваться элементарная сера.
Катодное восстановление применяют для удаления из сточных вод ионов металлов с получением осадков, для перевода загрязняющего компонента в менее токсичные соединения или в легко выводимую из воды форму (осадок, газ). Его можно использовать для очистки сточных вод от ионов тяжелых металлов Pb2+, Sn2+, Hg2+,Cu2+, As3+, Cr6+. Катодное восстановление металлов происходит по схеме
Men+ + ne-→ Ме0.
При этом металлы осаждаются на катоде и могут быть рекуперированы. Например, при восстановлении соединений хрома была достигнута высокая степень очистки: концентрация снижалась с 1000 до 1 мг/л. Расход электроэнергии на очистку составил 0,12 кВт.ч/м3. При электролизе сточных вод, содержащих Cr2O72-, оптимальное значение рН=2, а плотность тока 0,2-2,0 А/дм2. Реакция восстановления протекает следующим образом:
Cr2O72- + 14Н+ + 12е→ 2Cr3+ + 7Н2О.
Очистку сточных вод от ионов Pb2+, Cd2+, Hg2+,Cu2+ проводят на катодах, состоящих из смеси угольного и сернистого порошков в соотношении C: S от 80:20 до 20:80 при рН<7 и плотности тока 2,5 А/дм2. Осаждение этих ионов происходит в виде нерастворимых сульфидов или бисульфидов, которые удаляют механически.
Примером реакции, обеспечивающей удаление загрязнения в газовую фазу, является очистка от нитрата аммония. При восстановлении нитрата аммония на графитовом электроде он превращается в нитрит аммония, который разлагается при нагревании до элементарного азота.
Процессы анодного окисления используются также для обесцвечивания сточных вод от различных красителей, а также очистки сточных вод целлюлозно-бумажных, нефтеперерабатывающих, нефтехимических и других заводов.
4.7.2. Электрокоагуляция.
Для очистки промышленных сточных вод, содержащих высокоустойчивые загрязнения, проводят электролиз с использованием растворимых стальных или алюминиевых анодов. Под действием тока происходит растворение металла, в результате в воду переходят катионы железа или алюминия, которые, встречаясь с гидроксидными группами, образуют гидроксиды металлов в виде хлопьев. Наступает интенсивная коагуляция.
На процесс электрокоагуляции оказывает влияние материал электродов, расстояние между ними, скорость движения сточной воды между электродами, ее температура и состав, напряженность и плотность тока. С повышением концентрации взвешенных веществ более 100 мг/л эффективность электрокоагуляции снижается. С уменьшением расстояния между электродами расход энергии на анодное растворение металла уменьшается. Теоретический расход электроэнергии для растворения 1 г железа составляет 2,9 Вт.ч, а 1г алюминия – 12 Вт.ч. Электрокоагуляцию рекомендуют проводить в нейтральной или слабощелочной среде при плотности тока не более 20 мм и скорости движения не менее 0,5 м/с.
Достоинства метода электрокоагуляции: компактность установок и простота управления, отсутствие потребности в реагентах, малая чувствительность к изменениям условий проведения процесса очистки (температура, рН среды, присутствие токсичных веществ), получение шлама с хорошими структурно- механическими свойствами. Недостатком метода является повышенный расход металла и электроэнергии. Электрокоагуляция находит применение в пищевой, химической и целлюлозно-бумажной промышленности.
Электрокоагуляционную очистку сточных вод можно использовать для очистки от эмульсий нефтепродуктов, масел, жиров (электрокоагулятор представляет собой ванну с электродами). Эффективность очистки от нефтепродуктов составляет: от масел 54-68%, от жиров 92-99% при удельном расходе электроэнергии 0,2-3,0 Вт.ч/м3.
На практике наиболее широко используют безнапорные пластинчатые электрокоагуляторы, направление движения жидкости в которых может быть горизонтальным и вертикальным. Они могут быть однопоточными, многопоточными и смешанными.
Полезный объем ванны электрокоагулятора (объем сточных вод, постоянно находящихся в аппарате) равен: Vп = Qτ.
Расход железа на процесс: GFe = dcVп.
Ток, обеспечивающий растворение железа за время τ, равен: I = GFe/k τ.100/η.
Рабочая поверхность анодов и общее их число определяют из соотношений
S=I/i, n=S/S1/
Общее число электродов (катодов и анодов) составляет: Nэ = 2na + 1
Общий объем ванны электролизера равен: Vэл = Vп + Vэ,
где Q – расход сточных вод, м3/ч; τ – время процесса, ч; d – удельный расход железа на удаление определенного загрязнения, г/ч; с- исходная концентрация иона металла, загрязняющего воду, г/м3; k – электрохимический эквивалент железа, равный 1,042 г/(А.ч); η – выход железа по току, % (при обработке воды с рН = 3-5 близок к 100%); i – оптимальная плотность тока, А/м2; S1 – площадь одного анода, м2; Vэ – объем всех электродов.
Толщину электродов, их ширину, межэлектродное расстояние определяют с учетом конструктивных особенностей, а также заданной скорости движения воды.
4.7.3. Электрофлотация.
В этом процессе очистка сточных вод от взвешенных частиц проходит при помощи пузырьков газа образующихся при электролизе воды. На аноде возникают пузырьки кислорода, а на катоде – водорода. Поднимаясь в сточной воде, эти пузырьки флотируют взвешенные частицы. При использовании растворимых электродов происходит образование хлопьев коагулянтов и пузырьков газа, что способствует более эффективной флотации.
Основную роль при электрофлотации играют пузырьки, образующиеся на катоде. Диаметр пузырьков меняется от 20 до 100 мм. Для получения пузырьков требуемого размера необходим правильный подбор материала, диаметра проволоки катода и плотности тока. Оптимальное значение плотности тока 200-260 А/м2, газосодержание – около 0,1%.
При небольших объемах сточных вод (10-15 м3/ч) электрофлотационные установки могут быть однокамерными, при больших – следует применять двухкамерные установки, которые могут быть горизонтальными и вертикальными. Они состоят из электродного отделения и отстойной части.
|
|


 Схема однокамерной электрофлотационной установки (1 – корпус;2-электрофлотатор)
Схема однокамерной электрофлотационной установки (1 – корпус;2-электрофлотатор)
 | |||||||
 | |||||||
 | |||||||
 | |||||||
При очистке сточных вод в электрокоагуляторах с последующей электрофлотацией принимают следующие расчетные параметры электрофлотатора:
Расположение электродов горизонтальное
Материал:
анода графит или ОРТА
катода стальная стружка
Продолжител
<== предыдущая лекция
|
следующая лекция ==>
Отстойники | Цели организации. Цели и ресурсы организации
Дата добавления: 2014-01-07; Просмотров: 1124; Нарушение авторских прав?; Мы поможем в написании вашей работы!