
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Вимоги до осадів в кількісному аналізі
Методи фазового розділення елементів.
Окрім процесів осадження або утворення твердої фази, які найбільш розповсюдженні, для розділення елементів в аналізі (і технології) застосовуються й інші методи фазового розділення.
Фазою називається частина системи, яка відокремлена від інших її частин певною поверхнею розділу.
Гази змішуються між собою і тому утворюють одну фазу. Тому розділення суміші газів (без зрідження або поглинання рідкими або твердими сорбентами) в кількісному аналізі не застосовуються. А от утворення газової фази з розчину в ході аналізу, навпаки застосовується досить часто. Згадаймо, що в якісному аналізі ми мали справу з виділенням NH3 (визначення NH4+), CO2 (CO32-), H2S (S2-), SO2 (SO32-) та інших газів. Завдяки специфічності та деяким іншим особливостям реакції виділення газоподібних речовин мають велике значення і в кількісному аналізі. Вміст води в різноманітних продуктах визначають звичайно видаленням її у вигляді пари. Кількість води обчислюють за втратою маси; іноді пару поглинають придатною для цього речовиною, і кількість води визначають по збільшенню маси цієї речовини. Реакції утворення газоподібних продуктів застосовують в аналізі карбонатних порід, при визначенні вуглецю в сталі, аміаку в добривах, аміногруп в білкових речовинах, в інших випадках.
Виділення компоненту у вигляді рідкої фази має найбільше значення при здійсненні екстракції. Екстракцією або екстрагуванням називають такий метод, яким речовина, що знаходиться у водному розчині, вилучається за допомогою органічного розчинника. Останній не розчиняється у воді і, отже, утворює іншу фазу. В якісному аналізі при визначенні йоду і брому вже застосовувалась їх екстракція бензолом і катіонів кобальту у вигляді роданідного комплексу ізоаміловим спиртом (реакція ”синього кільця”).
На відміну від методів осадження, екстрагування застосовується в кількісному аналізі частіш за все для відокремлення тієї чи іншої речовини, після чого відбувається її реекстракція, а визначення виконується іншим методом, звичайно колориметричним або об’ємним.
Отже, ми дійшли висновку, що основним способом фазового розділення в кількісному, особливо ваговому методі аналізу, є утворення твердої фази з розчину, тобто осадження.
Багато погано розчинних сполук, які використовуються в якісному аналізі, виявляються непридатними для кількісного аналізу. Так, не можна застосовувати для кількісного аналізу реакцію “золотого дощу”, оскільки йодид свинцю помітно розчинний навіть у холодній воді: 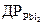 дорівнює 1,1·10-9, що відповідає розчинності Pb2+:
дорівнює 1,1·10-9, що відповідає розчинності Pb2+:
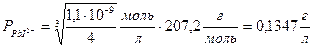
Ця розчинність є неприпустимо великою і призводить до значних похибок у зв’язку з втратою свинцю в маточному розчині
Інші осади, наприклад, Fe4[Fe(CN)6]3 i Fe2[Fe(CN)6]3, хоча і дуже малорозчинні, визначаються тим недоліком, що не мають постійного складу. Ці сполуки є подвійними солями зі змінною кількістю калію і заліза. Тому за масою такого осаду неможливо обчислити кількість заліза. Крім того, ці та деякі інші осади, часто утворюють колоїдні розчини, що також неприйнятно для кількісного аналізу.
Розглянуті приклади показують, що в кількісному аналізі осади повинні відповідати наступним вимогам.
а) Осад повинен бути практично нерозчинним.
Для визначення чисельного значення допустимої границі необхідно враховувати основні умови вимірів. Чутливість звичайних аналітичних терезів дорівнює 0,0001г (10-4г), а порядок величин молекулярних мас більшості осадів складає 100. Отже, допустима похибка в молях складає:
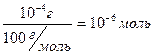
Об’єм рідини при осадженні складає звичайно 200-400мл, на промивання осаду витрачається ще 100-150мл розчину. Отже у крайньому випадку можна прийняти максимальний об’єм рідини, що знаходиться в рівновазі з осадом, рівним 1л. Тоді одержимо, що в звичайних умовах вагового аналізу необхідна і достатня межа розчинності дорівнює 10-6 моль/л. Цю загальну вимогу до осадів вивів Тананаєв, і воно відома як правило його.
б) Склад осаду після висушування або прожарювання повинен відповідати певній формулі, тобто бути сталим. В іншому випадку неможливими стають обчислення.
в) Молекулярна маса речовини осаду повинна бути по можливості великою. Це підвищує точність аналізу.
г) Осад повинен одержуватись у формі, зручній для відокремлення його від розчину фільтруванням.
Здійснення вимог б) і г) досягається шляхом дотримання певних умов осадження і термообробки, про що йтиметься у наступних розділах.
|
|
Дата добавления: 2014-01-07; Просмотров: 407; Нарушение авторских прав?; Мы поможем в написании вашей работы!