
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кислотные свойства
Химические свойства карбоновых кислот
Физические свойства предельных одноосновных карбоновых кислот
Первые три члена ряда С-С3 – подвижные бесцветные жидкости со жгучим запахом, смешиваются с водой. С4 и далее – маслянистые жидкости с запахом прогорклого масла, с водой не смешиваются, ратсворимость уменьшается с увеличением молекулярного веса. Неустойчивы к нагреванию. С1-С9 – жидкости; С10 и более – твердые вещества. Температуры кипения кислот высокие. У муравьиной кислоты – 1000С, дальше – еще выше. Это объясняется тем, что карбоновые кислоты образуют за счет водородных связей димеры, сохраняющиеся даже при кипении.
O…….H-O
СH3-C C-CH3
O-H…….O
а) Диссоциация в водном растворе
O O
R-C  R-C + H+
R-C + H+
O-H O-
По степени диссоциации – это слабые кислоты. Наиболее сильная – муравьиная кислота. У других кислот углеводородный радикал, обладающий электродонорными свойствами, отталкивает электроны к водороду (положительный индукционный эффект), и кислотность снижается.
HCOOH Кд=2,14.10-4
CH3 C
C O
O H Кд=1,75.10-5
H Кд=1,75.10-5
О
Степень диссоциации увеличивается при введении в радикал электроноакцепторных групп, например, групп С=О, ОН, Cl. Чем ближе эти группы расположены к СООН, тем сильнее кислота. Например, у хлоруксусной кислоты
Cl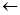 CH2
CH2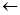 C
C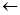 OH Кд=1,5.10-3
OH Кд=1,5.10-3
О
у трихлоруксусной
Cl
Cl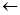 C
C C-O-H Кд=2,1.10-1
C-O-H Кд=2,1.10-1
Cl
т.е. трихлоруксусная кислота аналогична сильным минеральным кислотам.
2) Образование солей происходит при взаимодействии с металлами, окисями, гидроокисями металлов, с некоторыми другими солями и аммиаком
а) 2HCOOH + Mg  H2 + (HCOO)2Mg
H2 + (HCOO)2Mg
формиат магния
б) 2СH3COOH + CaO  (CH3COO)2Ca + H2O
(CH3COO)2Ca + H2O
ацетат кальция
в) С2H5COOH + NaOH  H2O + C2H5COONa
H2O + C2H5COONa
пропионат натрия
г) CH3COOH + NaHCO3  CH3COONa + CO2 + H2O
CH3COONa + CO2 + H2O
д) CH3COONa + AgNO3  CH3COOAg + NaNO3
CH3COOAg + NaNO3
е) CH3COOH + NH3  [CH3COO-]N+H4
[CH3COO-]N+H4
3) Образование производных карбоновых кислот путем замещения гидроксила (реакции ацилирования)
а) Образование хлорангидридов кислот
O O
CH3-C + PCl5  CH3-C + POCl3 + HCl
CH3-C + POCl3 + HCl
OH Cl
(или PCl3 хлорангидрид уксусной кислоты
SOCl2) (хлористый ацетил)
б) Образование амидов карбоновых кислот
O O
CH3-C + NH3  CH3-C + H2O
CH3-C + H2O
OH NH2
O O
CH3-C + NH3  CH3-C + HCl
CH3-C + HCl  NH4Cl
NH4Cl
Cl NH2
в) Образование сложных эфиров со спиртами (см. свойства спиртов)
|
Дата добавления: 2014-01-06; Просмотров: 359; Нарушение авторских прав?; Мы поможем в написании вашей работы!