
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Правило відрізків
|
|
|
|
Діаграми стану, їхнє значення.
3. Діаграми склад-властивості (Курнакова - Матисена).
1. Усі перетворення, що протікають в сплавах у залежності від температури і концентрації, можна зобразити наочно, що здійснюється на діаграмах стану. Діаграма стану - це графічне зображення фазового стану сплавів даної системи в залежності від температури та концентрації.
Діаграми стану дають у наочній формі картину зміни будови і властивостей сплаву при зміні його концентрацій і температури, дозволяють визначити температури плавлення, твердіння й алотропічних перетворень у сплавах, вивчити походження структур, що спостерігаються під мікроскопом, і зв’язати структуру сплаву з його механічними, технологічними і фізико-хімічними властивостями.
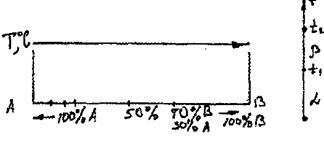 У залежності від характеру взаємодії компонентів сплавів у твердому стані розрізняють 4 основних типи діаграм стану подвійних сплавів. Діаграми стану подвійних сплавів будують у двох вимірах: по осі ординат відкладають температуру, по осі абсцис - концентрацію у вагових %(мал..15).
У залежності від характеру взаємодії компонентів сплавів у твердому стані розрізняють 4 основних типи діаграм стану подвійних сплавів. Діаграми стану подвійних сплавів будують у двох вимірах: по осі ординат відкладають температуру, по осі абсцис - концентрацію у вагових %(мал..15).
Мал. 15 Загальний вміст обох компонентів у сплаві дорівнює 100%. і кожна точка на осі абсцис відповідає певному вмісту кожного компонента. По мірі віддалення від точки А збільшується кількість компонента В і в точці В=100%. Кожна точка на діаграмі стану показує стан сплаву даної концентрації при даній температурі. Звичайно діаграми стану будують експериментально. Для визначення температур фазових переходів застосовують термічний аналіз. При цьому одержують експериментальні криві охолодження і по перегинах, які зв'язані з тепловими ефектами перетворень, визначають критичні температури (точки). Для дослідження перетворень, які проходять у сплаві у твердому стані застосовують рентгено - і мікроструктурний, магнітний і інші методи. Діаграми, на яких зображені фази в сплаві (тверді розчини, хімічні з’єднання чи механічні суміши), називають фазовими. Але, при вивченні будови сплавів під мікроскопом спостерігаються як фази, так і структурні складові сплаву, котрі мають певний розмір, форму та розташування. Діаграмами стану, в яких показані структурні складові, отримали назву структурні. Мікробудова сплаву обумовлює їх фізико-механічні, технологічні та експлуатаційні властивості. Розглянемо діаграму стану двохкомпонентних сплавів для випадків, коли обидва компонента нескінченно розчинні у жидком стані, а у твердому стані не розчинні, створюють механічну суміш. Такі діаграми умовно називають діаграми стану першого типу. Компонентами А і В, що складають розглянутий сплав, можуть служити як чисті елементи, так і хімічні сполуки. Криві охолодження компонентів і сплавів різних складів зображені на малюнку ліворуч і праворуч від діаграми.
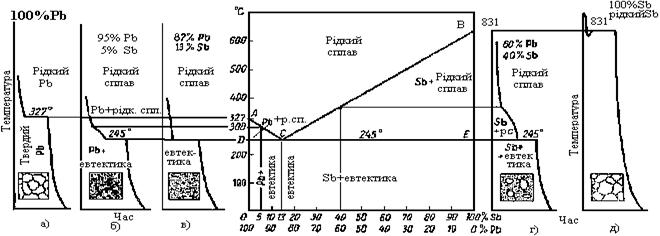 |
Мал. 16
На відміну від чистих компонентів, усі сплави за невеликим винятком кристалізуються в інтервалі температур. Причому, спочатку кристалізується тільки один з компонентів, тому що спільна кристалізація компонентів у випадку утворення механічної суміші можлива тільки при визначеній їх концентрації в розплаві. У нашому випадку такою концентрацією є 13% олова і 87% свинцю. При такій концентрації спільна кристалізація протікає при постійній температурі аналогічно кристалізації чистого компоненту. У сплавах, що відрізняються за складом від сплаву зі 13% олова спочатку кристалізується тільки один з компонентів: Pb - у випадку якщо концентрація Sn у сплаві менша 13%; i Sn – якщо концентрація Sn в сплаві більша 13%, при кристалізації надлишкового компоненту його рідкої фази все більше наближається до концентрації при якій можлива одночасна кристалізація обох компонентів тобто до 13% Sn і 87% Pb. Процес кристалізації будь-якого сплаву даної системи завершується одночасним утворенням кристалів речовин А(Pb) і В(Sn). При спільній кристалізації утворюється дисперсна суміш найдрібніших дендритів речовини В і кристалів речовини А, в товщі яких вони залягають. Такі суміші називають евтектиками. Це сплави утворені в результаті одночасної кристалізації різних компонентів при постійній температурі. Евтектики мають постійний хімічний склад і найнижчу температуру кристалізації для даної системи сплавів. Крива кристалізації евтектичного сплаву буде мати такий же вигляд, як і крива кристалізації чистого компонента. У сплавах заевтектичних (>13%Sn), спочатку кристалізується компонент В. При зменшенні концентрації компонента В у рідкій фазі до 13% в кристалізацію вступає також і компонент А, що призводить до утворення евтектики. Критичні точки початку і кінця кристалізації переносять з кривих охолодження на діаграму, де по вісі ординат - температура, по вісі абсцис – склад сплаву. Точки початку і кінця кристалізації з’єднують плавними лініями і одержують діаграму стану. Верхня ламана лінія АСВ відповідає початку кристалізації (кінець плавлення) і називається лінія ліквідус, лінія ДСЕ відповідає
кінцю кристалізації (початок плавлення) і називається лінією солідуса. Вище ліквідуса - сплави в рідкому стані. Між ліквідусом і солідусом йде процес кристалізації, і сплави складаються з твердої та рідкої фаз. Нижче лінії солідуса сплави складаються
з різних твердих фаз. Якщо компоненти сплавів значно відрізняється за густиною, то кристали які виділяються, будуть нерівномірно розподілені в рідкому сплаві. Більш важкі кристали осаджуються на дні форми. До моменту повної кристалізації евтектика виявляється переважно зверху, кристали більш важкого надлишкового компоненту знизу. В результаті хімічний склад в різних об’ємах злитку чи виливки буде не однорідним. Це явище носить назву ліквації за густиною (питомою вагою). Усунути її можна розмішуючи або струшуючи сплав який затвердіває. Сплави близькі за складом до евтектичного широко застосовуються в техніці через низьку температуру плавлення і кращі ливарних властивостей. Кількість і склад фаз у процесі кристалізації можна визначити по правилу відрізків (мал.19). Для визначення хімічного складу фаз через точку, що характеризує сплав, проводять горизонтальну пряму до перетину з найближчими лініями діаграми, при цьому проекція точок перетину на вісь абсцис покаже хімічний склад фаз. Кількісне співвідношення між масою рідкої фази і масою твердої фази визначається співвідношенням відрізків КL і NL. Користаючись концентраційними відрізками на осі абсцис можна знайти необхідну величину
Qр /Qтв =КL/NL
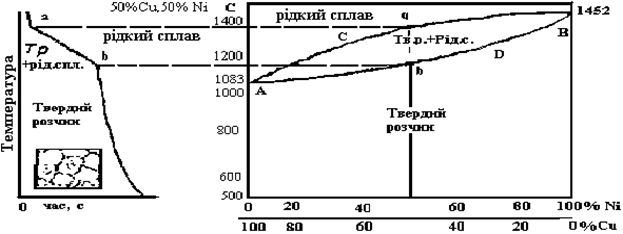 |
 Діаграма стану другого типу для випадку необмеженої розчинності компонентів у твердому стані. У цьому випадку кожен кристал будується сумісно
Діаграма стану другого типу для випадку необмеженої розчинності компонентів у твердому стані. У цьому випадку кожен кристал будується сумісно
атомами обох речовин і тому в
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 987; Нарушение авторских прав?; Мы поможем в написании вашей работы!