
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Кристалічна решітка
|
|
|
|
МОДЕЛЬ КОВАЛЕНТНОГО ЗВ'ЯЗКУ
Залежно від структурних особливостей твердих тіл прийнято розрізняти:
аморфні речовини, що не мають якої-небудь певної структури;
полікристалові речовини, що складаються з окремих гранул або малих областей. Кожна гранула має чітко виражену структуру, проте розміри і орієнтація гранул в сусідніх областях абсолютно довільні;
монокристалічні речовини, атоми яких просторово впорядковані і утворюють тривимірну періодичну структуру, звану кристалічною решіткою.
Для забезпечення необхідних властивостей напівпровідникові пристрої і інтегральні схеми виконують з монокристалів, серед яких найбільше значення мають монокристали кремнію (Si); даний напівпровідниковий матеріал в даний час використовують найчастіше. Проте будь-який монокристал неминуче містить ті або інші дефекти структури, які роблять істотний вплив на процеси перенесення носіїв заряду. Такі дефекти (наприклад, вакансії, включення, дислокації і межі) виникають в процесі вирощування монокристала, а також можуть бути слідством недостатньо високої якості технології.
Основну роль в процесі об'єднання атомів в кристал грають електрони. Міжатомний зв'язок виникає завдяки тому, що атоми в речовині розташовані близько один до одного. Розрізняють іонну, металеву і ковалентну зв'язку.
При іонному зв'язку електрони переміщаються від одних атомів до інших. Як наслідок, в структурі виникають іони. При металевому зв'язку кристалічна решітка з позитивно заряджених іонів оточена «електронним газом». Нарешті, у разі ковалентного зв'язку зовнішні, так звані валентні, електрони стають загальними для найближчих сусідніх атомів. У твердих тілах з ковалентним зв'язком утворюються різні кристалічні решітки, вид яких визначається кутами між напрямами різних ковалентних зв'язків.
Багато властивостей твердих тіл пояснюються тією періодичністю, з якою розміщені в просторі їх структурні елементи. Тому доцільно розглянути важливе поняття, зване кристалічною решіткою.
У періодичній кристалічній решітці можна виділити деякий елементарний осередок, який повторюється періодично по всьому кристалу. Виділяючи такий осередок, вдається описати положення атомів або іонів в речовині, і, отже, вона може служити для того, щоб з її допомогою характеризувати структуру кристалів. Положення, займані атомами або іонами, відповідають точкам (вузлам) грат. У напівпровідниках елементарний осередок полягає всього лише з декількох атомів. Просторово вона дуже мала і може бути розміщена усередині куба із стороною близько 0,5 нм.
Слід відмітити, що елементарний осередок не обов'язково співпадає з так званим примітивним осередком, який, за визначенням, є областю мінімального об'єму, грат, що містять один вузол.
Серед всіляких видів грат можна виділити кубічні грати, що мають декілька різновидів.
• Прості кубічні грати. У кожній вершині таких грат розташовується один атом, що належить одночасно восьми сусіднім елементарним осередкам (мал. 2.1, а). У такій формі кристалізується лише полоний (Ро).
• Кубічні об’ємноцентровані грати. Тут крім атомів у вершинах кубів є ще один атом в центрі (мал. 2.1,6). До даного типа відносяться кристалічні решітки молібдену і вольфраму.
• Кубічні гранецентрировані грати. Має шість атомів в центрах граней і, крім того, вісім атомів у вершинах куба (мал. 2.1, в). У такій формі кристалізується алюміній і ряд інших хімічних елементів.
• Грати типу алмазу. Може розглядатися як двоє вкладених один в одного кубічних гранецентрированих грат, зміщені на відстані чверті діагоналі куба (на мал. 2.1, г темними і світлими кухлями зображені одні і ті ж атоми). У даній формі кристалізуються вуглець, кремній, германій і сіра модифікація олова.
• Грати типу арсеніду галію виходять з грат типу алмазу у тому випадку, коли атоми Ga співпадають з вузлами одних гранецентрированих грат, а атоми As —с вузлами іншої (на рис. 1.1, г атоми Ga позначені світлими кухлями, а атоми As — темними).
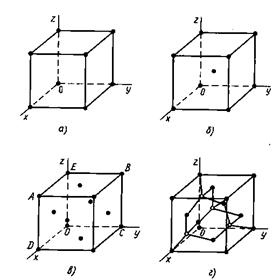
Рис. 1.1. Елементарні осередки кубічних грат.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 480; Нарушение авторских прав?; Мы поможем в написании вашей работы!