
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Основные тепловые эффекты термохимии взрывчатых веществ
|
|
|
|
Количество тепла, выделяющееся или поглощающееся при химических реакциях, зависит только от начального или конечного состояния веществ, участвующих в реакциях, а не от пути, каким вещества перешли из начального в конечное состояние.
Закон Гесса
Оговорка: баланс работы должен быть равен нулю. Обязательным условием при проведении расчетов по закону Гесса является написание уравнения. Кроме того, закон является вполне строгим лишь для процессов, протекающих либо при постоянном давлении, либо при постоянном объеме.
Из вышесказанного видно, что закон Гесса позволяет обращаться с термохимическими уравнениями как с алгебраическими, т. е. складывать и вычитать их, если термодинамические функции относятся к одинаковым условиям.
Например, диоксид углерода можно получить прямым синтезом из простых веществ (I) или в две стадии через промежуточный продукт (II):
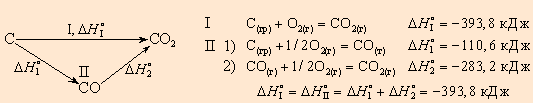
Закон Гесса позволяет очень точно определить тепловые эффекты достаточно сложных изменений системы исходя из других изменений в этой же системе.
Q0обр.пр.сгор.=Q0обр.вещества+Q0сгор.
Например, весьма сложно определить теплоту образования сложных химических соединений. Но если сжечь это вещество и замерить теплоту сгорания, то, зная продукты сгорания и теплоты их образования, можно очень точно рассчитать теплоту образования вещества.
Именно так на практике через теплоту сгорания и определяют теплоты образования сложных веществ.
В теории ВВ приходится иметь дело со следующими тепловыми эффектами: энтальпиями или теплотами образования, сгорания (в кислороде), горения и взрыва.
Стандартная энтальпия образования – тепловой эффект реакции образования одного моля соединения из простых веществ при стандартных условиях. Обозначается ΔН0298(обр).
Принято, что энтальпия образования простых веществ в том состоянии, в котором они находятся при стандартных условиях (атом или молекула, газ или жидкость, твердое) равна нулю.
Теплотой сгорания называют тепловой эффект реакции одного моля или единицы массы данного соединения с кислородом, при котором образуются высшие окислы CO2 и H2O; азот и галоген (за исключением F) выделяются в свободном состоянии (N2,Cl2), сера образует сероводород (H2S). Теплоту сгорания относят к стандартным условиям. Обозначают ΔН0сгор.
Теплоту сгорания можно определить экспериментально с помощью калориметрической установки. При необходимости вносят поправки для того, чтобы тепловой эффект строго соответствовал указанным продуктам сгорания и стандартным условиям.
Важнейшей характеристикой ВВ является теплота взрыва – количество тепла, которое выделяется при взрыве одного моля или единицы массы ВВ.
Теплота взрыва определяет работоспособность, скорость детонации, температуру взрыва, её знание необходимо при составлении уравнений взрывчатого превращения и т.д.
Теплота взрыва может быть вычислена на основании закона Гесса, но для этого необходимо определить теплоту образования ВВ и состав продуктов взрыва, а он значительно отличается от продуктов сгорания этого же вещества.
Если сравнить теплоты взрыва горения и сгорания в кислороде, то для большинства ВВ максимальное количество тепла выделяется при сгорании в кислороде, так как образуются высшие окислы. Наименьшее количество тепла выделяется при взрыве (при детонации). Во-первых, часто не хватает кислорода для образования высших окислов. Во-вторых, процесс очень быстрый и реакции не успевают пройти до конца.
Из сравнения скорости процессов горения и детонации нужно сделать вывод о том, что все расчеты процессов горения выполняют с учетом условия постоянства давления.
Расчеты процессов детонации выполняют при условии постоянства объема. Простейший пересчет можно выполнить по формуле:
QV=QP+(n2-n1)RT
n2, n1 - число молей газообразных исходных и конечных продуктов реакции.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 637; Нарушение авторских прав?; Мы поможем в написании вашей работы!