
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Горение жидкости со свободной поверхности
|
|
|
|
Самой медленной стадией выгорания жидкостей со свободной поверхности также является стадия испарения. У поверхности слоя жидкости всегда существуют пары, количество которых в состоянии равновесия характеризуется парциальным давлением, определяемым давлением насыщения. С ростом температуры жидкости давление насыщения возрастает. При увеличении давления насыщения интенсивность испарения увеличивается.
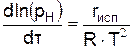 ,
,
где рН – давление насыщенных паров; t – время; rисп – скрытая теплота парообразования; R – газовая постоянная; Т – температура жидкости.
При достижении определённой температуры концентрация паров над поверхностью жидкости будет соответствовать нижнему концентрационному пределу воспламенения в паровоздушной смеси.. Такая температура получила название нижнего температурного предела воспламенения.
Кроме понятия нижнего температурного предела воспламенения существует близкое по смыслу понятие температуры вспышки.
Температура вспышки – это наименьшая температура конденсированного вещества, при которой над его поверхностью образуются пары, способные вспыхивать в воздухе от источника зажигания, устойчивое горение при этом не возникает. Под вспышкой понимают быстрое сгорание паровоздушной смеси над поверхностью горючего вещества, сопровождающееся кратковременным видимым свечением.
При вспышке паровоздушная смесь создаётся ненасыщенными парами, она способна локально воспламениться от источника зажигания. Соотношение между нижним температурным пределом воспламенения и температурой вспышки покажем на графике.
 |
Рис. 14. Зависимость парциального давления паров от температуры
Нагрев жидкости выше температуры вспышки увеличивает скорость испарения. В закрытой ёмкости жидкость может иметь температуру, при которой концентрация паров над слоем создаёт богатую смесь, неспособную к воспламенению. Такую температуру называют верхним температурным пределом воспламенения.
При локальном воздействии источника тепловой энергии на слой жидкости после достижения поверхностью жидкости температуры воспламенения в зоне воздействия происходит зажигание паровоздушной смеси. Возникает пламя, которое с определённой скоростью перемещается по поверхности слоя жидкости.
На значение скорости перемещения влияют начальная температура жидкости, теплота испарения, температура вспышки, интенсивность нагрева.
Увеличение начальной температуры жидкости уменьшает затраты энергии на нагрев. Когда температура жидкости достигает температуры вспышки, скорость распространения пламени резко возрастает. При дальнейшем повышении температуры скорость продолжает возрастать и Тсх становится скоростью распространения пламени в паровоздушной смеси стехиометрического состава. Покажем это на графике
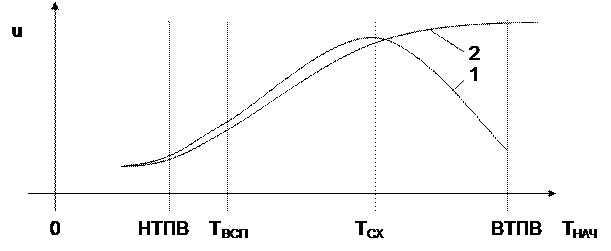 |
Рис. 15. Скорость распространения пламени в зависимости от начальной температуры жидкости 1 – в закрытой ёмкости; 2 – в открытой ёмкости;
Тсх – температура образования смеси стехиометрического состава
Скорость распространения пламени по свободной поверхности изменяется от нескольких миллиметров до нескольких метров в секунду.
После воспламенения жидкости и распространения пламени по её поверхности устанавливается диффузионный режим выгорания горючего вещества.
При установившемся режиме горения массовая скорость выгорания выражается следующей формулой:
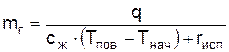 , кг/(м2с);
, кг/(м2с);
где q – плотность потока энергии из зоны горения на поверхность слоя жидкости; сж – удельная теплоёмкость жидкости; Тпов. – температура поверхности жидкости; Тнач – начальная температура жидкости.
К особенностям горения жидких углеводородных веществ со свободной поверхности следует отнести существенный недожог, приводящий к образованию продуктов неполного горения. Испаренные углеводороды в результате нахождения в зоне высоких температур и при отсутствии кислорода подвергаются термическому разложению (пиролизу):
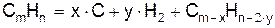
Образуются водород, свободный углерод и новое углеводородное вещество, которое также способно пиролизоваться:
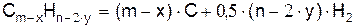
При высоких температурах и наличии окислителя продукты пиролиза выгорают. При недостатке окислителя свободный углерод приводит к образованию угарного газа. При невысоких температурах горения атомы свободного углерода объединяются в мельчайшие частицы сажи и уносятся с газообразными продуктами горения, образуя клубы чёрного дыма.
Рассмотрим горение жидкости, находящейся в резервуаре. Схема горения имеет следующий вид:
 пг
пг
в
пары
ТНАЧ ТКИП ТВ ТГ Т
жидкость х
Рис. 16. Схема горения
Процесс горения жидкости со свободной поверхности слоя проходит через несколько стадий:
1). Под действием потока энергии из зоны горения жидкость нагревается и испаряется;
2). В восходящий поток паров горючего вещества из окружающего пространства посредством диффузии поступает воздух, он перемешивается с парами жидкости и образует паровоздушную смесь.
3). Смесь нагревается, воспламеняется и горит, образуя зону пламени с высокой температурой, генерирующую видимое и инфракрасное излучение.
4). Горячие продукты полного и неполного горения перемешиваются с холодным воздухом, охлаждаются и образуют дым.
Нагрев поверхности сопровождается переносом тепловой энергии в слой жидкости. Прогрев жидкости можно описать следующим уравнением
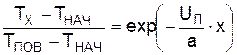
где Тх – температура слоя жидкости на глубине х, ТНАЧ – начальная температура жидкости, а – коэффициент температуропроводности жидкости; UЛ – линейная скорость выгорания жидкости, связанная с массовой скоростью соотношением
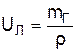 ,
,
где r – плотность жидкости.
Существует три режима горения жидкости со свободной поверхности: ламинарный, переходный и турбулентный.
В ламинарном режиме область горения имеет форму конуса, а в турбулентном она разорвана на множество отдельных очагов. Интенсивность горения в турбулентном режиме существенно выше, чем в ламинарном.
Скорость выгорания в любом режиме горения можно вычислить по следующей формуле
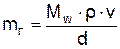 ;
;
r – плотность паров жидкости при температуре кипения, кг/м3;
n – кинематическая вязкость паров при температуре кипения, м2/с;
d – характерный размер поверхности горящей жидкости, м;
Мw –безразмерная скорость выгорания жидкости.
При определении плотности можно воспользоваться формулой
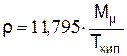 ,
,
Мm – молярная масса, кг/моль; Ткип – температура кипения, К.
Кинематическую вязкость паров можно оценить по формуле
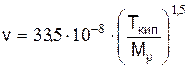
Характерный размер для поверхности горения в форме круга равен диаметру окружности, при другой форме
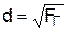 ;
;
где Fг – площадь поверхности горения.
При расчете скорости турбулентного горения d £ 10 м
Режим горения определяется по величине критерия Галилея
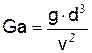 ,
,
где g – ускорение свободного падения.
В ламинарном режиме горения при Ga < 3×106 безразмерная скорость выгорания жидкости определяется по следующей формуле
 ,
,
где А – вспомогательная величина; В – безразмерный параметр, характеризующий интенсивность массопереноса;
Для переходного режима горения
а) при 3×106 £ Ga < 4,8×108
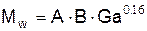
б) при 4,8×108 £ Ga < 3×1012
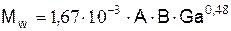
В турбулентном режиме горения при Ga ³ 3×1012
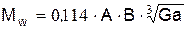
Вспомогательная величина
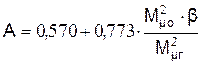
где b – удельный стехиометрический коэффициент реакции горения жидкости; Мmо – молярная масса кислорода; Мmг – молярная масса горючего.
Безразмерный параметр массопереноса
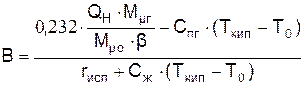
где QH – низшая теплота сгорания жидкости, кДж/кг; Спг – изобарная теплоёмкость продуктов горения жидкости (Спг = 1 кДж/кг/К); Т0 – температура окружающей среды (Т0 = 293 К); rисп – теплота парообразования жидкости при температуре кипения, кДж/кг; Сж – средняя изобарная теплоёмкость жидкости в интервале температур от Т0 доТкип.
12.Горение твёрдых веществ
12.1. Общая характеристика твёрдых техногенных веществ
Твёрдые горючие вещества, обращающиеся в техносфере подразделяются на естественные и искусственные.
К твёрдым горючим веществам естественного происхождения относятся следующие органические вещества: древесина, торф, бурый уголь, каменный уголь, горючие сланцы, продукты растениеводства.
В горючем составе каменного угля содержится:
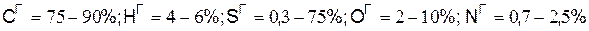
Содержание минеральных веществ АС=10–28%, а влаги Wi = 3–20%.
Вещества органического происхождения подвергают сухой перегонке, например в результате нагрева угля до 1000°С без доступа воздуха получают кокс.
К твёрдым горючим веществам искусственного происхождения относятся:
– продукты сухой перегонки
– термопластические полимеры, в том числе, полиэтилен, полиметилметакрилат, полистирол, поливинилхлорид;
– термоотверждающиеся полимеры, в том числе, пенополиуретан, пенофенопласт;
– термореактивные смолы;
– эластомеры (каучукоподобные вещества);
– парафины;
– неорганические вещества (сера);
– металлы (алюминий).
12.2.Процессы, сопровождающие горение твёрдых веществ
Горение твёрдых материалов сопровождают следующие процессы:
а) нагрев компонентов горючей системы;
б) термическое разложение (пиролиз) макромолекул на простые молекулы, образование летучих и твёрдых веществ;
в) перемещение компонентов горючей системы под действием разности плотностей нагретых и холодных газообразных сред;
г) возгонка;
д) плавление;
е) испарение;
ё) образование в горючей системе газообразной смеси посредством молекулярной и молярной (турбулентной) диффузии;
ж) химическое реагирование с выделением или поглощением тепловой энергии;
з) образование и распространение волн давления.
 Термические превращения сопровождаются фазовыми переходами. Образование газов и паров показано на следующей схеме
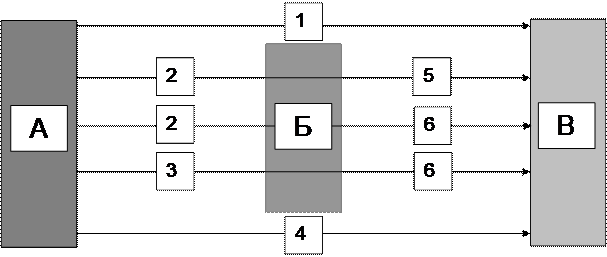
Термические превращения сопровождаются фазовыми переходами. Образование газов и паров показано на следующей схеме
Рис. 17. Схема образования летучих
А – твёрдое вещество; Б – жидкость; В – пары и газы;
1 – сублимация, 2 – плавление, 3 – плавление и разложение, 4 – разложение,
5 – испарение, 6 – разложение и испарение
Примеры термического разложения горючих веществ:
- нафталин при горении сублимируется;
- парафины с низкой молекулярной массой плавятся и испаряются без разложения;
- термопласты и парафины с высокой молекулярной массой плавятся, а затем разлагаются и испаряются;
- пенополиуретан разлагается с образованием расплавленных продуктов, которые продолжают разлагаться с образованием летучих;
- целлюлоза и некоторые смолы разлагаются с непосредственным образованием летучих.
Горение твёрдых веществ может проходит по одной из следующих схем:
5. Схема слоевого горения. На колосниковую решетку топки техногенного устройства подаётся горючее вещество. Через слой вещества продувается воздух. В слое происходит нагрев, термическое разложение, выделение летучих и образование горючей смеси. На выходе из слоя смесь воспламеняется и горит. Нагрев, термическое разложение и зажигание происходит под воздействием тепловой энергией продуктов горения.
6. Схема факельного горения. В объём топки техногенного устройства подаётся горючее вещество в пылевидном состоянии и воздух. Горение пылевоздушной смеси осуществляется в диффузионном факеле подобно факельному сжиганию жидкостей.
7. Схема выгорания с поверхности. Твёрдый конструкционный материал или техногенный продукт локально нагревается от источника зажигания, воспламеняется и горит. Пламя перемещается по поверхности. Происходит выгорание вещества с поверхности.
8. Схема пылевоздушного облака. Горючее вещество в результате техногенного происшествия приводит к возникновению пылевоздушного облака. Смесь локально воспламеняется от источника зажигания. Распространение пламени по объёму облака подобно распространению по паровоздушной или газовоздушной смеси. При особых условиях дефлаграция способна перерасти в детонацию.
|
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 2278; Нарушение авторских прав?; Мы поможем в написании вашей работы!