
КАТЕГОРИИ:
Архитектура-(3434)Астрономия-(809)Биология-(7483)Биотехнологии-(1457)Военное дело-(14632)Высокие технологии-(1363)География-(913)Геология-(1438)Государство-(451)Демография-(1065)Дом-(47672)Журналистика и СМИ-(912)Изобретательство-(14524)Иностранные языки-(4268)Информатика-(17799)Искусство-(1338)История-(13644)Компьютеры-(11121)Косметика-(55)Кулинария-(373)Культура-(8427)Лингвистика-(374)Литература-(1642)Маркетинг-(23702)Математика-(16968)Машиностроение-(1700)Медицина-(12668)Менеджмент-(24684)Механика-(15423)Науковедение-(506)Образование-(11852)Охрана труда-(3308)Педагогика-(5571)Полиграфия-(1312)Политика-(7869)Право-(5454)Приборостроение-(1369)Программирование-(2801)Производство-(97182)Промышленность-(8706)Психология-(18388)Религия-(3217)Связь-(10668)Сельское хозяйство-(299)Социология-(6455)Спорт-(42831)Строительство-(4793)Торговля-(5050)Транспорт-(2929)Туризм-(1568)Физика-(3942)Философия-(17015)Финансы-(26596)Химия-(22929)Экология-(12095)Экономика-(9961)Электроника-(8441)Электротехника-(4623)Энергетика-(12629)Юриспруденция-(1492)Ядерная техника-(1748)
Молекулярно-кинетические представления
|
|
|
|
Молекулярная физика изучает строение вещества, исходя из молекулярно-кинетических представлений, основывающихся на том, что все тела состоят из молекул, находящихся в непрерывном хаотическом движении. Идея об атомном строении вещества высказана впервые древнегреческим философом Демокритом (460 - 370 гг. до н. э.). Во время прогулки по берегу моря он наблюдал увлажнение одежды и пришел к выводу, что тела состоят из мельчайших неделимых частиц - атомов. В течение многих веков учение об атомах запрещалось церковью. Вновь атомистика возрождается лишь в XVII в. в трудах М.В. Ломоносова. Строгое развитие эта наука получила в XIX в. и связана с работами Клаузиуса, Максвелла, Больцмана и др.
Для построения молекулярно-кинетической теории надо знать размеры атомов. Оценки показывают, что размеры атомов порядка нескольких ангстрем. Ангстрем - это внесистемная единица длины, 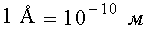 .
.
Число атомов или молекул в любом макроскопическом теле огромно. Например, найденное опытным путем число атомов в 12 г изотопа углерода 12С равно 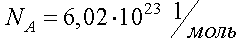 . Это число называется числом Авогадро.
. Это число называется числом Авогадро.
В молекулярной физике вводится единица количества вещества - моль (в системе СИ).
Один моль - это количество вещества, в котором содержится столько же молекул (или атомов), сколько атомов содержится в углероде массой 0,012 кг. Отсюда следует: в одном моле любого вещества содержится одинаковое число атомов или молекул, это число называется числом Авогадро.
Так как массы атомов очень малы, удобно использовать в расчетах не массы, измеренные в килограммах, а относительные массы. Относительной молекулярной (или относительной атомной) массой называют отношение массы молекулы (или атома) вещества к  массы атома углерода. Относительные атомные массы указаны в таблице Менделеева.
массы атома углерода. Относительные атомные массы указаны в таблице Менделеева.
Наряду с относительной молекулярной массой в физике и химии используется понятие молярная масса. Молярная масса вычисляется как масса одного моля вещества, выраженная в килограммах (в системе СИ). Например, молекулярная масса воды (Н2О) находится с помощью таблицы Менделеева и равна
М = 1 ∙ 2 + 16 = 18.
Молярная масса воды 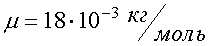 .
.
|
|
|
|
Дата добавления: 2014-01-07; Просмотров: 347; Нарушение авторских прав?; Мы поможем в написании вашей работы!